Nyt system tillader hurtig reaktion på hjerteanfald, begrænser hjerteskader
Kredit: ACS Nano
Forskere fra North Carolina State University og University of North Carolina i Chapel Hill har udviklet et lægemiddelleveringssystem, der tillader hurtig reaktion på hjerteanfald uden kirurgisk indgreb. I laboratorie- og dyreforsøg, systemet viste sig at være effektivt til at opløse blodpropper, begrænsning af langvarig ardannelse til hjertevæv og bevarer mere af hjertets normale funktion.
"Vores tilgang ville gøre det muligt for sundhedsudbydere at begynde at behandle hjerteanfald, før en patient når en kirurgisk suite, forhåbentlig forbedre patientresultaterne, " siger Ashley Brown, tilsvarende forfatter til et papir om arbejdet og en adjunkt i Joint Biomedical Engineering Program (BME) ved NC State og UNC. "Og fordi vi er i stand til at målrette blokeringen, vi er i stand til at bruge stærke stoffer, der kan udgøre en trussel mod andre dele af kroppen; målretningen reducerer risikoen for utilsigtede skader."
Hjerteanfald, eller myokardieinfarkter, opstår, når en trombe – eller blodprop – blokerer et blodkar i hjertet. For at behandle hjerteanfald, læger udfører ofte kirurgi for at indføre et kateter til blodkarret, giver dem mulighed for fysisk at bryde op eller fjerne tromben. Men ikke alle patienter har hurtig adgang til kirurgisk behandling.
Og der kan opstå flere skader, selv efter at blokeringen er blevet fjernet. Det er fordi tilbagevenden af frisk blod til væv, der var blevet blokeret af, kan forårsage skade i sig selv, kaldet reperfusionsskade. Reperfusionsskade kan forårsage ardannelse, afstivning af hjertevæv og begrænsning af hjertets normale funktionalitet.
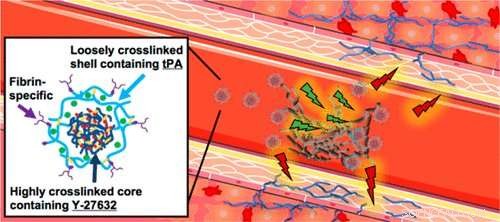
For at løse disse problemer, forskere har udviklet en løsning, der er afhængig af porøse nanogelkugler, omkring 250 nanometer i diameter, som målretter mod en trombe og afgiver en cocktail af to lægemidler:tPA og Y-27632.
En trombe kan være lavet af forskellige stoffer, såsom blodplader eller arterielle plaques, men de indeholder alle et stof, der hedder fibrin. Så, at målrette mod blokeringer, hver nanogel er belagt med proteiner, der binder specifikt til fibrin. Med andre ord, når nanogelerne når en trombe, de holder fast.
tPA og Y-27632 er lagdelt inde i nanosfæren, med tPA, der danner en skal, der omgiver Y-27632. Som resultat, tPA lækker først ud ved trombestedet, lader den gøre sit arbejde - som er at nedbryde fibrin og opløse koaguleret.
Efterhånden som tPA frigives, Y-27632 undslipper nanogelen. Mens tPA'en retter sig mod selve blodproppen, Y-27632 har til formål at begrænse skaden forårsaget af reperfusionsskade. Det gør den ved at begrænse stivheden af cellerne i området, der bidrager til ardannelse. Dette gør det muligt for disse celler at bevare mere af deres plasticitet, forbedre deres evne til at fungere normalt og bevare mere hjertefunktion.
In vitro test, forskerne fandt, at den målrettede tPA/Y-27632 cocktail opløste blodpropper i løbet af få minutter. Selvom dette endnu ikke er testet i forsøg, det kan virke hurtigere end kirurgiske indgreb, som kræver tid til at forberede patienten og få kateteret på plads.
I forsøg med laboratorierotter, forskerne fandt også ud af, at deres teknik begrænsede ardannelse og bevarede hjertefunktionen efter hjerteanfald bedre end målrettet tPA eller Y-27632 alene – og langt bedre end en kontrolgruppe, hvor dyrene ikke fik nogen af stofferne.
Specifikt, dyr, der modtog den målrettede cocktail, havde en venstre ventrikulær ejektionsfraktion, som måler et hjertes funktionalitet, på omkring 67 procent fire uger efter hjerteanfaldet - hvilket er sundt. tPA i sig selv var omkring 57 procent, som er i den lave ende af normalområdet, mens både kontrolgruppen og Y-27632 af sig selv dykkede ned i 40'erne. Tilsvarende den målrettede cocktail resulterede i arvæv over mindre end 5 procent af det berørte område. tPA og Y-27632 havde arvæv på tværs af cirka 7 procent af området, med kontrolgruppen, der så ardannelse på tværs af mere end 10 procent.
Hvad mere er, forskerne fandt ud af, at de målrettede nanogeler resulterede i, at kun få eller ingen af nanogelerne blev fundet i andre væv – såsom lunger og lever – især sammenlignet med brugen af de ikke-målrettede nanogeler.
"Dette er en vigtig del af vores resultater, fordi tPA og Y-27632 begge kan udgøre risici, hvis de begynder at virke på dele af kroppen uden for målområdet, " siger Brown. "F.eks. tPA kan forårsage blødning, og Y-27632 kan påvirke mange væv, hvor cellesammentrækning er nødvendig for normal funktion."
En anden fordel ved de målrettede nanogeler er, at på grund af deres lille størrelse, de kan målrette selv de blodkar, der er for små til at nå ved hjælp af katetre.
Forskerne bemærker også, at der er tale om et præklinisk studie. De næste trin for arbejdet omfatter yderligere evaluering af nanogelernes sikkerhed og test i større dyremodeller.
"Mens vi stadig er i de tidlige stadier af udviklingen af denne teknologi, vi ved, at det er vigtigt at anerkende problemer relateret til omkostninger, " siger Brown. "I betragtning af kompleksiteten af lægemiddelleveringssystemet, det burde være sammenligneligt med eller lidt dyrere end rekombinante proteinterapier, der i øjeblikket er i klinisk brug - såsom tPA i sig selv. Imidlertid, fordi stofferne er målrettet, doserne er sandsynligvis mindre. Det skulle være med til at holde omkostningerne sammenlignelige med eksisterende lægemidler på markedet."
Papiret, "Målrettet behandling af iskæmiske og fibrotiske komplikationer af myokardieinfarkt ved hjælp af et mikrogel-terapi med dobbelt levering, " er offentliggjort i tidsskriftet ACS Nano .
 Varme artikler
Varme artikler
-
 Arrays af små koniske spidser, der skubber ioniserede materialer ud, kunne fremstille enheder i nan…Til venstre er en tæt række af elektrospray-emittere (1, 900 emittere i 1 kvadratcentimeter). Til højre er et nærbillede af en enkelt sender, dækket af en skov af kulstofnanorør. Kredit:Journal of Mic
Arrays af små koniske spidser, der skubber ioniserede materialer ud, kunne fremstille enheder i nan…Til venstre er en tæt række af elektrospray-emittere (1, 900 emittere i 1 kvadratcentimeter). Til højre er et nærbillede af en enkelt sender, dækket af en skov af kulstofnanorør. Kredit:Journal of Mic -
 At genoverveje grundlæggende videnskab om grafensyntese viser vejen til produktion i industriel ska…En ny vej til fremstilling af grafen er blevet opdaget, der kunne gøre det 21. århundredes vidundermateriale lettere at rampe op til industriel skala. grafen, som har super styrke og evnen til at lede
At genoverveje grundlæggende videnskab om grafensyntese viser vejen til produktion i industriel ska…En ny vej til fremstilling af grafen er blevet opdaget, der kunne gøre det 21. århundredes vidundermateriale lettere at rampe op til industriel skala. grafen, som har super styrke og evnen til at lede -
 Studiet undersøger spontan symmetribrud i snoet dobbelt-dobbelt-grafenIllustration af et moiré-mønster, der fremkommer ved stabling og rotation af to ark tolagsgrafen. Korrelerede elektroniske tilstande med magnetisk orden opstår i snoet dobbelt-dobbelt-grafen over et l
Studiet undersøger spontan symmetribrud i snoet dobbelt-dobbelt-grafenIllustration af et moiré-mønster, der fremkommer ved stabling og rotation af to ark tolagsgrafen. Korrelerede elektroniske tilstande med magnetisk orden opstår i snoet dobbelt-dobbelt-grafen over et l -
 Som papir, grafen vrider og foldes til maskiner i nanoskalagrafen, ligesom papirmodellerne, er stærk men fleksibel, og kan strækkes eller trækkes med kræfter sammenlignelige med dem udøves af motorproteiner. Kredit: Joe Wilensky/Cornell Chronicle Kunsten
Som papir, grafen vrider og foldes til maskiner i nanoskalagrafen, ligesom papirmodellerne, er stærk men fleksibel, og kan strækkes eller trækkes med kræfter sammenlignelige med dem udøves af motorproteiner. Kredit: Joe Wilensky/Cornell Chronicle Kunsten
- Konstrueret gær kunne udvide biobrændstoffers rækkevidde
- Regn, der bryder bagsiden af den australske bushbrandskrise
- Trump sætter bremser på køretøjets emissionsmål
- Hvad er termisk teknologi?
- Sådan tilsluttes en 480V, 208V eller 120V transformer
- USA anklager Facebook for højteknologisk boligdiskrimination


