Programmerbare legos af DNA og protein byggesten skaber nye 3-D bure
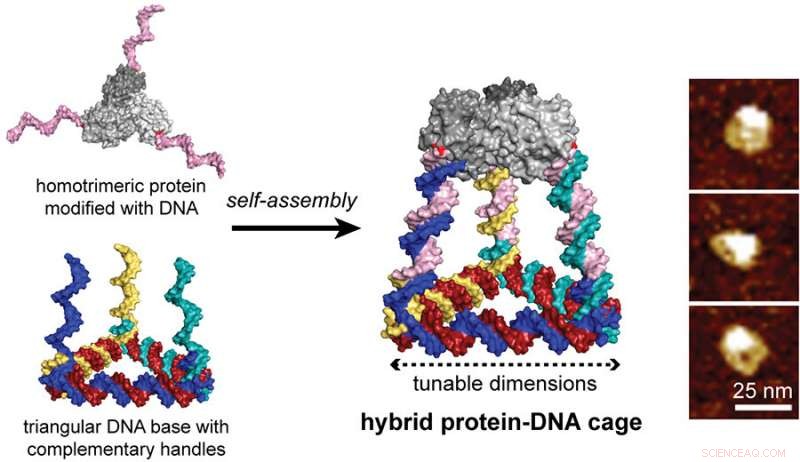
Dette protein-DNA 'Lego' blev samlet med en trekantet DNA-struktur, der bærer tre komplementære arme til håndtagene, hvilket resulterer i tetraedriske bure bestående af seks DNA-sider, der er dækket af proteintrimeren. Kredit:Nicholas Stephanopoulos
Det centrale mål for nanoteknologi er manipulation af materialer på atom- eller molekylær skala, især til at bygge mikroskopiske enheder eller strukturer. Tredimensionelle bure er et af de vigtigste mål, både for deres enkelhed og deres anvendelse som lægemiddelbærere til medicin. DNA-nanoteknologi bruger DNA-molekyler som programmerbare "Legos" til at samle strukturer med en kontrol, der ikke er mulig med andre molekyler.
Imidlertid, DNA-strukturen er meget enkel og mangler den mangfoldighed af proteiner, der udgør de fleste naturlige bure, som vira. Desværre, det er meget vanskeligt at kontrollere samlingen af proteiner med nøjagtigheden af DNA. Det er, indtil for nylig. Nicholas Stephanopoulos - en assisterende professor i Arizona State University's Biodesign Center for Molecular Design and Biomimetics, og School of Molecular Sciences - og hans team byggede et bur konstrueret af både protein- og DNA-byggesten ved brug af kovalente protein-DNA-konjugater.
I et blad udgivet i ACS Nano , Stephanopoulos modificerede et homotrimert protein (et naturligt enzym kaldet KDPG aldolase) med tre identiske enkeltstrengede DNA-håndtag ved at funktionalisere en reaktiv cysteinrest, de introducerede på proteinoverfladen. Dette protein-DNA "Lego" blev sammensat med en trekantet DNA-struktur, der bærer tre komplementære arme til håndtagene, hvilket resulterer i tetraedriske bure bestående af seks DNA-sider, der er dækket af proteintrimeren. Dimensionerne af buret kunne indstilles gennem antallet af omdrejninger pr. DNA-arm, og hybridstrukturerne blev oprenset og karakteriseret for at bekræfte den tredimensionelle struktur.
Bure blev også modificeret med DNA ved hjælp af klikkemi, som er en tilpasset type kemi, at skabe elementer hurtigt med stor pålidelighed ved at samle mikroskopiske enheder, hvilket demonstrerer metodens almene karakter.

Adjunkt Nicholas Stephanopoulos. Kredit:Nicholas Stephanopoulos
"Mit laboratoriums tilgang vil give mulighed for konstruktion af nanomaterialer, der besidder fordelene ved både protein- og DNA-nanoteknologi, og find applikationer inden for områder som målrettet levering, strukturel biologi, biomedicin, og katalytiske materialer, " sagde Stephanopoulos.
Stephanopoulos og hans team ser en mulighed med hybridbure – sammensmeltning af selvsamlende proteinbyggesten med et syntetisk DNA-stillads – der kan kombinere førstnævntes bioaktivitet og kemiske mangfoldighed med programmerbarheden af sidstnævnte. Og det er, hvad de satte sig for at skabe - en hybridstruktur konstrueret gennem kemisk konjugation af oligonukleotid (en syntetisk DNA-streng) håndtag på en proteinbyggesten. Den trekantede base, der bærer tre komplementære enkeltstrengede DNA-håndtag, samles selv og renses separat ved at opvarme den for at ændre dens egenskaber.
"Vi ræsonnerede, at ved at designe disse to rensede byggeklodser, de ville spontant klikke sammen på en programmerbar måde, ved at bruge DNA-håndtagenes genkendelsesegenskaber, " sagde Stephanopoulos. "Det var især vigtigt at bruge et meget termisk stabilt protein som denne aldolase, fordi denne selvsamling kun fungerer ved 55 grader Celsius, og mange proteiner falder fra hinanden ved disse temperaturer."
En anden fordel ved DNA, hvilket ikke er muligt med proteiner, justerer burstørrelsen uden at skulle redesigne alle komponenterne. Stephanopoulos fortsatte, "Størrelsen af denne samling kunne derefter rationelt indstilles ved at ændre længden af hver DNA-kant, hvorimod proteinet ville udgøre et stillads til vedhæftning af små molekyler, målrettet mod peptider eller endda fusionsproteiner."
Mens der findes andre eksempler på hybridstrukturer, dette særlige bur er det første, der er konstrueret gennem kemisk konjugation af oligonukleotidhåndtag på en proteinbyggesten. Denne strategi kan i princippet udvides til en bred vifte af proteiner (nogle med evner til målretning mod kræft, for eksempel). Dermed, Stephanopoulos' arbejde har potentialet til at muliggøre et helt nyt hybridfelt inden for protein-DNA-nanoteknologi med anvendelser, der ikke er mulige med hverken proteiner eller DNA alene.
 Varme artikler
Varme artikler
-
 Gør carbon nanorør lige så anvendelige som almindelig plastFire kontinuerlige tilstande af (a) carbon nanorørpulvere i cresolbaseret opløsningsmiddel:b) en fortyndet dispersion til støbning af tynde film, c) en tyk pasta til skovlbelægning maleri, silketryk e
Gør carbon nanorør lige så anvendelige som almindelig plastFire kontinuerlige tilstande af (a) carbon nanorørpulvere i cresolbaseret opløsningsmiddel:b) en fortyndet dispersion til støbning af tynde film, c) en tyk pasta til skovlbelægning maleri, silketryk e -
 Den næste generation af kulilte nanosensorerTilpasning af et scanningselektronmikroskopibillede af kobberoxidnanotråde, der bygger bro mellem nabokobbermikrostrukturer Detektion af kulilte (CO) i luften er et vigtigt spørgsmål, da CO er en
Den næste generation af kulilte nanosensorerTilpasning af et scanningselektronmikroskopibillede af kobberoxidnanotråde, der bygger bro mellem nabokobbermikrostrukturer Detektion af kulilte (CO) i luften er et vigtigt spørgsmål, da CO er en -
 Kemisk billeddannende mikroskop viser korrugeret gamma-aluminiumoxid overfladeOverfladen af de pladelignende partikler er langt fra glat, ifølge en ny transmissionselektronmikroskopi-undersøgelse udført af Pacific Northwest National Laboratory og FEI Company. (Phys.org) –
Kemisk billeddannende mikroskop viser korrugeret gamma-aluminiumoxid overfladeOverfladen af de pladelignende partikler er langt fra glat, ifølge en ny transmissionselektronmikroskopi-undersøgelse udført af Pacific Northwest National Laboratory og FEI Company. (Phys.org) – -
 Sådan åbner du bløde nanopartikler ved hjælp af lydbølgerKredit:CC0 Public Domain Ultralyd har længe været et vigtigt værktøj til medicinsk billeddannelse. For nylig, medicinske forskere har vist, at fokuserede ultralydsbølger også kan forbedre levering
Sådan åbner du bløde nanopartikler ved hjælp af lydbølgerKredit:CC0 Public Domain Ultralyd har længe været et vigtigt værktøj til medicinsk billeddannelse. For nylig, medicinske forskere har vist, at fokuserede ultralydsbølger også kan forbedre levering
- Sådan beregnes lumen pr. Watt
- Næste trin i at simulere universet
- Forskere daterer alder af den ældste kendte skov i West Junggar-regionen, Kina
- Fremgangsmåden for et videnskabsmæssigt projekt på Gummi Egg
- ExoMars videnskabskassen er gennemført, og aerobraking begynder
- Hvordan man tegner tællere i Math


