På vej til nanotheranostics
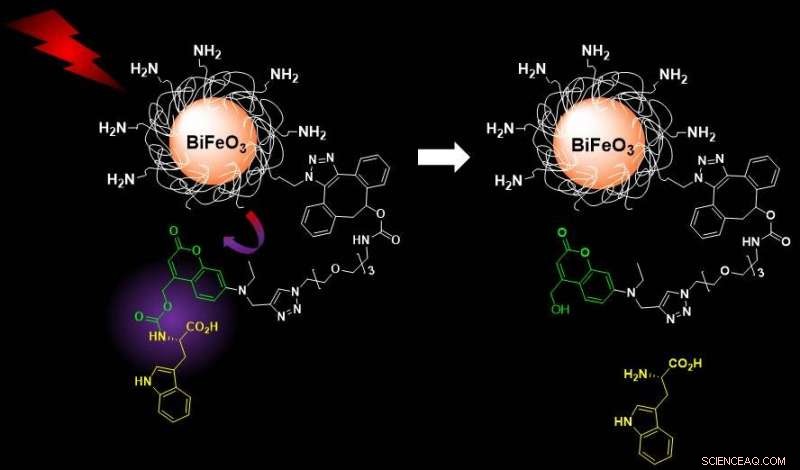
Nær-infrarød excitation af funktionaliserede bismuthferrit-nanopartikler resulterer i harmonisk emission, der udløser fotorelease af molekylære laster i bur, muliggør afkoblet billeddannelse og kontrollerede leveringsapplikationer. Kredit:S. Gerber/EPFL
Theranostics er et spirende område inden for medicin, hvis navn er en kombination af "terapeutik" og "diagnostik". Ideen bag theranostics er at kombinere medicin og/eller teknikker til samtidig - eller sekventielt - at diagnosticere og behandle medicinske tilstande, og også overvåge patientens reaktion. Dette sparer tid og penge, men kan også omgå nogle af de uønskede biologiske virkninger, der kan opstå, når disse strategier anvendes separat.
I dag, theranostics -applikationer bruger i stigende grad nanopartikler, der forener diagnostiske molekyler og lægemidler til et enkelt middel. Nanopartiklerne fungerer som bærere for molekylær "last, "fx et lægemiddel eller en radioisotop til kræftpatienter, der gennemgår strålebehandling, målrettet mod specifikke biologiske veje i patientens krop samtidig undgå skader på sunde væv.
En gang ved deres målvæv, nanopartiklerne producerer diagnostiske billeder og/eller leverer deres last. Dette er den nyeste teknologi inden for "nanotheranostics, "som er blevet et stort fokus for forskning - omend med mange begrænsninger at overvinde.
Nu, laboratoriet af Sandrine Gerber på EPFL, arbejder med fysikere ved universitetet i Genève, har udviklet et nyt nanotheranostisk system, der overvinder flere problemer med tidligere tilgange. Systemet anvender "harmoniske nanopartikler" (HNP'er), en familie af metaloxid-nanokrystaller med usædvanlige optiske egenskaber, især deres emission som reaktion på excitation fra ultraviolet til infrarødt lys, og deres høje fotostabilitet. Det var denne funktion, der bragte HNP'er til nanotheranostics, da forskere forsøgte at løse nogle problemer med fluorescerende sonder.
"De fleste lysaktiverede nanotheranostiske systemer har brug for UV-lys med høj energi for at begejstre deres fotoresponsive stilladser, "siger Gerber." Problemet er, at dette resulterer i dårlig indtrængningsdybde og kan skade levende celler og væv, hvilket begrænser biomedicinske anvendelser. "
Det nye system, som Gerbers gruppe udviklede, undgår disse problemer ved at bruge silica-belagte bismutferrit-HNP'er, der er funktionaliseret med lysreagerende molekylære laster i bur. Disse systemer kan let aktiveres med nær-infrarødt lys (bølgelængde 790 nanometer) og afbildes ved længere bølgelængde til både detekterings- og lægemiddelfrigivelsesprocesser. Begge disse funktioner gør systemet medicinsk sikkert for patienter.
Når lyset blev udløst, HNP'erne frigiver deres last - i dette tilfælde L-tryptophan, bruges som model. Forskerne overvågede og kvantificerede frigivelsen med en teknik, der kombinerer væskekromatografi og massespektrometri, dækker den billeddiagnostiske del af det nanotheranostiske system.
Forfatterne udtaler, at "dette arbejde er et vigtigt skridt i udviklingen af nanocarrier-platforme, der muliggør afkoblet billeddannelse i vævsdybde og frigivelse af terapier efter behov."
 Varme artikler
Varme artikler
-
 Smogædende grafenkomposit reducerer atmosfærisk forureningFotokatalysatoren nedbryder op til 70 % mere atmosfæriske nitrogenoxider (NOx) end standard titanium-nanopartikler i tests på rigtige forurenende stoffer. Kredit:Italcementi/Heidelberg Cement/Graphene
Smogædende grafenkomposit reducerer atmosfærisk forureningFotokatalysatoren nedbryder op til 70 % mere atmosfæriske nitrogenoxider (NOx) end standard titanium-nanopartikler i tests på rigtige forurenende stoffer. Kredit:Italcementi/Heidelberg Cement/Graphene -
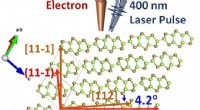 Ny indsigt i van der Waals materialer fundetGitterdynamikken for monoklinisk galliumtellurid (GaTe) undersøges ved ultrahurtig elektrodiffraktion (UED). Denne undersøgelse giver en generel forståelse af Friedels lov og en omfattende forklaring
Ny indsigt i van der Waals materialer fundetGitterdynamikken for monoklinisk galliumtellurid (GaTe) undersøges ved ultrahurtig elektrodiffraktion (UED). Denne undersøgelse giver en generel forståelse af Friedels lov og en omfattende forklaring -
 Fremskynder selvsamling af nanoskala mønstre til næste generations materialerMaterialeforsker Gregory Doerk forbereder en prøve til elektronmikroskopi ved Brookhaven Labs Center for Functional Nanomaterials. Scanningselektronmikroskopbilledet på computerskærmen viser et tværsn
Fremskynder selvsamling af nanoskala mønstre til næste generations materialerMaterialeforsker Gregory Doerk forbereder en prøve til elektronmikroskopi ved Brookhaven Labs Center for Functional Nanomaterials. Scanningselektronmikroskopbilledet på computerskærmen viser et tværsn -
 Sekvens det ... og de vil kommeScanning Electron Micrograph (SEM) af nål og tråd. Kredit:Public Domain Image Hurtig DNA-sekventering kan snart blive en rutinemæssig del af hver enkelt persons journal, leverer enorm information,
Sekvens det ... og de vil kommeScanning Electron Micrograph (SEM) af nål og tråd. Kredit:Public Domain Image Hurtig DNA-sekventering kan snart blive en rutinemæssig del af hver enkelt persons journal, leverer enorm information,
- En kæde i Mælkevejen forbundet med galaktisk kollision
- Meteoritternes oprindelse peger på mulig uopdaget asteroide
- Grundlæggende Dele af en DC Generator
- Integreret brintlager til brændselscellebiler
- Forskere afslører fælles oprindelse af Fermi-bobler og galaktiske centre røntgenudstrømninger
- Europarådet undersøger AI for at omforme fængsler


