Sekvens det ... og de vil komme
Scanning Electron Micrograph (SEM) af nål og tråd. Kredit:Public Domain Image
Hurtig DNA-sekventering kan snart blive en rutinemæssig del af hver enkelt persons journal, leverer enorm information, der tidligere var sekvestreret i det menneskelige genoms 3 milliarder nukleotidbaser. Denne uges NYHEDSFOKUS sektion af tidsskriftet Videnskab beskriver de seneste fremskridt inden for sekventeringsteknologi.
Stuart Lindsay, direktør for Biodesign Instituttets Center for Single Molecule Biophysics, er på forkant med denne forskning, har med succes adresseret en central anstødssten i nanopore-sekventering - læsning af enkelt nukleotidbaser i en DNA-kæde. Lindsays seneste eksperimentelle resultater, som viser kritiske forbedringer i DNA-aflæsninger, er netop dukket op i journalen Nanoteknologi .
Når den nøjagtige sekvensering falder under tærsklen på $1, 000 pr. genom, teknologien bør blive allestedsnærværende, ifølge mange. Som den nuværende videnskabsoversigt antyder, den dag kan nærme sig, da både hastigheden og omkostningerne ved hele genomsekventering udvikler sig i et tempo, der overgår Moores berømte lov, (hvilket tilsiger en fordobling af computerkraften – og halvering af udgifterne – hver 18. måned).
Den seneste teknologiske konkurrence involverer ideen om at føre en enkelt DNA-streng gennem en lille, Øje i molekylær skala kendt som en nanopore. Denne strategi kan snart tillade, at hele DNA-sekvensen kan læses på én gang, i stedet for at skære fra hinanden, tydet i korte fragmenter og møjsommeligt samlet igen.
Mens den første sekventering af det menneskelige genom tog forskere 13 år og 3 milliarder dollars at opnå, i regi af Human Genome Project, bedriften kan snart opnås med den blændende hastighed på 6 milliarder nukleotidbaser hver 6. time til en pris af $900. Det er i hvert fald den ekstravagante påstand, som Oxford Nanopore Technologies fremsætter, en af de banebrydende virksomheder, der driver nye sekventeringsudviklinger.
Siden den tilsyneladende quixotiske idé om nanopore-sekventering først blev tænkt på i midten af 1990'erne, der er gjort enorme fremskridt. Den grundlæggende idé er, at når en nanopore nedsænkes i en ledende væske, og der påføres en spænding over den, ledning af ioner gennem nanoporen vil producere en målbar elektrisk strøm. Denne strøm er meget følsom over for størrelsen og formen af nanoporen og i teorien, hver nukleotidbase i DNA-tråden vil blokere nanoporen, når den migrerer, ændre ionstrømmen på en genkendelig og reproducerbar måde.
DNA-"tråden" er dog et vanskeligt materiale at manipulere - så fint, at det ville tage omkring 5000 DNA-strenge lagt side om side for at svare til bredden af et menneskehår. Bare det at finde et passende øje i denne skala viste sig at være en udfordring. I første omgang, porøs, transmembrane proteiner blev undersøgt. Alfa hæmolysin (αHL), en bakterie, der forårsager lysis af røde blodlegemer, virkede som en særdeles lovende kandidat, givet den nanopore-diameter, der kræves til sekventering af DNA.
Siden da, andre proteinbaserede portaler til DNA er blevet pillet ved og for nylig, forskellige "solid state" nanoporer af silicium eller grafen er blevet undersøgt. Disse kan lettere fremstilles og deres egenskaber, mere præcist kontrolleret.
Ifølge Science's gennemgang af den nuværende state of the art, nanopore-sekventering "ser ud til at være klar til at forlade laboratoriet, ” og drømmen om et $1000-genom kan være lige ved hånden, selvom der stadig er udfordringer. Et vedvarende problem ved sekventering af individuelle baser har været, at de har tendens til at strømme gennem nanoporen for hurtigt til at lokalisere hver base uafhængigt. I stedet, den målte strøm i tidlige eksperimenter afspejlede gennemsnittet produceret af en gruppe baser, der bevægede sig gennem tunnelen.
Lindsays teknik bygger på at aflæse elektrisk strøm i et lille kredsløb bestående af et DNA-nukleotid fanget mellem et par guldelektroder, som spænder over en nanopore. Elektroderne er lavet ved at funktionalisere spidsen af et scanning tunneling mikroskop (STM), med molekyler, der kan binde individuelle DNA-baser, når de stikker hovedet gennem nanoporen.
Anerkendelsestunneling, navnet Lindsay gælder for hans sekventeringsmetode, er afhængig af at udstyre en af to elektroder med følerkemikalier, den anden med nukleotidmålet, der skal sanses. Et signal produceres, når krydset mellem sensing af kemikaliet og målet samler sig selv, at lukke kredsløbet.
I denne type kryds, hvor længder, der adskiller elektroder, er nede på en molekylær skala, elektroner kan udvise mærkelig adfærd forbundet med den kvante subatomære verden, "tunneling" gennem barrierer under forhold, der er forbudt af klassisk fysik. I et sådant scenarie, hver af de 4 nukleotider skal producere en signatur tunnelstrøm, som kan bruges til at sekventere DNA base-for-base, når det fodrer sig vej gennem nanoporen. At fange hver base kortvarigt giver tid til en nøjagtig identifikation, før den frigives og DNA-tråden fortsætter sin transmigrering gennem nanoporen.
Udskiftning af ionstrøm med tunnelstrøm kan potentielt forbedre sekvensopløsningen betydeligt og i deres seneste arbejde, Lindsays gruppe viser, at multiparameteranalyse af de strømspidser, der produceres ved tunnelering, faktisk kan identificere hver DNA-base, da den midlertidigt er fastgjort af hydrogenbinding mellem de funktionaliserede elektroder.
Der er mere.
Ud over at udpege nukleotididentitet med mere end 90 procent nøjagtighed, Teknikken gør det også muligt at identificere miljøgenmodifikationer, for eksempel, methylering. Dette repræsenterer et stort fremskridt for sekventering, da sådanne epigenetiske ændringer af genomet har dybtgående konsekvenser for studiet af menneskers sundhed og sygdom, herunder embryonal og postnatal udvikling, og kræft.
Nanoteknologi-papiret beskriver en ny tilgang til at analysere tunnelsignalerne. Lindsay-gruppen brugte maskinlæring (processen brugt af IBMs Watson til at vinde ved Jeopardy) til at træne en computer til at genkende DNA-baserne. Maskinen kaldte alle fire baser (A, T, C og G) samt den "femte base" - methyl - der bærer den epigenetiske kode, med 96 procent nøjagtighed på et enkelt molekyle aflæst.
"Oxford Nanopore har lavet et enormt gennembrud inden for nanopore-sekventering ved hjælp af ionstrøm, som fremhævet i NEWSFOCUS-historien, " siger Lindsay. "Men vi tror, vi kan bringe endnu mere til bordet med den overfølsomhed og kemiske opløsning af Recognition Tunneling."
Roche Pharmaceuticals har for nylig licenseret teknologien.
High stakes kapløbet om hurtig sekventering ser ud til at være på vej ind på hjemmebane, selvom nye overraskelser sandsynligvis er før målstregen. Når den først er krydset, æraen for personlig medicin vil være ankommet. Mange nye indsigter i det genomiske grundlag for menneskers sundhed og sygdom vil næsten helt sikkert følge.
 Varme artikler
Varme artikler
-
 Kontrolleret emission og rumlig opsplitning af elektronpar demonstreretÆtset halvledende kanal med elektronkilde (A) og barriere (B). Elektronparrene udsendes af kilden og opdeles ved barrieren i to separate elektriske ledere (pil). Kredit:PTB I kvanteoptik, at gener
Kontrolleret emission og rumlig opsplitning af elektronpar demonstreretÆtset halvledende kanal med elektronkilde (A) og barriere (B). Elektronparrene udsendes af kilden og opdeles ved barrieren i to separate elektriske ledere (pil). Kredit:PTB I kvanteoptik, at gener -
 Proces udviklet til ultratynde kulstofmembranerVed hjælp af en ny proces har teamet, der arbejder med professor Dr. Armin Gölzhäuser, produceret tolv forskellige nanomembraner. De tre billeder er lavet ved hjælp af Bielefeld Helium Ion Microscope
Proces udviklet til ultratynde kulstofmembranerVed hjælp af en ny proces har teamet, der arbejder med professor Dr. Armin Gölzhäuser, produceret tolv forskellige nanomembraner. De tre billeder er lavet ved hjælp af Bielefeld Helium Ion Microscope -
 Quantum dot-teknologi kan være med til at belyse fremtidenDen orange farve i bogstaverne OSU er fremstillet af kvanteprikker set under et mikroskop, da de absorberer blåt lys og udsender lyset som orange - en illustration af nogle af potentialerne ved ny tek
Quantum dot-teknologi kan være med til at belyse fremtidenDen orange farve i bogstaverne OSU er fremstillet af kvanteprikker set under et mikroskop, da de absorberer blåt lys og udsender lyset som orange - en illustration af nogle af potentialerne ved ny tek -
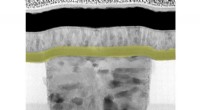 Nye hjernecellelignende nanoenheder arbejder sammen for at identificere mutationer i viraEt elektronmikrografi af den kunstige neuron. Niobiumdioxidlaget (gult) giver enheden neuronlignende adfærd. Kredit:Dr. R. Stanley Williams I septembernummeret af tidsskriftet Natur, forskere fr
Nye hjernecellelignende nanoenheder arbejder sammen for at identificere mutationer i viraEt elektronmikrografi af den kunstige neuron. Niobiumdioxidlaget (gult) giver enheden neuronlignende adfærd. Kredit:Dr. R. Stanley Williams I septembernummeret af tidsskriftet Natur, forskere fr
- Hvilken rolle spiller svampe i madkæder?
- ALMA ser den fjerneste støvede galakse skjult i almindeligt syn
- Klare ligheder mellem Boeing-ulykker i Etiopien, Indonesien
- Røntgenbilleder af menneskeskalle for at forbedre militærhjelme
- Forskere udvikler vaccine mod angreb på maskinlæring
- Ny model for stabilitet af Fannie Mae og Freddie Mac


