Nanokæder kan øge batterikapaciteten, reducere opladningstiden
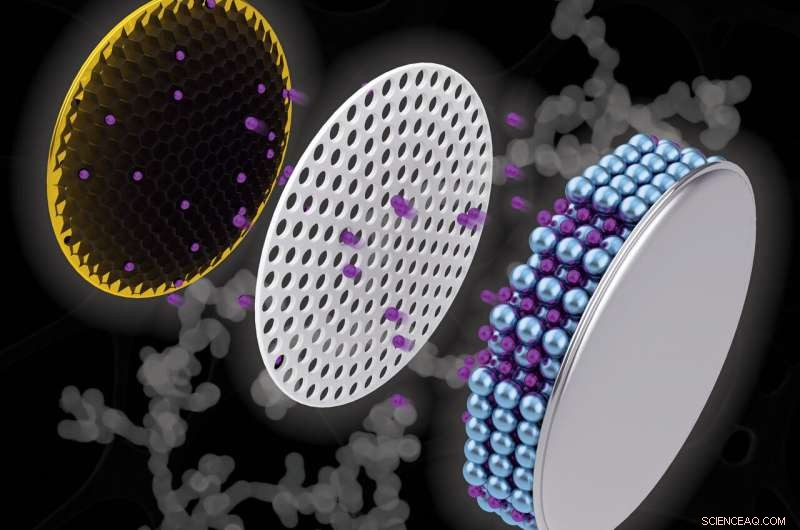
Kunstnerisk skildring af et møntcellebatteri med en kobberelektrode (til venstre) indeholdende en sort nanokædestruktur, som forskere har opdaget kan øge kapaciteten af et batteri og reducere opladningstiden. Kredit:Purdue University illustration/Henry Hamann
Hvor længe batteriet på din telefon eller computer holder afhænger af, hvor mange lithium-ioner der kan opbevares i batteriets negative elektrodemateriale. Hvis batteriet løber tør for disse ioner, den kan ikke generere en elektrisk strøm til at køre en enhed og fejler i sidste ende.
Materialer med en højere lithiumion-lagringskapacitet er enten for tunge eller den forkerte form til at erstatte grafit, det elektrodemateriale, der i øjeblikket bruges i nutidens batterier.
Forskere og ingeniører fra Purdue University har introduceret en potentiel måde, hvorpå disse materialer kan omstruktureres til et nyt elektrodedesign, der vil give dem mulighed for at forlænge et batteris levetid, gør den mere stabil og forkort dens opladningstid.
Studiet, vises som forsiden af septembernummeret af Anvendte nanomaterialer , skabt en netlignende struktur, kaldet en "nanokæde, "af antimon, en metalloid, der er kendt for at forbedre lithium-ion-opladningskapaciteten i batterier.
Forskerne sammenlignede nanochain-elektroderne med grafitelektroder, fandt ud af, at når møntcellebatterier med nanochain-elektroden kun blev opladet i 30 minutter, de opnåede det dobbelte af lithium-ion-kapaciteten for 100 opladnings-afladningscyklusser.
Nogle typer kommercielle batterier bruger allerede kul-metal-kompositter, der ligner antimonmetal negative elektroder, men materialet har en tendens til at udvide sig op til tre gange, når det optager lithiumioner, hvilket får det til at blive en sikkerhedsrisiko, når batteriet oplades.

En ny metode kunne gøre det muligt for bedre materialer at udgøre batterielektroder ved at konvertere dem til en nanokædestruktur, det sorte materiale på denne kobberelektrode af en møntcelle. Kredit:Purdue University /Kayla Wiles
"Du vil gerne rumme den type udvidelse i dine smartphone-batterier. På den måde bærer du ikke rundt på noget usikkert, " sagde Vilas Pol, en Purdue lektor i kemiteknik.
Ved at anvende kemiske forbindelser - et reduktionsmiddel og et kernedannende middel - forbandt Purdue-forskere de bittesmå antimonpartikler til en nanokædeform, der ville rumme den nødvendige ekspansion. Det særlige reduktionsmiddel holdet brugte, ammoniak-boran, er ansvarlig for at skabe de tomme rum - porerne inde i nanokæden - der rummer ekspansion og undertrykker elektrodefejl.
Holdet anvendte ammoniak-boran på flere forskellige forbindelser af antimon, fandt ud af, at kun antimon-chlorid producerede nanokædestrukturen.
"Vores procedure til at fremstille nanopartiklerne giver konsekvent kædestrukturerne, sagde P.V. Ramachandran, en professor i organisk kemi ved Purdue.
Nanokæden holder også lithiumionkapaciteten stabil i mindst 100 opladnings-afladningscyklusser. "Der er stort set ingen ændring fra cyklus 1 til cyklus 100, så vi har ingen grund til at tro, at cyklus 102 ikke vil være den samme, " sagde Pol.
Henry Hamann, en kandidatstuderende i kemi ved Purdue, syntetiserede antimon-nanokædestrukturen og Jassiel Rodriguez, en Purdue kemiingeniør postdoc-kandidat, testet den elektrokemiske batteriydelse.
Elektrodedesignet har potentialet til at være skalerbart til større batterier, siger forskerne. Holdet planlægger at teste designet i posecellebatterier næste gang.
 Varme artikler
Varme artikler
-
 Foldede DNA-skabeloner giver forskere mulighed for præcist at skære grafenformer ud, som kan bruge…Til venstre, metalliseret DNA (rødt) danner bogstaver på en grafenoverflade. Behandling med oxygenplasma ætser formen af bogstaverne ind i grafen, ret. Kredit:ZHONG JIN DNAs unikke struktur er i
Foldede DNA-skabeloner giver forskere mulighed for præcist at skære grafenformer ud, som kan bruge…Til venstre, metalliseret DNA (rødt) danner bogstaver på en grafenoverflade. Behandling med oxygenplasma ætser formen af bogstaverne ind i grafen, ret. Kredit:ZHONG JIN DNAs unikke struktur er i -
 Forskere bruger nanoteknologi til at jage efter skjulte patogenerDr. Saleh Naser arbejdede sammen med Dr. J. Manuel Perez for at udvikle en ny nanopartikelteknik, der en dag kan hjælpe læger med at diagnosticere visse tilstande hurtigere. Kredit:UCF Forskere ve
Forskere bruger nanoteknologi til at jage efter skjulte patogenerDr. Saleh Naser arbejdede sammen med Dr. J. Manuel Perez for at udvikle en ny nanopartikelteknik, der en dag kan hjælpe læger med at diagnosticere visse tilstande hurtigere. Kredit:UCF Forskere ve -
 Discovery vil tillade mere sofistikeret arbejde på nanoskalaForskere ledet af en ingeniør fra University of Houston har rapporteret om en ny måde at stimulere væskeflow på nanoskala ved at bruge en lille stigning i temperatur eller spænding. Kredit:ACS Applied
Discovery vil tillade mere sofistikeret arbejde på nanoskalaForskere ledet af en ingeniør fra University of Houston har rapporteret om en ny måde at stimulere væskeflow på nanoskala ved at bruge en lille stigning i temperatur eller spænding. Kredit:ACS Applied -
 Nano-velcro låser tungmetalmolekyler i sine greb© Northwestern University (Phys.org) – Forskere har udtænkt en enkel, system baseret på nanopartikler, at påvise kviksølv samt andre forurenende stoffer. Denne teknologi gør det muligt nemt og bil
Nano-velcro låser tungmetalmolekyler i sine greb© Northwestern University (Phys.org) – Forskere har udtænkt en enkel, system baseret på nanopartikler, at påvise kviksølv samt andre forurenende stoffer. Denne teknologi gør det muligt nemt og bil
- Materialeforskere former overfladen af små, buede kulfiber ved hjælp af laserstrukturering
- Ny forskning kan revolutionere fiberoptisk kommunikation
- Sådan fodres vilde fugle og doves
- Optøning af permafrost kan frigive mere CO2 end tidligere antaget, undersøgelse tyder på
- Hvorfor ændrer hydrater farve, når de opvarmes?
- Kunne hjorte holde spor om sammenhængen mellem malariaresistens og seglcelle?


