Elektrificerende videnskab:Ny undersøgelse beskriver ledning gennem proteiner
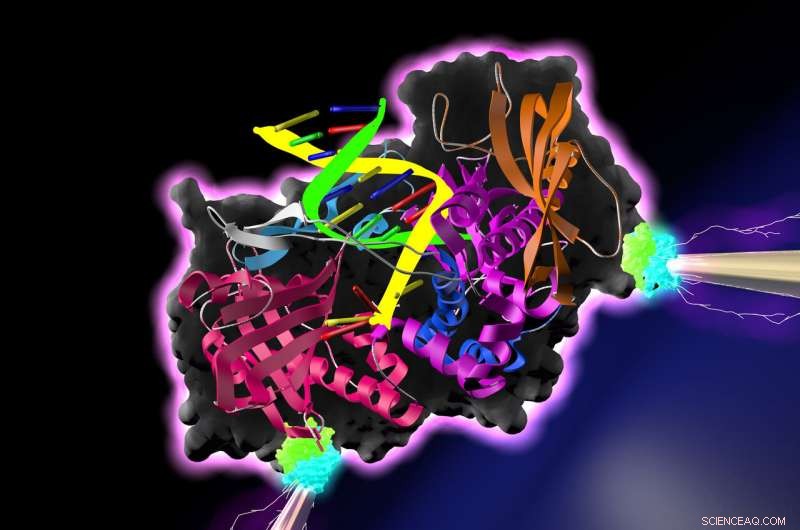
En DNA-polymerase - et enzym, der syntetiserer DNA-molekyler fra nukleotidbyggesten - er placeret mellem et par elektroder. Binding af nukleotider af polymerasen forårsager konduktansspidser, som kan være karakteristisk for de specifikke molekyler bundet af polymerasen. Sådan en anordning, i teorien, kunne udføre hurtigt, nøjagtig, lavpris DNA-sekventering, og kan have mange yderligere applikationer inden for medicinsk diagnostik, industriproduktion og andre områder. Kredit:Lindsay lab
Midt i den zoologiske have af biomolekyler, der er afgørende for livet, enzymer er blandt de mest vitale. Uden disse specialiserede proteiner, som fremskynder hastigheden af kemiske reaktioner, tusindvis af væsentlige livsprocesser, fra cellevækst og fordøjelse til respiration og nervefunktion, ville være umuligt.
I ny forskning, Stuart Lindsay og hans kolleger undersøger en nyligt opdaget bedrift udført af enzymer, og højst sandsynligt, alle proteiner. Under de rette forhold, de kan fungere som fremragende ledere af elektricitet, tillader dem at blive inkorporeret i en række elektroniske enheder. "Det er en måde at tilslutte den fantastiske kemiske mangfoldighed af enzymer direkte til en computer, " siger Lindsay.
Mens proteinkonduktansens rolle i naturen forbliver et spørgsmål om mystik og spekulation, udnyttelse af dette fænomen til menneskelig brug vil sandsynligvis åbne nye veje for biokemiske sensorenheder, smart industriel produktion og nye innovationer inden for medicinsk diagnostik.
Måske mest spændende, elektrisk ledningsevne gennem en særlig type enzym kan signalere et betydeligt fremskridt for DNA-sekventering. Ved hjælp af en DNA-polymerase, naturens egen højopløselige DNA-læser, i en sådan enhed kunne potentielt give mulighed for lynhurtig sekventering af hele menneskelige genomer med hidtil uset nøjagtighed til meget lave omkostninger. Den nye undersøgelse "åbner Pandoras æske med at se på funktionen af ethvert enzym i en computerchip."
Aktuelle anliggender
Forfatterne af det nye studie beskriver de tricks, de brugte til at fastgøre en DNA-polymerase til et par elektroder og de resulterende strømspidser, der er forbundet med, at enzymet successivt binder og frigiver mål-DNA-nukleotider. Den vellykkede demonstration af enzymledningsevne baner vejen for til sidst at montere arrays af proteiner på computerchips, hvor de kan fungere som biologiske parallelle processorer til en række forskellige opgaver.
"Enzymer er utrolige molekyler, der udfører kemiske reaktioner, som ellers bare ikke ville ske, " siger Lindsay. For at give en fornemmelse af kraften i disse molekyler, visse reaktioner afgørende for livsprocesser, udfolder sig tusindvis af gange i sekundet, ville kræve årtusinder at opstå i fravær af enzymer.
Lindsay leder Biosedign Center for Single Molecule Biophysics ved Arizona State University. Centrets primære forskning fokuserer på videnskab i sammenhængen mellem molekylær medicin og nanoteknologi.
Hans gruppes resultater vises i den kommende udgave af tidsskriftet ACS Nano .
Proteiner som ledere
Indtil for ganske nylig, proteiner blev strengt taget betragtet som isolatorer af elektrisk strøm. Nu, det ser ud til, deres usædvanlige fysiske egenskaber kan føre til en tilstand, hvor de er følsomt placeret mellem en isolator og en leder. (Et fænomen kendt som kvantekriticitet kan være kernen i deres ejendommelige adfærd.)
Ja, i tidligere forskning, Lindsay demonstrerede stærk elektrisk ledningsevne gennem et protein fanget mellem et par elektroder. Den nye forskning fører undersøgelserne af proteinkonduktans et skridt videre. Tidligere, proteinet blev koblet op via dets to såkaldte aktive steder. Dette er de områder af et protein, der binder udvalgte molekyler, resulterer ofte i en konformationsændring i molekylets komplekse 3-D struktur og fuldførelsen af proteinets givne opgave.
Denne gang, biomolekylet var følsomt forbundet til elektroderne ved hjælp af alternative bindingssteder på enzymet, efterlader de aktive steder tilgængelige til at binde molekyler og udføre naturlig proteinfunktion.
Naturens Kindle
Det enzymmolekyle, der er valgt til forsøgene, er et af de vigtigste for livet. Kendt som en DNA-polymerase, dette enzym binder med successive nukleotider i en længde af DNA og genererer en komplementær kæde af nukleotider, en efter en. Denne alsidige nanomaskine bruges i levende systemer til at kopiere DNA under cellereplikation samt til at reparere brud eller andre fornærmelser mod DNA'et.
Undersøgelsen beskriver teknikker til at fastgøre DNA-polymerasen til elektroder for at generere stærke konduktanssignaler ved hjælp af to specialiserede bindingskemikalier kendt som biotin og streptavidin. Når en elektrode blev funktionaliseret ved hjælp af denne teknik, små konduktansspidser blev genereret, da DNA-polymerasen successivt bandt og frigav hvert nukleotid, som en gribende hånd, der fanger og slipper en baseball. Når begge elektroder var udstyret med streptavidin og biotin, meget stærkere konduktanssignaler, måler 3-5 gange så stor, blev observeret.

Stuart Lindsay leder Biodesign Center for Single Molecule Biophysics. Han er også en Regents' Professor og Nadine og Edward Carson professor i fysik og kemi. Kredit:Biodesign Institute ved ASU
Ideen til at udnytte en polymerase til at udføre hurtig DNA-sekventering har været hos Lindsay i et stykke tid. Han havde overvejet at bruge det i tidligere enheder, han skabte, hvor dele af DNA blev fodret gennem smalle tunnelforbindelser. "Ville det ikke være pænt, hvis du kunne sætte et par elektroder inde i polymeraser, fordi polymerasen griber DNA'et og skubber det gennem krydset. Hvis du havde en udlæsningsmekanisme indlejret i polymerasen, du har den ideelle sekventeringsmaskine."
Den nye metode håber at tage en anden tilgang, ved at bruge polymerasens egen ekspertise i hurtiglæsning til at give en udlæsning af nukleotider gennem konduktansspidser, der er specifikke for hver af de 4 DNA-baser. I praksis, en række designhindringer skal overvindes. Korrekt vedhæftning af polymerasen til elektrisk ledningsevne er en delikat affære og involverede meget forsøg og fejl. Bindingssteder skal konstrueres på specifikke domæner, der ikke påvirker proteinfoldning og funktion, og forbindelser skulle udtænkes for at forhindre, at enzymet selv kommer i kontakt med elektroderne. Brugen af biotin til at binde molekylet ser også ud til at være kritisk for høj ledningsevne. Biotin, der binder en lomme af streptavidin, ser ud til at hjælpe med at drive elektrontransport dybt ind i proteinets indre, derved maksimerer ledningsevnen.
Adskillelse af konduktanssignaler, der registrerer hver successiv DNA-base fra baggrundsstøj og tilfældige bevægelser af kontaktpunkterne for enzymet, har også vist, at udfordrende og sofistikerede maskinlæringsalgoritmer bliver bragt i anvendelse for at tydeliggøre konduktansudlæsningerne. Lindsay mener, at mange af disse støjproblemer vil blive løst, når polymeraserne inkorporeres i korrekt isolerede og forseglede chips, der holder enzymet stift på plads.
Enzym grænser
Det første komplette menneskelige genom var en milepæl for videnskab og medicin. Den store indsats fra Human Genome Project forbrugte 13 års arbejdskraft til en pris af en milliard dollars. Nu åbner sluserne til en ny æra af proteinbioelektronik sig muligvis, med mange overraskelser i vente.
Hvis de resterende tekniske forhindringer kan overvindes, DNA-sekventering kunne udføres med den hæsblæsende hastighed af en funktionel DNA-polymerase, eller omkring hundrede nukleotider i sekundet. "Hvis du sætter 10, 000 molekyler på en chip - ikke en svær ting at gøre - du vil sekventere et helt genom på under en time, " siger Lindsay
 Varme artikler
Varme artikler
-
 Et fremskridt mod ultra-bærbare elektroniske enhederForskere rapporterer om et vigtigt fremskridt mod den længe ventede æra med enkeltmolekyleelektronik, når almindelige elektroniske kredsløb i computere, smartphones, lydafspillere, og andre enheder ka
Et fremskridt mod ultra-bærbare elektroniske enhederForskere rapporterer om et vigtigt fremskridt mod den længe ventede æra med enkeltmolekyleelektronik, når almindelige elektroniske kredsløb i computere, smartphones, lydafspillere, og andre enheder ka -
 Umklapp-spredning i supergitter fundet at forringe højtemperaturmobilitet af grafener ladningsbære…Denne visualisering viser lag af grafen, der bruges til membraner. Kredit:University of Manchester Et team af forskere fra Storbritannien, Japan og USA har fundet ud af, at Umklapp-spredning i moi
Umklapp-spredning i supergitter fundet at forringe højtemperaturmobilitet af grafener ladningsbære…Denne visualisering viser lag af grafen, der bruges til membraner. Kredit:University of Manchester Et team af forskere fra Storbritannien, Japan og USA har fundet ud af, at Umklapp-spredning i moi -
 Transistorer bygget af ultratynde 2D-materialer tager et skridt fremadKredit:CC0 Public Domain todimensionelle materialer kan bruges til at skabe mindre, højtydende transistorer traditionelt lavet af silicium, ifølge Saptarshi Das, assisterende professor i ingeniørv
Transistorer bygget af ultratynde 2D-materialer tager et skridt fremadKredit:CC0 Public Domain todimensionelle materialer kan bruges til at skabe mindre, højtydende transistorer traditionelt lavet af silicium, ifølge Saptarshi Das, assisterende professor i ingeniørv -
 Struktur af ny form for superhårdt kulstof identificeretVisninger langs [100]/[001], og retninger af 2x2x2 supercelle af bct-Carbon, de stiplede stiplede i (b) angiver den vinkelrette grafen-lignende struktur af bct-Carbon. Billedkredit:Xiang-Feng Zhou, ht
Struktur af ny form for superhårdt kulstof identificeretVisninger langs [100]/[001], og retninger af 2x2x2 supercelle af bct-Carbon, de stiplede stiplede i (b) angiver den vinkelrette grafen-lignende struktur af bct-Carbon. Billedkredit:Xiang-Feng Zhou, ht
- Hvordan fungerer trick fødselsdagslys?
- Labour-kulstoffattige varme hjem til alle kunne revolutionere sociale boliger – eksperter
- Hvordan man laver et simpelt kredsløb
- Forskere udvikler lagdelt koboltoxid med en rekordhøj termoelektrisk værdi
- Undersøgelse afslører nye spor om Mount Everests dødbringende lavine
- Folk passer bedre på offentlige steder, når de føler, at de har en andel i dem


