Nanocontainer sender genterapier og lægemidler af titanstørrelse ind i celler
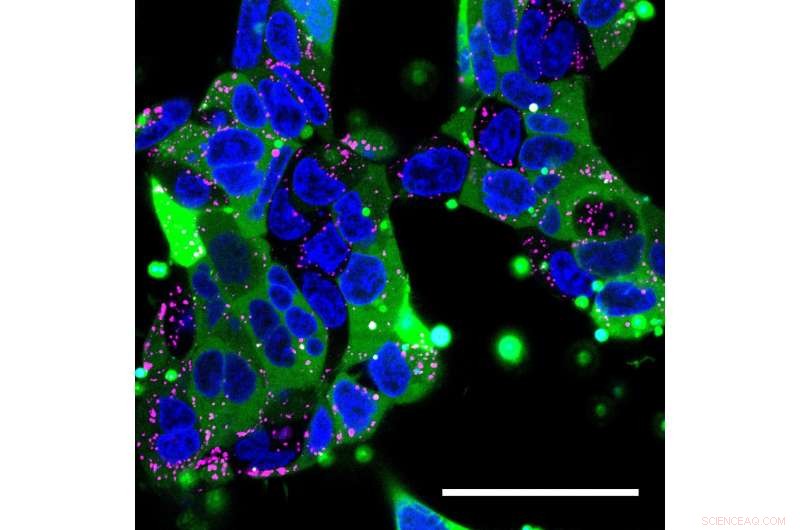
Konfokal mikroskopi billede af humane embryonale nyreceller. Nanopartikler fyldt med humant immunglobulin blev leveret til cellerne. Cellekernen er blå, endosomer (hvilke udskiller materialer optaget af celler) er mærket med pink, og immunglobulinproteinerne er mærket med et grønt fluorescerende mærke. Nanopartiklens last har spredt sig bredt gennem de fleste celler (grøn) uden at den er fanget i endosomer. Kredit:Yuan Rui, Johns Hopkins medicin
Forskere ved Johns Hopkins Medicine rapporterer, at de har skabt en lille, nanosize-beholder, der kan glide inde i celler og levere proteinbaserede lægemidler og genterapier af enhver størrelse-selv kraftige, der er knyttet til genredigeringsværktøjet kaldet CRISPR. Hvis deres oprettelse - konstrueret af en bionedbrydeligt polymer - består flere laboratorietests, det kunne tilbyde en måde til effektivt at færge større medicinske forbindelser til specifikt udvalgte målceller.
En rapport om deres arbejde vises i 6. december -udgaven af Videnskab fremskridt .
"De fleste lægemidler spredes i hele kroppen på en vilkårlig måde og er ikke målrettet mod en bestemt celle, "siger biomedicinsk ingeniør Jordan Green, Ph.d., leder af forskergruppen. "Nogle lægemidler, såsom antistoffer, låse fast på mål på cellens overfladereceptorer, men vi har ikke gode systemer til levering af biologiske lægemidler lige ind i en celle, det er her, terapier ville have den bedste chance for at fungere korrekt og med færre bivirkninger. "
Mange akademiske og kommercielle forskere har længe søgt bedre transitsystemer til terapier, siger Green, professor i biomedicinsk teknik, oftalmologi, onkologi, neurokirurgi, materialevidenskab og teknik, og kemisk og biomolekylær teknik ved Johns Hopkins University School of Medicine, og medlem af Bloomberg ~ Kimmel Institute for Cancer Immunotherapy hos Johns Hopkins.
Nogle kommercielt tilgængelige teknikker bruger afskalede former for vira - kendt for deres evne til at "inficere" celler direkte - til at levere terapier, selvom de ikke -infektiøse versioner af disse leveringssystemer kan frigøre et uønsket immunsystemrespons. Andre behandlinger rettet mod syge blodlegemer, for eksempel, er mere besværlige, kræver, at patienters blod fjernes derefter zappet med en elektrisk strøm, der åbner porerne i cellemembranen for at få adgang.
Den nanosize -beholder, som Green og hans team udviklede på Johns Hopkins, låner en idé fra virussens egenskaber, hvoraf mange er næsten kugleformede og bærer både negative og positive ladninger. Med en mere neutral samlet afgift, vira kan komme tæt på celler. Sådan er det ikke med mange biologiske lægemidler, som består af højt opladede, store proteiner og nukleinsyrer, der har en tendens til at afvise celler.
For at overvinde dette, kandidatstuderende Yuan Rui udviklede et nyt bionedbrydeligt polymermateriale. Polymer er den generelle betegnelse for et stof, der består af mange molekyler. For at lave polymeren, Rui spændte sammen - som grenene på et træ - fire komponentmolekyler, der, over tid, nedbrydes og opløses i vand. Molekylerne indeholder både positive og negative ladninger.
Med en balance mellem positive og negative ladninger, molekylerne skubber og trækker i henhold til deres ladning og deres hydrogenatomer binder sig til en biologisk terapi i nærheden. Resultatet er en nanostruktur, der indeholder den biologiske terapi.
Nanosize -beholderens positive ladninger interagerer med cellens membran, og beholderen opsluges i en cellulær pakning kaldet et endosom.
En gang indenfor, nanosize -beholderen åbner endosomet, og polymererne nedbrydes, lader medicinen virke inde i cellen.
For at teste deres opfindelse, Rui lavede en nanocontainer af et lille protein og fodrede det med musenyreceller i kulturretter. Hun fastgjorde et grønt fluorescerende mærke til det lille protein og så lysegrønne stænk i de fleste celler, hvilket indikerer, at proteinet blev leveret med succes.
Derefter, Rui pakket et større protein:humant immunglobulin, en terapi, der typisk bruges til at styrke immunsystemet og en model for antistofbehandlinger. Denne gang, hun fandt ud af, at 90% af nyrecellerne, hun behandlede, lyste op med det grønne fluorescerende mærke fastgjort til immunglobulinet.
"Når nanopartikler kommer ind i en celle, de bliver ofte udskilt til endosomer, som forringer dets indhold, men vores eksperimenter viser, at proteinpakkerne er ensartet spredt i de fleste celler og ikke sidder fast i endosomerne, "siger Rui.
For en endnu større udfordring, Rui skabte en nanopakke indeholdende et CRISPR-baseret protein- og nukleinsyrekompleks, der kunne slukke et grønt fluorescenssignal eller få cellerne til at lyse rødt, når CRISPR-forbindelsen skærer en del af en celles genom. Forskerne så, at genredigeringen for at deaktivere et gen fungerede i op til 77% af cellerne, der blev dyrket i laboratoriet, og for at tilføje eller reparere et gen i omkring 4% af cellerne.
"Det er ret effektivt i betragtning af med andre genredigeringssystemer, du får muligvis det korrekte genskæringsresultat mindre end 10 procent af tiden, "sagde Rui. CRISPR-baserede terapier har potentiale til at gøre lægemidler langt mere præcise med deres evne til præcist at målrette mod genetiske fejl, der bidrager til sygdom. Nogle CRISPR-behandlinger testes i kliniske forsøg.
I et sidste forsøg, Rui og hendes kolleger implanterede kræftceller i hjernen i musens hjerner. Hun injicerede nanokontainerne med genredigeringskomponenter direkte i musens hjerner og analyserede deres celler for en rød glød, der indikerer vellykket genredigering. Hun fandt kræftceller i hjernen, der glødede rødt flere millimeter væk fra, hvor hun injicerede dem.
'Da jeg startede dette projekt første gang for fem år siden, forskere troede ikke, at du kunne bruge noget andet end en virus til at levere disse terapier ind i celler, "siger Rui." Udvikling af nye teknologier kan hjælpe os med at forstå mere om sygdom, men også mere om at lave nye lægemidler. "
Rui og Green forsøger at gøre nanokontainerne mere stabile, så de kan injiceres i blodbanen og målrettes mod celler med visse genetiske signaturer.
Forskerne ansøger om patenter relateret til dette arbejde.
 Varme artikler
Varme artikler
-
 Argonne hjemmedyrket hybrid solcelle sigter efter lavpris strømDette computergenererede billede viser nanorør, 10, 000 gange mindre end bredden af et menneskehår, som omfatter en ny teknik udviklet hos Argonne til at dyrke solceller. Billede udlånt af Seth Darl
Argonne hjemmedyrket hybrid solcelle sigter efter lavpris strømDette computergenererede billede viser nanorør, 10, 000 gange mindre end bredden af et menneskehår, som omfatter en ny teknik udviklet hos Argonne til at dyrke solceller. Billede udlånt af Seth Darl -
 Selvbevidste materialer bygger fundamentet for levende strukturerEn illustration af det nye selvbevidste metamaterialesystem, som bruges i en kranspulsårstent. Designet kan mærke restenose, når det bruges i en stent, og samme design kan bruges i stor skala i brobjæ
Selvbevidste materialer bygger fundamentet for levende strukturerEn illustration af det nye selvbevidste metamaterialesystem, som bruges i en kranspulsårstent. Designet kan mærke restenose, når det bruges i en stent, og samme design kan bruges i stor skala i brobjæ -
 Nanocage-værktøj løsner (molekylær) spaghettiUniversity of Vermont post-doc forsker Mona Sharafi hjalp med at bygge et værktøj i nanoskala, der kan løse knuder af protein, plast eller andre polymerer. Kaldes en nanocage, fremskridtet inden for k
Nanocage-værktøj løsner (molekylær) spaghettiUniversity of Vermont post-doc forsker Mona Sharafi hjalp med at bygge et værktøj i nanoskala, der kan løse knuder af protein, plast eller andre polymerer. Kaldes en nanocage, fremskridtet inden for k -
 Ny model letter forudsigelser om, hvordan nanopartikler dannes, giver fingerpeg om, hvordan processe…Følg altid kompasset:Mikroorganismer, der orienterer sig efter Jordens magnetfelt, har omkring 20 magnetosomer, som stiller sig op til små nåle. De indeholder magnetiske nanopartikler af jernoxid i en
Ny model letter forudsigelser om, hvordan nanopartikler dannes, giver fingerpeg om, hvordan processe…Følg altid kompasset:Mikroorganismer, der orienterer sig efter Jordens magnetfelt, har omkring 20 magnetosomer, som stiller sig op til små nåle. De indeholder magnetiske nanopartikler af jernoxid i en
- Egenskaber af hydrater til kemieksperimenter
- Forskere designer teknologi, der ser nerveceller brande
- I kolliderende galakser, en pipsqueak skinner klart
- Bevis for Higgs -partiklerne henfalder i kvarker
- Arkæologiske opdagelser sker hurtigere end nogensinde før, hjælpe med at forfine den menneskelige…
- Ring, Amazon sagsøgt af en mand, der siger, at hacker generede sine børn


