Iron nanorobots viser deres sande slag
Ved at kombinere laveffektmagnetiske felter, som omrører nanotråde, med laseropvarmning og medicinlevering, målceller kan dræbes effektivt. Kredit:KAUST
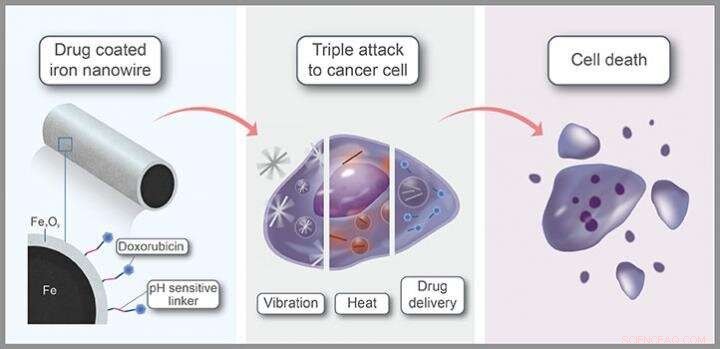
Narkotika belagt med jern-nanotråde, der kan ledes til stedet for en tumor ved hjælp af et eksternt magnetfelt, før en tre-trins kræftdræbende mekanisme aktiveres, kan give en effektiv mulighed for kræftbehandling.
Medudviklet af KAUST-forskere, disse nanotråde frigiver deres lægemiddelfragt inde i kræftceller, samtidig med at der stikkes huller i cellens membran og leverer et brag af varme. Mens kombinationsterapien maksimerer kræftcelledød, dens meget målrettede karakter bør minimere bivirkninger.
Jern var det oplagte materiale til fremstilling af nanotråde, siger Jürgen Kosel, der leder gruppen på KAUST, som omfatter Jasmeen Merzaban og Boon Ooi, og som ledede arbejdet sammen med forskere fra CIC biomaGUNE i San Sebastian, Spanien.
Den første overvejelse er sikkerhed. "Jern, i molekylær form, er et naturligt materiale i vores kroppe, afgørende for ilttransport, "Forklarer Kosel. Nanotråde består af en jernkerne, belagt med en jernoxidskal. "Jernoxidbaserede nanomaterialer er godkendt af tilsynsmyndigheder til brug ved magnetisk resonansbilleddannelse og som kosttilskud i tilfælde af ernæringsmangel " han siger.
Ud over deres biokompatibilitet, de magnetiske egenskaber ved jernbaserede materialer er en vigtig fordel. "Brug af harmløse magnetfelter, vi kan transportere dem; koncentrer dem i det ønskede område; rotere eller få dem til at vibrere, sådan som vi gjorde i denne undersøgelse; og endda opdage dem ved hjælp af magnetisk resonansbilleddannelse, "siger Aldo Martínez-Banderas, medlem af Kosels team. Anvendelse af laveffektmagnetfelter, holdet agiterede nanotråde på en måde, der åbnede membranen af målceller, fremkalder celledød.
Den ekstra fordel er, at nanotråde med kerneskal stærkt absorberer nær-infrarødt lys, opvarmning, mens de gør det. Fordi lys ved denne bølgelængde kan trænge langt ind i kroppen, nanotråde kunne opvarmes ved hjælp af lasere rettet mod tumorstedet. "Core-shell nanotråde viste en ekstremt høj fototermisk konverteringseffektivitet på mere end 80 procent, som omsatte til en stor intracellulær varmedosis, ”Siger Martínez-Banderas.
Endelig, anticancer-lægemidlet doxorubicin blev knyttet til nanotråde via pH-følsomme linkere. Da tumormiljøet typisk er mere surt end sundt væv, linkeren nedbrydes selektivt i eller i nærheden af tumorceller, frigive stoffet, hvor det er nødvendigt. "Kombinationen af behandling resulterede i næsten fuldstændig kræftcelleablation og var mere effektiv end individuelle behandlinger eller medicin mod kræft alene, ”Siger Martínez-Banderas.
"Taget sammen, mulighederne for jernbaserede nanomaterialer gør dem meget lovende for oprettelsen af biomedicinske nanorobotter, som kan revolutionere sundhedsvæsenet, "Tilføjer Kosel." Selvom dette kan virke futuristisk, udviklingen er godt på vej. "
 Varme artikler
Varme artikler
-
 Indfangning af nanopartikler med optisk pincetIndfangning af fluorescerende partikler med Arago-pletter. Kredit: European Physical Journal E Ved at udnytte en bestemt egenskab ved lysdiffraktion ved grænsefladen mellem et glas og en væske, f
Indfangning af nanopartikler med optisk pincetIndfangning af fluorescerende partikler med Arago-pletter. Kredit: European Physical Journal E Ved at udnytte en bestemt egenskab ved lysdiffraktion ved grænsefladen mellem et glas og en væske, f -
 Forskere udvikler nanococktail mod kræftDoxorubicin-ladede liposomer er designet til at dræbe tumorer. (PhysOrg.com)-Et team af forskere i Californien og Massachusetts har udviklet en cocktail af forskellige partikler i nanometerstørrel
Forskere udvikler nanococktail mod kræftDoxorubicin-ladede liposomer er designet til at dræbe tumorer. (PhysOrg.com)-Et team af forskere i Californien og Massachusetts har udviklet en cocktail af forskellige partikler i nanometerstørrel -
 Jagten på effektivitet i termoelektriske nanotrådeGraham Yelton og Sandia National Laboratories kolleger har udviklet en enkelt elektroformningsteknik, der skræddersyede nøglefaktorer til bedre termoelektrisk ydeevne:krystalorientering, krystalstørre
Jagten på effektivitet i termoelektriske nanotrådeGraham Yelton og Sandia National Laboratories kolleger har udviklet en enkelt elektroformningsteknik, der skræddersyede nøglefaktorer til bedre termoelektrisk ydeevne:krystalorientering, krystalstørre -
 Hall-fejls afsløringer rejser forhåbninger om 2-D materialerScanning af elektronmikroskopbillede af en 2D Hall-enhed med fire par elektroder for at teste fire forskellige geometrier med en 2D InAs-prøve. Kredit:Adam Micolich En af de første ting, folk gør,
Hall-fejls afsløringer rejser forhåbninger om 2-D materialerScanning af elektronmikroskopbillede af en 2D Hall-enhed med fire par elektroder for at teste fire forskellige geometrier med en 2D InAs-prøve. Kredit:Adam Micolich En af de første ting, folk gør,
- De bedste spioner i himlen analyserer Mellaria
- Forskelle mellem et surt rengøringsmiddel Fiber og et neutralt rengøringsmiddel Fiber
- Kobberbelægning på 3-D-printede plastikfiltre foreslået som en pandemibekæmper
- Nyt batteridesign kan oplade en elbil på 10 minutter
- Multiplicering af lys kan være nøglen til ultrakraftfulde optiske computere
- Ny strategi til at designe mekano-responsive selvlysende materialer


