Selektiv aflivning af kræftceller ved at ødelægge deres affaldsbortskaffelsessystem
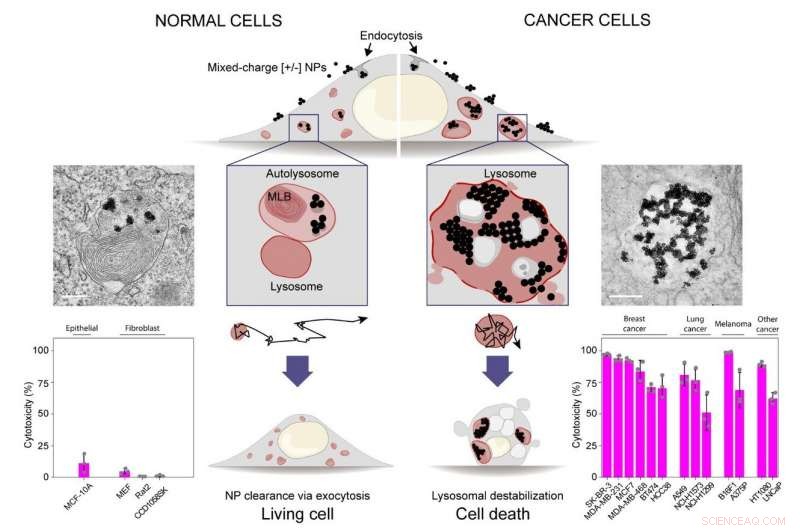
Blandede nanopartikler til destabilisering af kræftlysosomer og selektiv aflivning af kræftceller. Histogrammer i nederste række viser, at nanopartikler med blandet ladning selektivt dræber tretten kræftcellelinjer (histogram til højre), uden at skade fire normale epitel- eller fibroblast celletyper/linjer (histogram til venstre). Kredit:IBS
Et team af forskere fra Center for Soft and Living Matter, inden for Institute of Basic Science (IBS, Sydkorea) og tilknyttet Ulsan National Institute of Science and Technology (UNIST) har opdaget en ny tilgang til selektivt at målrette og dræbe flere typer kræftceller.
Lysosomer er små sække fyldt med et stort antal enzymer og syre, der arbejder for at nedbryde og genbruge beskadigede og uønskede cellulære komponenter. Med andre ord, de er samtidigt både en celles affaldsbeholder og genbrugscentral. Typisk, lysosomer slippe af med biprodukterne ved denne nedbrydningsproces ved at frigive dem uden for cellen. At slippe affaldet ud udenfor giver kun mening. For eksempel, forestil dig at samle alt affaldet i dit hus i en skraldespand og derefter tømme den samme skraldespand lige på gulvet i køkkenet, gør dine levevilkår elendige. Tilsvarende punktering af lysosomer og frigivelse af deres giftige indhold inde i cellen beskadiger cellulære komponenter uden reparation, hvilket, i ekstreme tilfælde, kan udløse celledød.
Da kræftlysosomer er lettere at beskadige end raske cellers lysosomer, forskere har undersøgt at bruge denne strategi som et lovende alternativ til at målrette kræft, der er resistente over for konventionelle behandlinger. Imidlertid, kun en håndfuld potentielle terapeutika kan målrette lysosomer, og de fleste af dem mangler kræftselektivitet.
Udgivet i Naturnanoteknologi , denne undersøgelse viser, at nanopartikler dækket med en blanding af positivt [+] og negativt [-] ladede molekyler selektivt kan dræbe kræftceller ved at målrette deres lysosomer. Døden af kræftceller skyldes en bemærkelsesværdig række af transport- og aggregeringsfænomener, startende med dannelsen af små klynger af nanopartikler ved celleoverflader og kulminerede med samlingen af nanopartikelkrystaller i mikronstørrelse inde i kræftlysosomerne. Nanopartikelkrystaller fremkalder lysosomal hævelse, gradvist tab af lysosomale membraners integritet, og endelig celledød.
"I dette arbejde, vi har udnyttet kræftcellernes deregulerede affaldshåndteringssystem til at fungere som en "nanoskala samlebånd" til konstruktion af nanopartikelkrystaller af høj kvalitet, der ødelægger de meget lysosome "reaktorer", der tillod dem at vokse i første omgang, "siger Bartosz A. Grzybowski, medførende forfatter til undersøgelsen.
Aggregeringen af blandede nanopartikler foretrækkes af det sure miljø, der er typisk for kræftceller. "Ikke-kræftceller, imidlertid, også internalisere blandede ladning nanopartikler, men aggregering af nanopartikler er begrænset. Nanopartiklerne passerer hurtigt gennem genbrugsruter og ryddes fra disse celler, "forklarer Kristiana Kandere-Grzybowska, medførende forfatter til undersøgelsen.
"Vores konklusioner er baseret på en sammenligning af tretten forskellige sarkomer, melanom, bryst- og lungecarcinomcellelinier med fire ikke-kræftcelletyper, "tilføjer den første forfatter til undersøgelsen, Magdalena Borkowska. "Nanopartiklerne var effektive mod alle tretten kræftlinjer, samtidig med at de ikke skader ikke-kræftceller. "
Aggregeringen af nanopartiklerne, når de passerer gennem det endolysosomale system af kræftceller, er en kompleks proces. Teamet opdagede, at nanopartikler med en overfladesammensætning på ca. 80% [+] og 20% [-] ligander viser optimal kræftselektivitet. Det faktum, at negativt ladede ligander også er pH-følsomme, synes at være nøglen til kræftselektivitet. I den sure pH, findes omkring kræftceller og inde i lysosomerne, disse ligander er protonerede og tilbøjelige til at interagere med lignende ligander på de tilstødende nanopartikler, dermed fremme deres aggregering. Balancen mellem attraktive interaktioner-bindingerne mellem [-] ligander og stærke interaktioner mellem nanopartikelkerner-og elektrostatiske afstødninger mellem [+] ligander på nabopartiklerne bestemmer omfanget af nanopartikelaggregation. Samlet set, interaktionen mellem partikler, serumproteiner og cellers indre miljø arbejder sammen om at forringe kræftlysosomer.
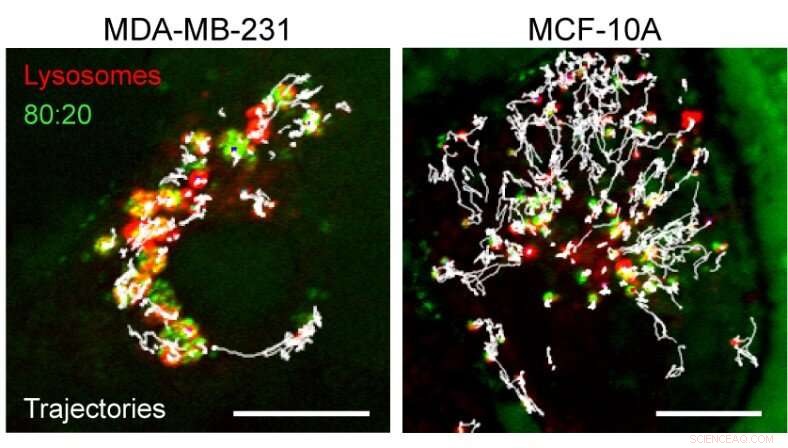
Effekten af nanopartikelaggregering inde i lysosomer. Billedet viser banerne (hvide) for lysosomer (rød) i kræft (til venstre) kontra normale (til højre) celler. Nanopartikelaggregater (grønne) i kræftceller nedsatte lysosomers evne til at undersøge cellens indre. Skala bar, 10? M. Kredit:IBS
"Nanopartikelklyngerne kan ændre liposammensætningen i lysosommembranen, påvirke dens integritet og gøre den mindre mekanisk robust. Uventet, vores team opdagede også, at nogle proteiner, såsom cellevækst -signalmolekylerne mTORC1, er forskudt (og dermed hæmmet) fra overfladen af nanopartikelholdige kræftlysosomer. Dette er vigtigt, fordi kræftcellevækst og -deling kræver mTORC1, og nanopartikler lukker det kun ned i kræftceller, "forklarer Kandere-Grzybowska.
Mens enkelte nanopartikler er omtrent samme størrelse som et gennemsnitligt proteinmolekyle, og dermed for lille til at blive set med de fleste dynamiske levende cellemikroskopimetoder, krystallerne sammensat af flere nanopartikler kan observeres. Teamet brugte en kombination af komplementære tilgange, herunder mørkfeltmikroskopi, konfokal refleksionsmikroskopi, og TEM, samt biokemiske og beregningsmæssige tilgange til at vurdere den fulde effekt af blandede ladning nanopartikler på lysosomale organeller.
Denne undersøgelse åbner for nye forskningsretninger. Strategien for blandet ladning kan anvendes på andre typer nanopartikler, såsom polymerbaserede partikler, dendrimerer eller jernoxid -nanopartikler. Et andet vigtigt skridt vil være at teste effektiviteten af blandede nanopartikler mod tumorer i dyremodeller.
 Varme artikler
Varme artikler
-
 IBM-forskere laver verdens mindste film ved hjælp af atomer (med video)Filmplakat A Boy and His Atom. Kredit:IBM (Phys.org) – Forskere fra IBM afslørede i dag verdens mindste film, lavet med et af de mindste grundstoffer i universet:atomer. Navnet En dreng og hans at
IBM-forskere laver verdens mindste film ved hjælp af atomer (med video)Filmplakat A Boy and His Atom. Kredit:IBM (Phys.org) – Forskere fra IBM afslørede i dag verdens mindste film, lavet med et af de mindste grundstoffer i universet:atomer. Navnet En dreng og hans at -
 Beholder i nanostørrelse med fotoswitche frigiver last ved bestrålingSkematisk fremstilling af gæsteoptagelse via formaling og frigivelse af gæsten ved bestråling i vand. Beholderen kan regenereres ved lysbestråling eller opvarmning. Kredit:Tokyo Tech Forskere ved
Beholder i nanostørrelse med fotoswitche frigiver last ved bestrålingSkematisk fremstilling af gæsteoptagelse via formaling og frigivelse af gæsten ved bestråling i vand. Beholderen kan regenereres ved lysbestråling eller opvarmning. Kredit:Tokyo Tech Forskere ved -
 Ultratyndt halvledende ark, der viser gasfølsomme elektroniske egenskaber til meget følsomme gasse…Atomistisk model, der viser ladningsakkumulering (gul) og udtømning (rød) ved NO-adsorption på PtSe2-monolag. Platinatomer vises i gråt, og selenatomer vises med grønt. Kreditering:Gengivet med tillad
Ultratyndt halvledende ark, der viser gasfølsomme elektroniske egenskaber til meget følsomme gasse…Atomistisk model, der viser ladningsakkumulering (gul) og udtømning (rød) ved NO-adsorption på PtSe2-monolag. Platinatomer vises i gråt, og selenatomer vises med grønt. Kreditering:Gengivet med tillad -
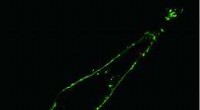 Et enkeltcellet endoskop:Forskere bruger nanofotonik til optisk kig inde i levende cellerFluorescens konfokalt billede af en enkelt levende HeLa-celle viser, at der via nanoendoskopi er blevet leveret en kvantepunktklynge (rød prik) til cytoplasmaet i cellens membran (grøn). Udlånt af Ber
Et enkeltcellet endoskop:Forskere bruger nanofotonik til optisk kig inde i levende cellerFluorescens konfokalt billede af en enkelt levende HeLa-celle viser, at der via nanoendoskopi er blevet leveret en kvantepunktklynge (rød prik) til cytoplasmaet i cellens membran (grøn). Udlånt af Ber
- Van der Waals krydsspindventiler uden afstandsstykke
- Knækker koden til soddannelse - forskere låser op for mysterium for at hjælpe med at reducere far…
- Serendipity udvider mulighederne for fremstilling af grafit
- Mikrobiel produktion af et naturligt rødt farvestof karminsyre
- Forskning tester, hvilket nanosystem der fungerer bedst til kræftbehandling
- SpaceX lancerer 59 satellitter i rummet som en del af StarLink -projektet


