Designer nanozymer til reaktive iltarter, der fjerner antiinflammatorisk terapi
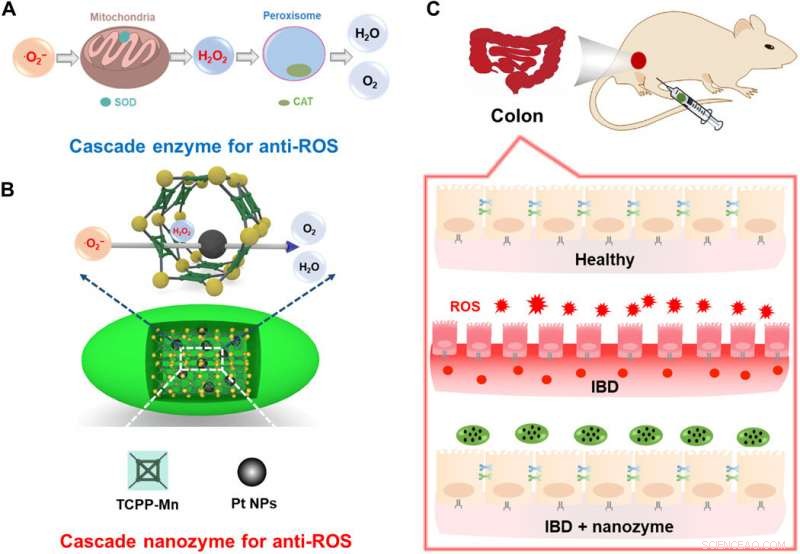
Skematisk illustration af designet af et integreret nanozym med kaskade anti-ROS-aktivitet til IBD-terapi. (A) Cellulære kaskadeenzymer til anti-ROS. Den terapeutiske effektivitet af et sådant system er begrænset på grund af de forskellige subcellulære placeringer af SOD- og CAT-enzymer og begrænset ekstracellulær stabilitet. (B) Konstruktion af et kaskade-nanozym til anti-ROS-terapi ved at indlejre Pt NP'er i PCN222-Mn MOF. Nanoskala nærhed af katalytiske aktive steder fremmer kaskadereaktionerne. (C) IBD af mus kan effektivt lindres gennem behandling med det integrerede kaskade-nanozym. Kredit:Science Advances, doi:10.1126/sciadv.abb2695
I en nylig rapport, Yufeng Liu og et team af tværfaglige forskere i Kina udviklede en integreret nanozym-kaskade til at eliminere overskydende reaktive oxygenarter (ROS; oxygen-frie radikaler). Nanozymet efterlignede superoxiddismutase (en gruppe enzymer) og inkorporerede en mangan (Mn)-baseret metal-organisk ramme (MOF) for at omdanne iltradikaler til hydrogenperoxid (H) 2 O 2 ). Ved at bruge in-lab og in vivo eksperimenter, holdet viste ROS-opfangende potentiale af integrerede kaskade nanozymer. Som proof of concept, de lindrede to former for inflammatorisk tarmsygdom (IBD) - colitis ulcerosa og Crohns sygdom ved at bruge kaskade nanozymer som effektive behandlinger. Undersøgelsen gav en ny metode til at konstruere enzymlignende kaskadesystemer og illustrere løftet om deres effektive terapi til behandling af IBD in vivo. Værket er nu udgivet på Videnskabens fremskridt .
Under kaskadekatalytiske reaktioner, der forekommer i levende organismer, flere enzymer er kombineret inde i subcellulære rum for nøjagtig signaltransduktion og effektiv metabolisme. Sådanne begrænsede kaskadereaktioner er fordelagtige sammenlignet med konventionelle flertrinsreaktioner på grund af reducerede diffusionsbarrierer og forbedrede lokale koncentrationer af mellemprodukter for forbedret atomøkonomi og reaktioner i alt. Forskere har gjort en betydelig indsats for at efterligne sådanne kaskadesystemer på stilladser, men deres høje omkostninger og lave stabilitet har begrænsede brede praktiske anvendelser. Som resultat, forskere har udforsket enzymefterligninger for at forstå og konstruere kaskadereaktioner i laboratoriet. I dette arbejde, Liu et al. detaljerede et enkeltkomponent nanozym-baseret kaskadereaktionssystem med høj aktivitet og demonstrerede deres rolle under in vivo-terapien af reaktive oxygenarter (ROS)-associeret inflammatorisk tarmsygdom (IBD).
Design, syntese og karakterisering af enzymstilladset
Holdet designede og syntetiserede et integreret superoxiddismutase (SOD) og katalase (CAT) mimetisk kaskade nanozym og betegnede det som Pt@PCN222-Mn. For at konstruere stilladset, de introducerede en SOD-lignende del af mangan (Mn) (III) porphyrin og en CAT-lignende platinnanopartikel i en nanoskala zirconium (Zr)-baseret metalorganisk ramme (MOF) ved navn PCN222. Den integrerede konstruktion (Pt@PCN222-Mn) viste forbedret ROS-opfangende aktivitet for at beskytte mus mod ROS-relateret IBD, en uhelbredelig kronisk sygdom endnu, og derved at udvide potentialet af kaskade nanozymer til in vivo biomedicinske anvendelser.
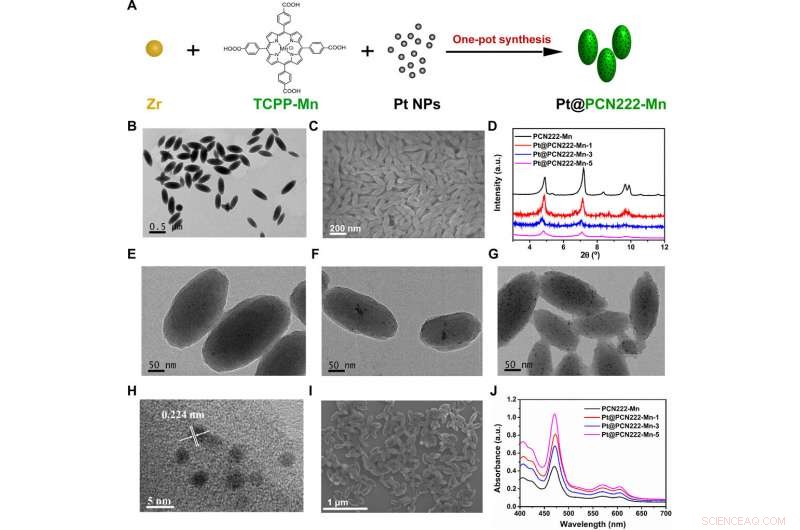
Syntese og strukturel karakterisering af Pt@PCN222-Mn og relaterede materialer. (A) Synteseprocedure af Pt@PCN222-Mn. (B) Transmissionselektronmikroskopiske (TEM) og (C) Scanningelektronmikroskopiske (SEM) billeder af PCN222-Mn. (D) Pulver røntgendiffraktion (PXRD) mønstre af PCN222-Mn, Pt@PCN222-Mn-1, Pt@PCN222-Mn-3, og Pt@PCN222-Mn-5. TEM-billeder af (E) Pt@PCN222-Mn-1, (F) Pt@PCN222-Mn-3, og (G) Pt@PCN222-Mn-5. (H) Højopløselige TEM- og (I) SEM-billeder af Pt@PCN222-Mn-5. (J) Absorptionsspektre af PCN222-Mn, Pt@PCN222-Mn-1, Pt@PCN222-Mn-3, og Pt@PCN222-Mn-5. a.u., vilkårlige enheder. Kredit:Science Advances, doi:10.1126/sciadv.abb2695
Under forsøgene, Liu et al. bekræftede den vellykkede syntese af de foreløbige manganbaserede konstruktioner ved hjælp af nuklear magnetisk resonans, Fourier transform infrarød spektroskopi og ultraviolet synlige spektroskopiske målinger. Holdet syntetiserede komponenten indeholdende en MOF i nanoskala og bekræftede dens dannelse med transmissionselektronmikroskopi (TEM) og scanningselektronmikroskopi (SEM). Forskerne udviklede derefter tre kaskade nanozymer og kaldte dem Pt@PCN222-Mn-1, Pt@PCN222-Mn-3 og Pt@PCN222-Mn-5, henholdsvis. Af disse, Pt@PCN222-Mn-5 havde et højere overfladeareal sammenlignet med andre anti-ROS nanozymer, der er undersøgt hidtil.
Undersøgelse af den katalytiske aktivitet af kaskadenanozymer
Opfangning af iltradikaler ( • O 2 − ) er det indledende trin i anti-ROS-kaskadereaktionen, Derfor undersøgte holdet den katalytiske aktivitet af de syntetiske konstruktioner for at overvåge deres evne til på lignende måde at eliminere oxygenradikaler. Arbejdet fremhævede mangans nøglerolle i porphyrin til at efterligne superoxiddismutase (SOD)-lignende aktiviteter af de forskellige enzymkonstruktioner, hvor Pt@PCN222-Mn-5-konstruktioner udviste den højeste SOD-lignende aktivitet blandt enzymmimikerne. Holdet bekræftede resultaterne ved hjælp af elektron paramagnetisk resonans (EPR) spektroskopi.
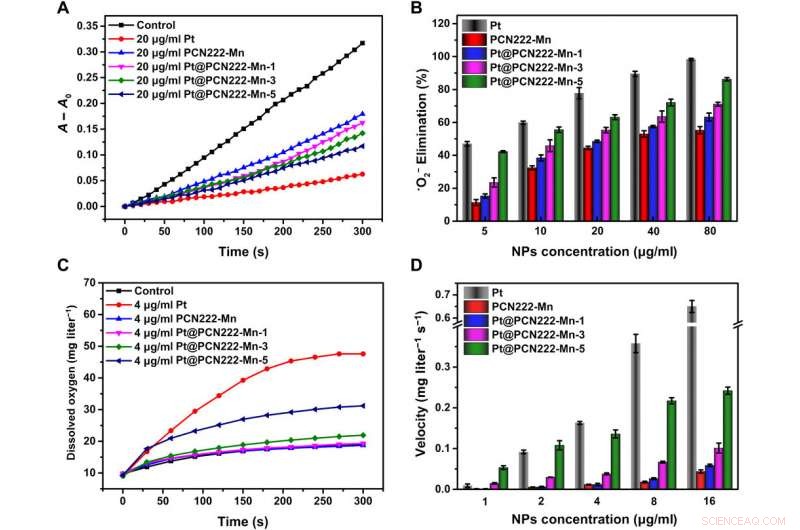
ROS-rensende aktiviteter af Pt@PCN222-Mn og relaterede materialer. (A) Typiske kinetiske kurver for A - A0 (550 nm) til overvågning af reduktionen af NBT med X og XO i fravær og tilstedeværelse af Pt, PCN222-Mn, Pt@PCN222-Mn-1, Pt@PCN222-Mn-3, og Pt@PCN222-Mn-5. (B) Afhængighed mellem eliminationseffektiviteten af •O2− og koncentrationer af nanozymer. (C) Typiske kinetiske kurver for iltdannelse fra nedbrydning af H2O2 (50 mM) i nærvær af Pt, PCN222-Mn, Pt@PCN222-Mn-1, Pt@PCN222-Mn-3, og Pt@PCN222-Mn-5. (D) Afhængighed mellem iltproduktionshastighederne i de første 60 s og koncentrationer af nanozymer. Dataene er vist som middel ± SD (n =3). Kredit:Science Advances, doi:10.1126/sciadv.abb2695
Som et andet afgørende skridt i den ROS-opfangende kaskade i biologiske miljøer, CAT (catalase) enzymet katalyserede nedbrydningen af hydrogenperoxid (H 2 O 2 ) til vand og oxygen. Liu et al. overvågede derfor de CAT-lignende aktiviteter af nanozymer ved at overvåge oxygen genereret fra nedbrydning af hydrogenperoxid. Som før, Pt@PCN222-Mn-5 viste den højeste CAT-lignende aktivitet blandt MOF-baserede enzymefterligninger. Baseret på resultaterne, Liu et al. bekræftede den SOD-lignende aktivitet som følge af den manganbundne del af enzymkonstruktionen, mens integrerede platinnanopartikler hovedsageligt var ansvarlige for den CAT-lignende aktivitet.
Fokus enzym Pt@PCN222-Mn-5 og in vivo antiinflammatorisk behandling
For fuldt ud at forstå aktiviteten af kaskadenanozymet Pt@PCN222-Mn-5, holdet undersøgte dets synergistiske SOD-lignende og CAT-lignende enzymaktivitet og observerede udtalte synergistiske effekter for sidstnævnte. Holdet valgte nanozymet til yderligere undersøgelser og testede dets funktionalitet med en cellelinje under cytotoksicitetsundersøgelser. Ved en koncentration under 80 µg/ml, nanozymet udviste ingen cytotoksicitet og udviste fremragende reaktive oxygenarter scanning potentiale.
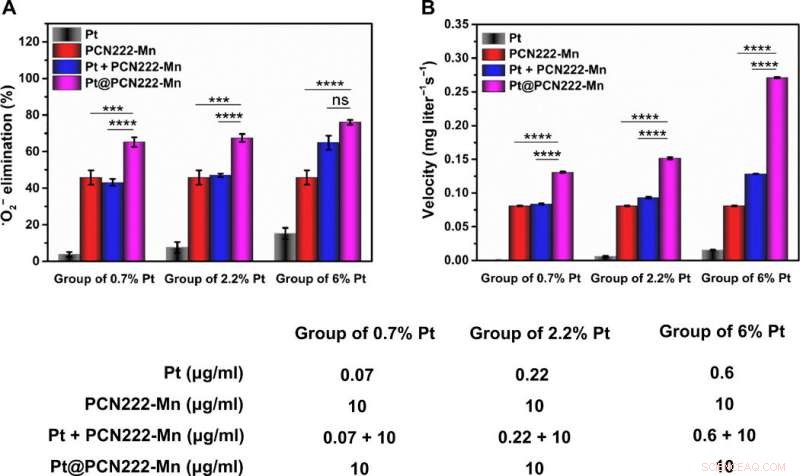
Synergistisk ROS-fjernende aktivitet af Pt@PCN222-Mn-5. (A) Elimineringseffektivitet af •O2− med forskellige koncentrationer af Pt, PCN222-Mn, Pt + PCN222-Mn, og Pt@PCN222-Mn. (B) Iltproduktionshastigheder i de første 60 s, med forskellige koncentrationer af Pt, PCN222-Mn, Pt + PCN222-Mn, og Pt@PCN222-Mn. Dataene er vist som middel ± SD (n =3). ***P <0,005 og ****P <0,001; ns, ikke signifikant; t test. Kredit:Science Advances, doi:10.1126/sciadv.abb2695
Baseret på forsøgsresultaterne, Liu et al. udført in vivo-terapier til behandling af colitis ulcerosa (UC) og Crohns sygdom (CD) i musemodeller af sygdommen. Da UC er en form for inflammatorisk tarmsygdom, der typisk er ledsaget af overproducerede reaktive oxygenarter, forskerne testede de terapeutiske virkninger af Pt@PCN222-Mn-5 sammen med eksisterende medicin til IBD-behandling. Holdet administrerede behandlingen via intraperitoneal injektion til hver mus og observerede vellykkede terapeutiske virkninger af Pt@PCN222-Mn-5 for at lindre UC-sygdomstilstanden hos mus. Holdet optimerede doserne af kaskadenanozymet ved hjælp af flere behandlingsgrupper og fandt, at fokusenzymet af interesse var det mest gunstige. Da de på samme måde udforskede cd'er, en anden type IBD ved hjælp af en sygdomsinduceret musemodel, behandlingsstrategien indikerede større effektivitet for kaskadenanozymer sammenlignet med traditionelle småmolekylære lægemidler, der anvendes i IBD-behandling.
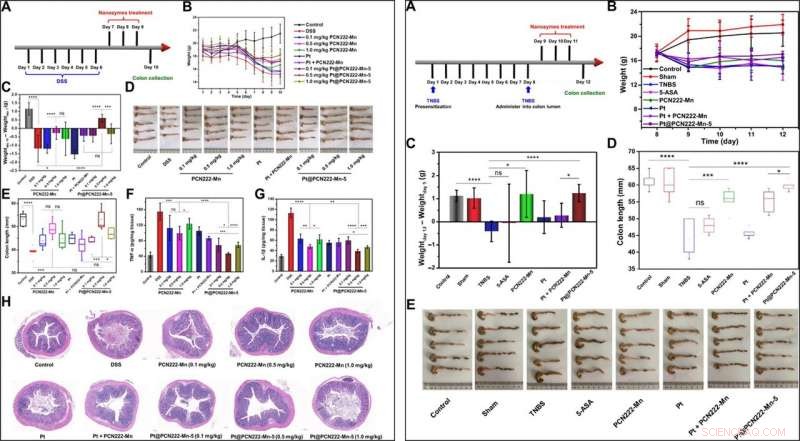
TIL VENSTRE:UC-terapi med Pt@PCN222-Mn-5. (A) Overordnet procedure for dyreforsøget (DSS-induceret colitis). (B) Daglig kropsvægtudvikling i 10 dage. (C) Ændringer i kropsvægt hos mus før (dag 7) og efter indikerede behandlinger (dag 10). (D) Billeder af tyktarmen og (E) de tilsvarende tyktarmslængder i angivne grupper. (F) IL-1β og (G) TNF-a-niveauer i colonhomogenater fra angivne grupper. (H) H&E-farvede tyktarmssnit af mus fra angivne grupper på dag 10. Dataene er vist som middelværdier ± SD (n =5). *P <0,05, **P <0,01, ***P <0,005, og ****P <0,001; ns, ikke signifikant; t test. Billedkredit (D):Yufeng Liu, College of Engineering and Applied Sciences, Nanjing Universitet. TIL HØJRE:CD-terapi med Pt@PCN222-Mn-5. (A) Overordnet procedure for dyreforsøget [2, 4, 6-trinitrobenzensulfonsyre (TNBS)-induceret colitis]. (B) Daglig kropsvægtudvikling efter administration af TNBS-opløsning i tyktarmens lumen. (C) Ændringer i kropsvægt hos mus før (dag 9) og efter indikerede behandlinger (dag 12). (D) Kolonlængder og (E) de tilsvarende billeder af koloner i angivne grupper. Dataene er vist som middel ± SD (n =5). *P <0,05, ***P <0,005, og ****P <0,001; ns, ikke signifikant; t test. Billedkredit (E):Yuan Cheng, College of Engineering and Applied Sciences, Nanjing Universitet. Kredit:Science Advances, doi:10.1126/sciadv.abb2695
På denne måde Yufeng Liu og kolleger udviklede et integreret nanozym til at katalysere kaskadereaktioner og eliminere reaktive oxygenarter (ROS). Det integrerede nanozym havde to rumligt adskilte aktive steder til at efterligne superoxiddismutase (SOD) og katalase (CAT). Ved hjælp af laboratorieeksperimenter viste de den fremragende ROS-fjernende aktivitet af kaskadenanozymet, deres fremragende biokompatibilitet og gode vandige dispergerbarhed. Holdet etablerede en inflammatorisk dyremodel for at teste kaskadenanozymets anti-ROS-kapacitet i en biologisk organisme og bestemte deres overlegne terapeutiske potentiale over for både ulcerøs colitis (UC) og Crohns sygdom (CD) modeller for inflammatorisk tarmsygdom (IBD). Holdet optimerede koncentrationen af nanozymet for at opnå effektiv lindring af IBD i dyremodeller. Arbejdet viste fremragende ROS-fjernende aktiviteter til inflammatorisk behandling og giver en lovende metode til at konstruere nanozymer med flere aktive steder til yderligere anvendelse i biomedicin.
© 2020 Science X Network
 Varme artikler
Varme artikler
-
 Nanotech forbedrer cystisk fibrose-antibiotikum med 100, 000 gangeKredit:Shutterstock Verdens første nanoteknologi udviklet af University of South Australia kan ændre livet for tusindvis af mennesker, der lever med cystisk fibrose (CF), som viser, at det kan for
Nanotech forbedrer cystisk fibrose-antibiotikum med 100, 000 gangeKredit:Shutterstock Verdens første nanoteknologi udviklet af University of South Australia kan ændre livet for tusindvis af mennesker, der lever med cystisk fibrose (CF), som viser, at det kan for -
 Små partikelfri sølvblæktryk, højtydende elektronikReaktivt sølvblæk airbrushes på en tynd, elastisk plastikfilm til at lave en fleksibel sølvelektrode. Kredit:S. Brett Walker Materialeforskere fra University of Illinois har udviklet en ny reaktiv
Små partikelfri sølvblæktryk, højtydende elektronikReaktivt sølvblæk airbrushes på en tynd, elastisk plastikfilm til at lave en fleksibel sølvelektrode. Kredit:S. Brett Walker Materialeforskere fra University of Illinois har udviklet en ny reaktiv -
 Hvad hvis nanoverdenen glider:En ny undersøgelse for bedre at forstå, hvordan friktion virkerHvad hvis nanoverdenen glider? Kredit:SISSA En undersøgelse offentliggjort af Andrea Vanossi, Nicola Manini og Erio Tosatti - tre SISSA-forskere - i PNAS ( Procedurer fra National Academy of Sc
Hvad hvis nanoverdenen glider:En ny undersøgelse for bedre at forstå, hvordan friktion virkerHvad hvis nanoverdenen glider? Kredit:SISSA En undersøgelse offentliggjort af Andrea Vanossi, Nicola Manini og Erio Tosatti - tre SISSA-forskere - i PNAS ( Procedurer fra National Academy of Sc -
 Forskere udskriver nanoskala billeddannelsessonde på spidsen af optisk fiberEn ny proces kaldet fiber nanoimprinting accelererer fremstillingen af nano-optiske enheder, såsom denne pyramideformede Campanile-sonde præget på en optisk fiber (fanget i et scanning-elektronmikro
Forskere udskriver nanoskala billeddannelsessonde på spidsen af optisk fiberEn ny proces kaldet fiber nanoimprinting accelererer fremstillingen af nano-optiske enheder, såsom denne pyramideformede Campanile-sonde præget på en optisk fiber (fanget i et scanning-elektronmikro
- Brug af mobiltelefoner til at opdage skadelige luftbårne stoffer
- Amerikansk lastrumfartøj indstillet til afgang fra den internationale rumstation
- Dødelige hedebølger vil være almindelige i Sydasien, selv ved 1,5 graders opvarmning
- Ny undersøgelse præsenterer effektive, løsning-behandlet, hybrid tandem solceller
- NASA finder Tropical Depression Dahlias center blottet for nedbør
- Forskere når en milepæl i brugen af nanopartikler til at dræbe kræft med varme


