Kræftlægemidler kunne leveres i molekylære bure låst op af lys
Kredit:Imperial College London
Molekylære bure skabt af imperiale forskere kan føre til mere målrettet kræfttilførsel af lægemidler, medfører større effektivitet og færre bivirkninger.
Mange stoffer, herunder kræftbehandlinger, kan nedbrydes i kroppen, hvilket reducerer deres effektivitet og kan betyde, at der er behov for flere doser. De kan også forårsage bivirkninger, når de beskadiger sundt væv.
Forskere søger derfor efter måder at gøre stoffer mere målrettede, så de begynder først at virke, når de når den højre del af kroppen, såsom stedet for en kræfttumor.
Nu, forskere fra Institut for Kemi ved Imperial College London har skabt en ny type 'bur' til et molekyle med anticancer-egenskaber. Frigivelsen af molekylet fra buret kan derefter kontrolleres af eksterne stimuli, såsom lys. Undersøgelsen er offentliggjort i dag i Angewandte Chemie .
Ph.D. studerende Timothy Kench sagde:"Vi er virkelig begejstrede for tilgangen. Ved at regulere den biologiske aktivitet af små molekyler, vi kan designe forbedrede terapier eller studere specifikke cellulære processer."
Indfangning af lægemiddelmolekyler
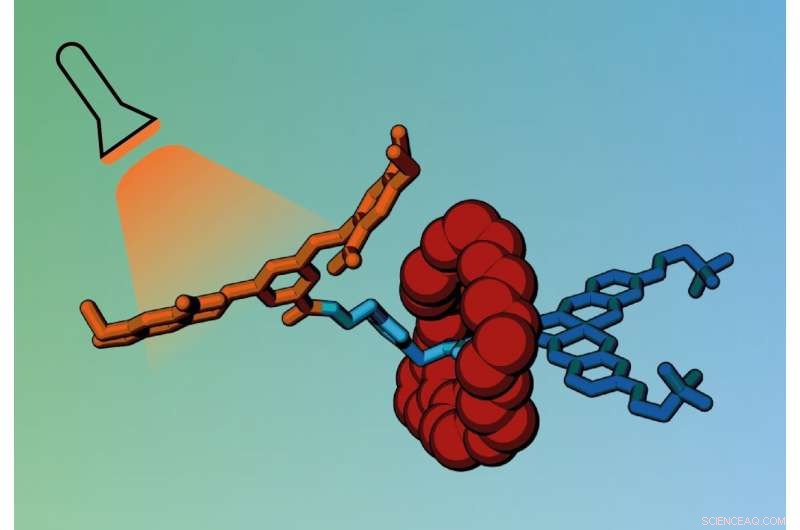
Det nye bur fungerer ved at 'fange' lægemiddelmolekyler i en ikke-toksisk bærer, der kan transportere lægemidlet til det nødvendige sted, før det frigives. Buret består af voluminøse molekylære grupper, der omslutter stoffet, blokerer dens biologiske aktivitet, indtil de løsnes ved påføring af en trigger.
For at lave buret, holdet brugte en bestemt type molekyle kaldet en rotaxan. Rotaxaner har en molekylær ring fanget på en håndvægtformet komponent, kaldet en aksel, som har stopgrupper i hver ende for at forhindre ringen i at glide af. Ringen fungerer som et molekylært skjold, blokerer adgangen til akslen og forhindrer den i at interagere med andre molekyler.
Forskerne designet en rotaxan med en aksel, der inkluderer et biologisk aktivt molekyle, der normalt dræber kræftceller ved at interagere med deres DNA. Mens ringen er til stede, det aktive molekyle kan ikke binde til DNA, lukker for dets toksicitet.
Imidlertid, når de udsættes for lys eller et specifikt enzym, den ene ende af akslen brækker af, frigiver ringen og lader det aktive molekyle binde til DNA i kræftceller.

Lys frigiver det aktive molekyle (blåt) fra det molekylære bur, lader den binde til kræftcellen (grå). Kredit:Imperial College London
Målrettet mod kræft
Det aktive molekyle, der er inkorporeret i rotaxanen, er særligt godt til at interagere med en speciel type DNA-struktur kaldet en G-quadruplex (G4). På grund af de biologiske roller, som disse DNA-strukturer spiller i celler, de er blevet foreslået som potentielle lægemiddelmål for kræft, giver forskerne håb om, at forbindelser, der kan interagere med G4'er, kan bruges i fremtiden som nye lægemidler mod kræft.
Forskerne testede først deres nye rotaxane-lægemiddelbærer ved hjælp af DNA-strenge ekstraheret fra celler og fandt ingen interaktion overhovedet, bekræfter, at rotaxanens ring blokerede adgangen til den aktive forbindelse.
Næste, de testede deres rotaxan i levende kræftceller, først viste, at rotaxanen fyldt med den aktive forbindelse ikke var toksisk for disse celler under normale forhold. Når de udsættes for lys, imidlertid, næsten alle kræftceller var døde inden for et par timer, demonstrerer, at den aktive forbindelse kunne frigives i de målrettede cancerceller på en meget kontrolleret måde.
Sporing af rotaxanen i kræftcellerne ved hjælp af konfokal mikroskopi viste, at før den skinnede lys forblev den i de ydre dele af cellen, som ikke indeholder DNA. Efter at der blev skinnet lys på cellerne, imidlertid, det frigivne aktive molekyle flyttede til kernen, hvor størstedelen af DNA'et i celler er lagret. Disse eksperimenter antydede, at det var den udløste binding til DNA, der fik kræftcellerne til at dø.
Professor Ramon Vilar sagde:"At være i stand til at levere lægemidler på det rigtige sted og på det rigtige tidspunkt er en vigtig udfordring i medicinsk kemi. Vores forskning viser, at det er muligt at opnå dette ved at indkapsle aktive molekyler i rotaxaner."
Klik på kemi
While light is a good trigger in terms of how well its location and intensity can be controlled, in practical use it would be limited to skin cancers or potentially those that can be reached inside the body with an endoscope. The researchers are therefore also testing the possibility of releasing the rotaxane ring with specific enzymes, such as those found in abundance only in cancer cells. Dr. Jamie Lewis said:
"'Click reactions, " which were used to prepare these rotaxanes, are easy and modular reactions that join up building blocks, like a molecular Lego kit. This is great because you can 'click' all sorts of different molecules together, making our approach very general and adaptable."
The modularity of their approach would allow researchers to use a different anti-cancer molecule or introduce an alternative mechanism for activation. Effectively, researchers could just choose the components they want and click them together using the same process.
 Varme artikler
Varme artikler
-
 Nanoteknologi kan hjælpe med at bekæmpe diabetes:Injicerbar nanogel kan overvåge blodsukkerniveau…Injicerbare nanopartikler udviklet på MIT kan en dag eliminere behovet for, at patienter med type 1-diabetes konstant skal overvåge deres blodsukkerniveauer og injicere sig selv med insulin. Nanopart
Nanoteknologi kan hjælpe med at bekæmpe diabetes:Injicerbar nanogel kan overvåge blodsukkerniveau…Injicerbare nanopartikler udviklet på MIT kan en dag eliminere behovet for, at patienter med type 1-diabetes konstant skal overvåge deres blodsukkerniveauer og injicere sig selv med insulin. Nanopart -
 Quantum-dot lasere er lovende for integrerede fotoniske kredsløbEn type laser, der er særligt velegnet til kvanteprikker, er en tilstandslåst laser, som passivt genererer ultrakorte pulser på mindre end et picosekund i varighed. Kredit:Peter Allen Tusinder af
Quantum-dot lasere er lovende for integrerede fotoniske kredsløbEn type laser, der er særligt velegnet til kvanteprikker, er en tilstandslåst laser, som passivt genererer ultrakorte pulser på mindre end et picosekund i varighed. Kredit:Peter Allen Tusinder af -
 Fysikere navngiver og kodificerer nyt felt inden for nanoteknologi:elektronkvantemetamaterialerNathaniel Gabor er lektor i fysik ved UC Riverside. Kredit:CIFAR. Når to atomisk tynde todimensionelle lag stables oven på hinanden, og det ene lag får det til at rotere mod det andet lag, de begy
Fysikere navngiver og kodificerer nyt felt inden for nanoteknologi:elektronkvantemetamaterialerNathaniel Gabor er lektor i fysik ved UC Riverside. Kredit:CIFAR. Når to atomisk tynde todimensionelle lag stables oven på hinanden, og det ene lag får det til at rotere mod det andet lag, de begy -
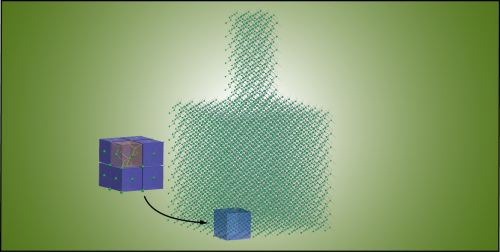 Nanoskala -søjler kan radikalt forbedre omdannelsen af varme til elektricitetDette viser en atomskala-model af et nanofononisk metamateriale. Vibrationerne forårsaget af søjlen bremser den vandrette varmestrøm gennem den tynde film. Kredit:Mahmoud Hussein Boulder -forskere
Nanoskala -søjler kan radikalt forbedre omdannelsen af varme til elektricitetDette viser en atomskala-model af et nanofononisk metamateriale. Vibrationerne forårsaget af søjlen bremser den vandrette varmestrøm gennem den tynde film. Kredit:Mahmoud Hussein Boulder -forskere
- Ny facilitet til at simulere forhold på Venus
- Fysikere studerer kompleks magnetisme i en sjælden jordforbindelse
- Hvad er en total solformørkelse, og hvorfor denne er så usædvanlig
- Hvordan er Math involveret i at blive en apoteket?
- Huawei sagsøger Verizon for påstået patentkrænkelse
- Italiens anti-Netflix-lov til beskyttelse af filmindustrien


