Bakteriebaserede biohybride mikrorobotter på en mission for en dag at bekæmpe kræft
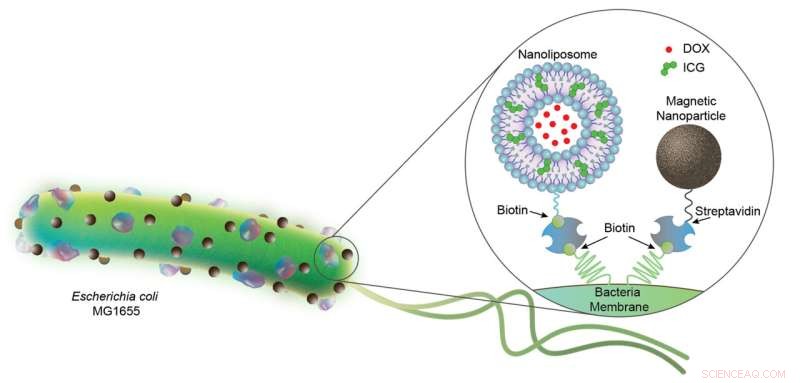
Figur 1. Bakterielle biohybrider, der bærer nanoliposomer (200 nm) og magnetiske nanopartikler (100 nm). Nanoliposomer er fyldt med kemoterapeutisk DOX og fototermisk middel ICG, og begge ladninger er konjugeret til E. coli-bakterier (2 til 3 µm i længden) via biotin-streptavidin-interaktioner. Kredit:Science Advances (2022). DOI:10.1126/sciadv.abo6163
Et team af forskere i afdelingen for fysisk intelligens ved Max Planck Institute for Intelligent Systems har kombineret robotteknologi med biologi ved at udstyre E. coli-bakterier med kunstige komponenter til at konstruere biohybride mikrorobotter. For det første, som det kan ses i figur 1, knyttede holdet flere nanoliposomer til hver bakterie. På deres ydre cirkel omslutter disse sfærisk-formede bærere et materiale (ICG, grønne partikler), der smelter, når det belyses af nær infrarødt lys. Længere mod midten, inde i den vandige kerne, indkapsler liposomerne vandopløselige kemoterapeutiske lægemiddelmolekyler (DOX).
Den anden komponent, forskerne knyttede til bakterien, er magnetiske nanopartikler. Når de udsættes for et magnetfelt, tjener jernoxidpartiklerne som en on-top booster til denne allerede meget bevægelige mikroorganisme. På denne måde er det nemmere at kontrollere svømningen af bakterier - et forbedret design mod en in vivo-applikation. I mellemtiden er rebet, der binder liposomerne og de magnetiske partikler til bakterien, et meget stabilt og svært at bryde streptavidin- og biotinkompleks, som blev udviklet et par år tidligere og rapporteret i en Nature artikel, og kommer til nytte, når man konstruerer biohybride mikrorobotter.
E. coli-bakterier er hurtige og alsidige svømmere, der kan navigere gennem materiale lige fra væsker til meget viskøst væv. Men det er ikke alt, de har også meget avancerede sanseevner. Bakterier trækkes til kemiske gradienter såsom lave iltniveauer eller høj surhedsgrad - begge udbredt nær tumorvæv. Behandling af kræft ved at injicere bakterier i nærheden er kendt som bakteriemedieret tumorterapi. Mikroorganismerne strømmer til, hvor tumoren er placeret, vokser der og aktiverer på den måde patienternes immunforsvar. Bakteriemedieret tumorterapi har været en terapeutisk tilgang i mere end et århundrede.
I de sidste par årtier har videnskabsmænd ledt efter måder at øge denne mikroorganismes superkræfter endnu mere. De udstyrede bakterier med ekstra komponenter for at hjælpe med at kæmpe kampen. Men tilføjelse af kunstige komponenter er ingen nem opgave. Komplekse kemiske reaktioner er på spil, og densitetshastigheden af partikler, der er lastet på bakterierne, har betydning for at undgå fortynding. Holdet i Stuttgart har nu hævet overliggeren ret højt. Det lykkedes dem at udstyre 86 ud af 100 bakterier med både liposomer og magnetiske partikler.
Forskerne viste, hvordan det lykkedes dem eksternt at styre sådan en højdensitetsløsning gennem forskellige kurser. Først gennem en L-formet smal kanal med to rum i hver ende, med en tumorsfæroid i hver. For det andet en endnu smallere opstilling, der ligner små blodkar. De tilføjede en ekstra permanent magnet på den ene side og viste, hvordan de præcist styrer de lægemiddelfyldte mikrorobotter mod tumorsfæroider. Og for det tredje – at gå et skridt videre – styrede holdet mikrorobotterne gennem en tyktflydende kollagengel (ligner tumorvæv) med tre niveauer af stivhed og porøsitet, lige fra blød til medium til stiv. Jo stivere kollagenet er, jo strammere er nettet af proteinstrenge, jo sværere bliver det for bakterierne at finde en vej gennem matrixen (Figur 2). Holdet viste, at når de tilføjer et magnetfelt, formår bakterierne at navigere helt til den anden ende af gelen, da bakterierne havde en højere kraft. På grund af konstant tilpasning fandt bakterierne en vej gennem fibrene.
Når først mikrorobotterne er akkumuleret på det ønskede punkt (tumorsfæroiden), genererer en nær infrarød laser stråler med temperaturer på op til 55 grader Celsius, hvilket udløser en smelteproces af liposomet og en frigivelse af de medfølgende lægemidler. Et lavt pH-niveau eller et surt miljø får også nanoliposomerne til at bryde op - derfor frigives lægemidlerne i nærheden af en tumor automatisk.
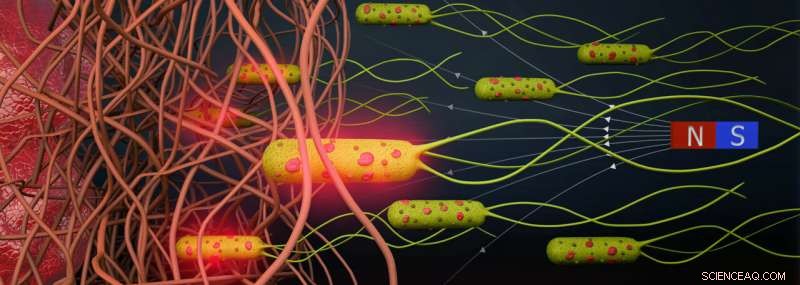
Figur 2. Skematisk, der viser bakterielle biohybride mikrorobotter magnetisk styret gennem fibrøse miljøer. Bakterielle biohybrider kan frigive deres nyttelast ved NIR-bestråling. Kredit:Science Advances (2022). DOI:10.1126/sciadv.abo6163
"Forestil dig, at vi ville injicere sådanne bakteriebaserede mikrorobotter i en kræftpatients krop. Med en magnet kunne vi præcist styre partiklerne mod tumoren. Når nok mikrorobotter omgiver tumoren, peger vi en laser på vævet og udløser derved frigivelsen af lægemidlet. Nu bliver ikke kun immunsystemet udløst til at vågne op, men de yderligere lægemidler hjælper også med at ødelægge tumoren," siger Birgül Akolpoglu, en Ph.D. studerende i Fysisk Efterretningsafdeling på MPI-IS. She is the first author of the publication titled "Magnetically steerable bacterial microrobots moving in 3D biological matrices for stimuli-responsive cargo delivery" co-led by former postdoctoral researcher in the Physical Intelligence Department, Dr. Yunus Alapan. It was published in Science Advances on July 15, 2022.
"This on-the-spot delivery would be minimally invasive for the patient, painless, bear minimal toxicity and the drugs would develop their effect where needed and not inside the entire body," Alapan adds.
"Bacteria-based biohybrid microrobots with medical functionalities could one day battle cancer more effectively. It is a new therapeutic approach not too far away from how we treat cancer today," says Prof. Dr. Metin Sitti, who leads the Physical Intelligence Department and is the last author of the publication. "The therapeutic effects of medical microrobots in seeking and destroying tumor cells could be substantial. Our work is a great example of basic research that aims to benefit our society." + Udforsk yderligere
Magnetic bacteria as micropumps
 Varme artikler
Varme artikler
-
 Nanopartikler kunne muliggøre en mere følsom og holdbar hurtig COVID-19-testEn 3D-printet enhed registrerer temperaturændringer, når SARS-CoV-2 binder til molekylært prægede polymernanopartikler (linealen viser cm). Kredit:Tilpasset fra ACS-sensorer 2022, DOI:10.1021/acssenso
Nanopartikler kunne muliggøre en mere følsom og holdbar hurtig COVID-19-testEn 3D-printet enhed registrerer temperaturændringer, når SARS-CoV-2 binder til molekylært prægede polymernanopartikler (linealen viser cm). Kredit:Tilpasset fra ACS-sensorer 2022, DOI:10.1021/acssenso -
 Forskning i cellebiologiens mysterium kan afsløre grundårsager til Alzheimers og andre sygdommeSamling af en hvælvingspartikel på et polyribosom. Til venstre viser begyndelsen af processen, hvor fire proteindimerer bringes sammen på polyribosomet. I midten er halvdelen af hvælvningen dannet
Forskning i cellebiologiens mysterium kan afsløre grundårsager til Alzheimers og andre sygdommeSamling af en hvælvingspartikel på et polyribosom. Til venstre viser begyndelsen af processen, hvor fire proteindimerer bringes sammen på polyribosomet. I midten er halvdelen af hvælvningen dannet -
 Elektro-optisk enhed giver løsning til hurtigere computerhukommelser og processorerKredit:CC0 Public Domain Den første integrerede enhed i nanoskala nogensinde, som kan programmeres med enten fotoner eller elektroner, er blevet udviklet af forskere i Harish Bhaskarans Advanced N
Elektro-optisk enhed giver løsning til hurtigere computerhukommelser og processorerKredit:CC0 Public Domain Den første integrerede enhed i nanoskala nogensinde, som kan programmeres med enten fotoner eller elektroner, er blevet udviklet af forskere i Harish Bhaskarans Advanced N -
 Den gyldne vej mod nye todimensionale halvledereTo-dimensionelle (2D) halvledere er lovende til kvanteberegning og fremtidig elektronik. Nu, forskere kan konvertere metallisk guld til halvleder og tilpasse materialet atom-for-atom på bornitrid-nano
Den gyldne vej mod nye todimensionale halvledereTo-dimensionelle (2D) halvledere er lovende til kvanteberegning og fremtidig elektronik. Nu, forskere kan konvertere metallisk guld til halvleder og tilpasse materialet atom-for-atom på bornitrid-nano
- Forskere viser, hvordan man laver sin egen supernova
- Æblers næste iPhones vil tage designelementer fra den nyeste iPad Pro, siger rapporten
- Opdagelse af en ny kilde til verdens dødeligste toksin
- Brug af droner til at forenkle filmanimation
- Hvad er temperaturen på en komet?
- 600 år gammel havsvamp har århundreder gamle klimarekorder


