Sukkerovertrukne nanopartikler målretter mod makrofager, omvendt lungefibrose

Kredit:Unsplash/CC0 Public Domain
Forskere ved University of Illinois Chicago har udviklet en behandling for lungefibrose ved at bruge nanopartikler belagt med mannose - en type sukker - for at stoppe en population af lungeceller kaldet makrofager, der bidrager til ardannelse i lungevæv. Cellemålretningsmetoden lover at forhindre denne alvorlige lungeardannelse, som kan resultere i livstruende komplikationer som åndenød.
Forskerne siger, at behandlingen endnu ikke er klar til at blive testet i kliniske forsøg, men dens succes i relevante dyremodeller er et lovende tegn på, at det kan være muligt at behandle sygdommen - som der er meget begrænsede og upræcise behandlinger til.
En væsentlig årsag til lungefibrose er aktiveringen af skadelige immunceller, der forårsager overdreven betændelse.
"Kroppens inflammatoriske processer er meget komplekse, og det er meget vanskeligt at finde behandlinger for sygdomme, der skyldes langvarig eller overdreven inflammation, fordi de behandlinger, der forhindrer skadelig betændelse, også - desværre - forhindrer hjælpsom inflammation, som bekæmper infektioner og helbreder skader," sagde Abhalaxmi Singh, gæsteforskningsassistent i afdelingen for farmakologi og regenerativ medicin ved UIC College of Medicine. "At have en målrettet behandling, der adresserede en grundlæggende årsag til skadeligt inflammationsarbejde i en dyremodel, er spændende."
Den coatede nanopartikelbehandling stopper fibrose ved at binde sig til en undergruppe af makrofager, en type hvide blodlegemer, der findes i alle organer, og som har en receptor for mannose, et sukkermolekyle. Denne receptor, kaldet CD206, er hyperudtrykt hos patienter med lungefibrose.
Forskerne fandt ud af, at de makrofager, der forårsager lungefibrose, har meget høje niveauer af mannose. Ved lungefibrose gennemgår makrofager en overgang, der frigiver cytokiner og fremmer ardannelse. Singh og hendes kolleger karakteriserede overfladerne af disse ar-fremmende makrofager og CD206 mannosereceptoren og designede en nano-vehikel til at målrette mod disse receptorer.
Når den sukkerovertrukne nanopartikel binder til cellens receptor, leverer den nukleotidet - et fragment af silencing RNA (siRNA) rettet mod transforming growth factor beta (TGFB) - som forskerne har indlæst i nanopartiklerne. SiRNA-målretning TGFB er en cellesignalvej, der vides at være involveret i lungefibrose. Når det først er i cellen, blokerer nukleotidet makrofagens evne til at lave for store mængder proteiner, såsom kollagen, involveret i ardannelse.
"Makrofager er spændende, komplekse celler, og den tilgang, Dr. Singh og vores team tog i belægningen af nanopartiklerne med sukker for at binde sig til mannosereceptoren, er en spændende og præcis måde at sikre målrettet levering af en lyddæmpende RNA-behandling til denne undergruppe af celler, som bidrage til fibrose," sagde Asrar Malik, Schweppe Family Distinguished Professor og leder af afdelingen for farmakologi og regenerativ medicin.
Holdet er allerede begyndt at teste behandlingen i humane lungevævsprøver med kolleger ved University of California i San Francisco.
Nanopartiklerne, der blev brugt i eksperimenterne, er formuleret ud fra et protein kaldet albumin, og det er en platform, som forskerne studerer som et værktøj til at levere terapeutika til en række forskellige tilstande.
Maliks team opdagede først, at albumin-nanopartikler kan bruges til at undertrykke inflammation på en præcis medicinsk måde. Deres oprindelige opdagelse blev rapporteret i en 2014 Nature Nanotechnology forskningsartikel. Opfinderne etablerede efterfølgende Nano Biotherapeutics, et uafhængigt opstartsfirma støttet af et National Institutes of Health fase II Small Business Technology Transfer-tilskud for at tiltrække de partnere og investorer, der er nødvendige for at bringe innovationen på markedet.
Den nye forskning er beskrevet i artiklen "Nanoparticle Targeting of de novo Pro-fibrotic Macrophages Mitigates Lung Fibrosis", som er publiceret i Proceedings of the National Academy of Sciences.
Artiklen er medforfatter af Sreeparna Chakraborty, Sing Wan Wong, Nicole Hefner, AndrewStuart, Abdul Qadir, Amitabha Mukhopadhyay, Kurt Bachmaier, Jae-Won Shin og Jalees Rehman. + Udforsk yderligere
Microgel-coating giver donorceller et boost i at vende lungefibrose
 Varme artikler
Varme artikler
-
 At lave en mini Mona LisaGeorgia Tech-forskere har skabt Mini Lisa på en substratoverflade på cirka 30 mikron i bredden. Billedet demonstrerer en teknik, der potentielt kan bruges til at opnå nano-fremstilling af enheder, for
At lave en mini Mona LisaGeorgia Tech-forskere har skabt Mini Lisa på en substratoverflade på cirka 30 mikron i bredden. Billedet demonstrerer en teknik, der potentielt kan bruges til at opnå nano-fremstilling af enheder, for -
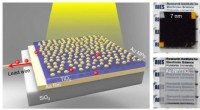 Fotoelektrode, der kan høste 85 procent af synligt lysTil venstre:Den nyudviklede fotoelektrode, en sandwich af halvlederlag (TiO2) mellem guldfilm (Au -film) og guldnanopartikler (Au NPer). Guldnanopartiklerne blev delvist indlagt på overfladen af tit
Fotoelektrode, der kan høste 85 procent af synligt lysTil venstre:Den nyudviklede fotoelektrode, en sandwich af halvlederlag (TiO2) mellem guldfilm (Au -film) og guldnanopartikler (Au NPer). Guldnanopartiklerne blev delvist indlagt på overfladen af tit -
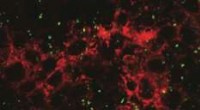 Indtagede nanopartikler kan være sundhedsskadeligeEt tarmcelle-monolag efter eksponering for nanopartikler, vist med grønt. (PhysOrg.com) -- Milliarder af konstruerede nanopartikler i fødevarer og lægemidler indtages af mennesker dagligt, og ny C
Indtagede nanopartikler kan være sundhedsskadeligeEt tarmcelle-monolag efter eksponering for nanopartikler, vist med grønt. (PhysOrg.com) -- Milliarder af konstruerede nanopartikler i fødevarer og lægemidler indtages af mennesker dagligt, og ny C -
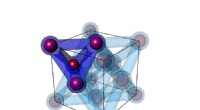 Byg hårde 3D nanomaterialer med DNAMineralisering af 3D-gitter dannet af DNA-tetraedre (ca. 30 nm) og guldnanopartikler til helt uorganiske 3D-silica-Au-replikaer med bevaret arkitektur. Kredit:Oleg Gang/Columbia Engineering Columb
Byg hårde 3D nanomaterialer med DNAMineralisering af 3D-gitter dannet af DNA-tetraedre (ca. 30 nm) og guldnanopartikler til helt uorganiske 3D-silica-Au-replikaer med bevaret arkitektur. Kredit:Oleg Gang/Columbia Engineering Columb
- Brandmændene forbereder sig på mudderskred, mens stormen bevæger sig ind i Californien
- Ny rapport fremhæver sammenhængen mellem luftforurening og spædbørnsdødelighed
- Frozen Zoo DNA kan afværge udryddelse af arter
- Nyt AI-værktøj identificerer kræftudfald ved hjælp af radiologirapporter
- Antibakterielle nanozymer:Heling af kroniske sår med nanokemi
- Hvordan virker en EMF-detektor?


