Forskere fra Prag udvider mulighederne for at bruge RNA i genmedicin
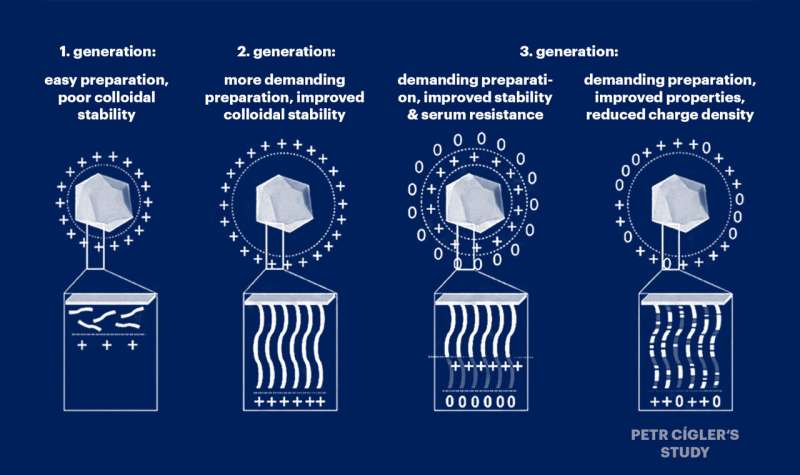
Dr. Petr Cígler og hans samarbejdspartnere arbejder på at forfine molekylære systemer til transport af ribonukleinsyre (RNA) molekyler ind i celler. Spørgsmålet om, hvordan man effektivt kan levere RNA til et udpeget sted i kroppen for at dæmpe et defekt gen, er en af de største udfordringer i det hastigt voksende område inden for genmedicin.
Nu har forskere fra Institut for Organisk Kemi og Biokemi ved Det Tjekkiske Videnskabsakademi (IOCB Prag) taget endnu et vigtigt skridt hen imod at nå dette mål. De har detaljeret beskrevet fremstillingen af et nyt sammensat vektor nanomateriale til transport af RNA, hvor de primært fokuserede på at sikre dets ikke-toksicitet for celler. Årsagen er, at skadeligheden af hidtil kendte nukleinsyrevektorer udgør en alvorlig hindring for udvidelsen af genterapi.
En artikel om emnet er blevet publiceret i Advanced Functional Materials .
Petr Cígler og hans kolleger arbejdede med den antagelse, at toksiciteten af nukleinsyrevektorer er forårsaget af en overdreven ophobning af positive ladninger langs kæderne af bærerpolymerer, der binder nukleinsyrer. Derfor fortyndede de systematisk denne positive ladning med uladede monomerer og fandt ud af, at dens lille fortynding ikke forringede systemets evne til at transportere nukleinsyrer.
I deres grundige undersøgelse beskriver de også, under hvilke omstændigheder nye materialer kan forberedes til brug i genmedicin. Forskerne var meget opmærksomme på de forhold, hvorunder disse stoffer binder nukleinsyrer mest effektivt og i hvilket støkiometrisk forhold.
Celler kan regulere oversættelsen af gener fra mRNA til proteiner på flere måder. En af dem er at dæmpe et gen ved hjælp af et siRNA (lille interfererende RNA) molekyle. Dette blokerer produktionen af målproteinet, hvilket er særligt nyttigt, hvis genet, der koder, er muteret eller på anden måde defekt. Derudover er det muligt at gribe ind, hvis oversættelsesreguleringens medfødte mekanismer er svækket. I et sådant tilfælde produceres der for meget af et protein i kroppen, hvilket er skadeligt for dets helbred.
"Genterapi er ikke kun yderst effektiv, men også akut målrettet. Dens største fordel ligger i, at den præcist målretter individuelle mutationer eller lidelser uden fare for at gå glip af målet. Ved hjælp af siRNA er det muligt at ramme selv en enkelt muteret ' bogstavet i et gen," siger Marek Kindermann, den første forfatter til undersøgelsen, og oplister de vigtigste fordele ved genterapi. I øjeblikket er fem lægemidler baseret på siRNA godkendt til verdensomspændende brug, og der er omkring et dusin flere på "ventelisten."
Den terapeutiske anvendelse af siRNA hæmmes af, at siRNA-molekyler er ustabile og derfor nedbrydes meget hurtigt i kroppen. Eksperter rundt om i verden adresserer derfor problemet med, hvordan man leverer siRNA til et udpeget sted og lader det gøre sit job, som er at stoppe eller begrænse produktionen af et bestemt uønsket protein ved at dæmpe genet for det.
Denne opgave blev også taget op af Petr Cíglers team ved IOCB Prag sammen med kolleger fra Institut for Mikrobiologi ved Det Tjekkiske Videnskabsakademi, ledet af lederen af Nanomedicin-gruppen, Dr. Veronika Benson.
"Hvert transportsystem er designet til at opfylde to grundlæggende mål:For det første har det til opgave at beskytte molekylet mod henfald, og for det andet skal det sikre dets transport ind i cellen, så det når cytosolen og opfylder sin mission som en stof der," forklarer Petr Cígler.
"I vores undersøgelse beskæftiger vi os meget detaljeret med transportsystemets egenskaber. Vi falder helt ned til niveauet af strukturelle detaljer af molekyler, der interagerer med nukleinsyrer. Vi beskriver de betingelser, der er nødvendige for, at siRNA med succes kan binde til transportere nanosystemet og derefter nå det intracellulære rum."
Forskere fra IOCB Prag baner således vejen for brugen af partikler, der omtales som ikke-virale vektorer, som ikke udnytter vira til at bære RNA. De har placeret hele transportsystemet, inklusive nukleinsyren, på overfladen af diamantnanopartikler. Det er markant stabile bærerpartikler, som også udsender en særlig type fluorescens. Dette gør det muligt at spore deres rejse gennem væv og overvåge, hvordan de opfører sig inde i celler.
En komplikation er, at det er svært for kroppen at slippe af med nanodiamanter, så denne genterapimetode er hovedsageligt velegnet til behandling af svært helende overfladiske sår. Det er til disse typer terapi, med fokus på heling af bensår hos patienter med diabetes, at de nye transport-nanomaterialer, præsenteret i dette og andre værker af teamet af Dr. Cígler og samarbejdspartnere, er tiltænkt.
Deres seneste dybdegående undersøgelse blev også muliggjort takket være AMULET-projektet, som fokuserer på udviklingen af multi-skala nanomaterialer og samler otte partnere ledet af Jaroslav Heyrovský Institute of Physical Chemistry.
Flere oplysninger: Marek Kindermann et al., Designregler for Nano-Bio Interface af Nanodiamonds:Implikationer for siRNA Vectorization, Avancerede funktionelle materialer (2024). DOI:10.1002/adfm.202314088
Journaloplysninger: Avancerede funktionelle materialer
Leveret af Institute of Organic Chemistry and Biochemistry i CAS
 Varme artikler
Varme artikler
-
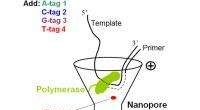 Forskere rapporterer om en ny tilgang til elektronisk DNA-sekventering af enkeltmolekylerSkematisk af enkeltmolekyle DNA-sekventering af en nanopore med fosfatmærkede nukleotider. Hvert af de fire nukleotider vil bære et andet mærke. Under SBS, disse tags, bundet via nukleotidets terminal
Forskere rapporterer om en ny tilgang til elektronisk DNA-sekventering af enkeltmolekylerSkematisk af enkeltmolekyle DNA-sekventering af en nanopore med fosfatmærkede nukleotider. Hvert af de fire nukleotider vil bære et andet mærke. Under SBS, disse tags, bundet via nukleotidets terminal -
 Ny kemi til ultratynde gassensorerKredit:CC0 Public Domain Anvendelsen af zinkoxidlag i industrien er mangfoldig og spænder fra beskyttelse af nedbrydelige varer til påvisning af giftig nitrogenoxidgas. Sådanne lag kan aflejres
Ny kemi til ultratynde gassensorerKredit:CC0 Public Domain Anvendelsen af zinkoxidlag i industrien er mangfoldig og spænder fra beskyttelse af nedbrydelige varer til påvisning af giftig nitrogenoxidgas. Sådanne lag kan aflejres -
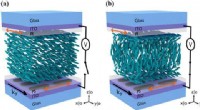 Arrays af metalliske nanopartikler kan danne et optisk hulrum, der kan indstilles af flydende krysta…FIG. 1. (a) Skematisk repræsentation af enheden med plan LC. Enheden består af et glassubstrat belagt med ITO med et nanopartikelarray fremstillet på toppen og dækket af et PS-justeringslag. LC-laget
Arrays af metalliske nanopartikler kan danne et optisk hulrum, der kan indstilles af flydende krysta…FIG. 1. (a) Skematisk repræsentation af enheden med plan LC. Enheden består af et glassubstrat belagt med ITO med et nanopartikelarray fremstillet på toppen og dækket af et PS-justeringslag. LC-laget -
 Fastsættelse af spilleregler for nanoteknologisk forskningDenne mesokosmos, der bruges af Center for Miljøimplikationer af Nanoteknologi, er dybest set en lille, selvstændigt økosystem med integrerede sensorer, der bruges til at studere, hvordan nanopartikle
Fastsættelse af spilleregler for nanoteknologisk forskningDenne mesokosmos, der bruges af Center for Miljøimplikationer af Nanoteknologi, er dybest set en lille, selvstændigt økosystem med integrerede sensorer, der bruges til at studere, hvordan nanopartikle
- Amazon investerer i det britiske madbud Deliveroo
- 5 ting, du ikke vidste om efterårsjævndøgn
- Amazon lover at være CO2-neutral i 2040
- Schweizisk ureeksport tikker frem i april
- Ny formulering tillader brug af toksin fra klapperslangegift til behandling af kroniske smerter
- Forskere demonstrerer potentialet i et nyt kvantemateriale til at skabe to spintronic -teknologier


