Nye nanosensorer gør diagnostiske procedurer mere følsomme

Fraunhofer Institute for Microelectronic Circuits and Systems IMS og Ruhr University Bochum, Tyskland, har udviklet en proces, der muliggør en ny form for signalforstærkning til diagnostiske tests. Gennem den avancerede brug af selvlysende enkeltvæggede kulstofnanorør i bioanalytik kan testprocedurer udføres mere følsomt, hurtigt og billigt.
Sensorerne kan bruges til enzymatiske processer. Deres tilpasningsevne til forskellige reaktionsbetingelser åbner op for en bred vifte af anvendelser for standardmetoder såsom ELISA'er, en forkortelse for Enzyme-linked Immunosorbent Assay.
Resultaterne blev offentliggjort den 15. december 2023 i Angewandte Chemie International Edition . De åbner op for nye muligheder for at forbedre diagnostiske procedurer og gemme detektionsmidler.
Diagnostiske grænser kan forbedres med lysende kulstofsensor
Mange diagnostiske procedurer bruger lys til at detektere mængden af et bestemt stof. Dette kan være et farvet stof eller et selvlysende stof. Desværre er der mange baggrundssignaler i det synlige lysområde. For at skifte det optiske signal fra en måling til et bedre spektralområde brugte forskerne kulstofrør på mindre end en nanometer i diameter. Dette er omkring 100.000 gange tyndere end et menneskehår.
Sensorerne fluorescerer i det nær-infrarøde område, som ikke er synligt for det menneskelige øje, og bleger ikke. Derudover er sensorernes fluorescens følsom over for deres kemiske miljø på grund af en modifikation på deres overflade. Dette gør det muligt at observere kemiske reaktioner og detektere reaktionsprodukter, når de interagerer med nanorøret.
Nanorørenes fluorescens flytter signalet ind i det nær-infrarøde område, hvilket kombineret med nanorørernes høje følsomhed resulterer i et skift i detektionsgrænsen. Dette er f.eks. vigtigt, når sygdomsmarkører er til stede i meget lave niveauer i en infektion eller sygdom såsom kræft.
Evnen til at skræddersy nanorørene til forskellige analytter åbner op for en bred vifte af muligheder, herunder en forøgelse af følsomheden. Denne gevinst i følsomhed giver mulighed for et potentielt skift i detektionsgrænser, hvilket kan føre til både materiale- og tidsbesparelser i diagnostiske processer. Denne innovative tilgang kunne øge effektiviteten af detektionsmetoder i medicinsk diagnostik betydeligt.
Gruppen demonstrerede, at det nye sensorprincip virker ved at bruge substraterne p-phenylendiamin og tetramethylbenzidin til enzymet peberrodsperoxidase. "Dette enzym bruges i en række biokemiske detektionsmetoder," forklarer Justus Metternich fra Fraunhofer IMS.
"I princippet kan konceptet dog anvendes på alle slags systemer. For eksempel har vi også undersøgt enzymet β-galactosidase, som er af interesse til diagnostiske anvendelser. Med få modifikationer vil det også kunne bruges i bioreaktioner ."
I fremtiden planlægger gruppen at tilpasse sensorerne til andre applikationer. For eksempel kan sensorerne, afhængigt af anvendelsen, gøres mere stabile med såkaldte kvantefejl. "Det vil især være fordelagtigt, hvis man ikke kun vil måle i simple vandige opløsninger, men også vil følge enzymatiske reaktioner i komplicerede miljøer med celler, i blodet eller i selve en bioreaktor," forklarer Sebastian Kruss, professor i fysisk kemi ved Ruhr University Bochum og leder af Attract Group Biomedical Nanosensors ved Fraunhofer IMS.
Flere oplysninger: Justus T. Metternich et al., Signal Amplification and Near-Infrared Translation of Enzymatic Reactions by Nanosensors, Angewandte Chemie International Edition (2023). DOI:10.1002/anie.202316965
Leveret af Ruhr-Universitaet-Bochum
 Varme artikler
Varme artikler
-
 Titandioxid som en nanoskala sensor for mekanisk belastningForskere fra EPFL, Tyskland og Frankrig har afsløret en ny ejendom af det billige og rigelige materiale anatase titandioxid, som lover applikationer som et medium for stuetemperatur-nanosensorer af me
Titandioxid som en nanoskala sensor for mekanisk belastningForskere fra EPFL, Tyskland og Frankrig har afsløret en ny ejendom af det billige og rigelige materiale anatase titandioxid, som lover applikationer som et medium for stuetemperatur-nanosensorer af me -
 Metoden tilbyder billig billeddannelse i skalaen af viruspartiklerMIT-ingeniører har udtænkt en ny teknik til billeddannelse af biologiske prøver ned til en opløsning på 9 nanometer. De udviklede en ny type hydrogel, der bevarer en mere ensartet konfiguration, afbil
Metoden tilbyder billig billeddannelse i skalaen af viruspartiklerMIT-ingeniører har udtænkt en ny teknik til billeddannelse af biologiske prøver ned til en opløsning på 9 nanometer. De udviklede en ny type hydrogel, der bevarer en mere ensartet konfiguration, afbil -
 Fra levende computere til nano-robotter:hvordan tog DNA ud over genetikMolekylær computer. Kredit:Shutterstock DNA er et af de mest fantastiske molekyler i naturen, giver en måde at bære de nødvendige instruktioner til at skabe næsten enhver livsform på Jorden i en m
Fra levende computere til nano-robotter:hvordan tog DNA ud over genetikMolekylær computer. Kredit:Shutterstock DNA er et af de mest fantastiske molekyler i naturen, giver en måde at bære de nødvendige instruktioner til at skabe næsten enhver livsform på Jorden i en m -
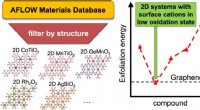 På jagt efter ultratynde materialer ved hjælp af data mining:Undersøgelse identificerer omfattend…Grafisk abstrakt. Kredit:Nano Letters (2022). DOI:10.1021/acs.nanolett.1c03841 Todimensionelle (2D) materialer har ekstraordinære egenskaber. De består normalt af atomlag, der kun er nogle få nanom
På jagt efter ultratynde materialer ved hjælp af data mining:Undersøgelse identificerer omfattend…Grafisk abstrakt. Kredit:Nano Letters (2022). DOI:10.1021/acs.nanolett.1c03841 Todimensionelle (2D) materialer har ekstraordinære egenskaber. De består normalt af atomlag, der kun er nogle få nanom
- Hvorfor absorberer æggekartoner lyd?
- Google står over for EU's antitrustbøder på grund af Android:kilder
- Hvordan hjælper solenergi miljøet?
- Hvor længe kan et menneske overleve i det ydre rum?
- Meteoritter viser transport af materiale i det tidlige solsystem
- Blocky and Raw:Er brutalismearkitektur på vej tilbage?


