Lægemiddelleveringsteknik med karmålrettede guldnanopartikler viser voksende løfter for behandling af hjernekræft

En teknik udviklet af University of Texas i Dallas og UT Southwestern Medical Center-forskere til at levere medicin gennem blod-hjerne-barrieren har vist lovende i et præklinisk studie til behandling af glioblastom, den mest almindelige kræft i hjernen hos mennesker.
Forskerne demonstrerede metoden i mus i en undersøgelse offentliggjort i Nature Communications .
Glioblastom er en aggressiv hjernekræft, der rammer omkring 12.000 mennesker årligt i USA; patienter har en median overlevelse på 15 til 18 måneder efter diagnosen. Nuværende behandlinger, som omfatter kirurgi, kemoterapi og stråling, er stort set ineffektive. Det er svært at få kemoterapi ind i glioblastom-tumorer, fordi de fleste medicin ikke passerer gennem blod-hjerne-barrieren, som er en unik egenskab ved blodkar i hjernen, der begrænser og aktivt forhindrer stoffer i blodbanen i at nå hjerneparenkymet.
Barrieren fungerer som et meget selektivt filter og en beskyttende barriere for hjernen, sagde medkorresponderende forfatter til undersøgelsen Dr. Zhenpeng Qin, lektor i maskinteknik og stipendiat, Eugene McDermott professor ved Erik Jonsson School of Engineering and Computer Science.
"Den største udfordring ved at behandle enhver hjernesygdom er denne barriere. Den er fantastisk; den er kun en mikron tyk, men den forhindrer 98% af molekylerne i at komme ind i hjernen," sagde Qin. Til sammenligning er diameteren af menneskehår 70 mikron.
Qin samarbejdede med UT Southwestern-kolleger Dr. Robert Bachoo, medkorresponderende forfatter og lektor i neurologi og intern medicin, og Dr. Elizabeth Maher, professor i intern medicin og neurologi. Forskningen involverede gensplejsede mus, der havde mutationer fundet i humane glioblastompatienter.
Qins lægemiddelleveringsmetode er afhængig af samlevering af medicin med karmålrettede guldnanopartikler, som sprøjtes ind i blodbanen. Fra en ekstern kilde påfører forskere korte laserimpulser, som passerer gennem musekraniet og aktiverer guldnanopartiklerne. Denne aktivering genererer termomekaniske bølger og gør kortvarigt blod-hjerne-barrieren permeabel, hvilket gør det muligt for medicin at nå sit mål. I deres eksperimenter brugte forskere paclitaxel, et kemoterapilægemiddel, der bruges til at behandle ovarie-, bryst- og lungekræft, som blev forladt til potentiel brug mod hjernekræft, fordi lægemiddelmolekylet i sig selv ikke krydser barrieren.
Undersøgelsen viste, at den nye tilgang overvandt barrieren, selvom der vil være behov for mange års forskning, før metoden kan testes på mennesker. Yderligere prækliniske undersøgelser er i gang.
"Tumorerne krympede i størrelse, og vi udvidede overlevelsen med mere end 50%," sagde Qin. "Vi håber, at dette vil føre til udvidede terapeutiske muligheder for behandling af sygdomme i hjernen og centralnervesystemet."
Flere oplysninger: Qi Cai et al., Optisk blod-hjerne-tumor-barrieremodulation udvider terapeutiske muligheder for behandling af glioblastom, Nature Communications (2023). DOI:10.1038/s41467-023-40579-1
Journaloplysninger: Nature Communications
Leveret af University of Texas i Dallas
 Varme artikler
Varme artikler
-
 Skiftende lys med et sølvatomSwitchen er baseret på den spændingsinducerede forskydning af et eller flere sølvatomer i det smalle mellemrum mellem en sølv- og en platinplade. Kredit:Alexandros Emboras / ETH Zürich Forskere, d
Skiftende lys med et sølvatomSwitchen er baseret på den spændingsinducerede forskydning af et eller flere sølvatomer i det smalle mellemrum mellem en sølv- og en platinplade. Kredit:Alexandros Emboras / ETH Zürich Forskere, d -
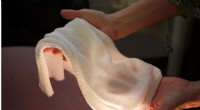 Forskere udvikler det første stof til automatisk at afkøle eller isolere afhængigt af forholdeneDette nye stof, der er udviklet af University of Maryland-forskerne YuHuang Wang og Ouyang Min, er det første tekstil, der automatisk ændrer egenskaber for at fange eller frigive varme afhængigt af fo
Forskere udvikler det første stof til automatisk at afkøle eller isolere afhængigt af forholdeneDette nye stof, der er udviklet af University of Maryland-forskerne YuHuang Wang og Ouyang Min, er det første tekstil, der automatisk ændrer egenskaber for at fange eller frigive varme afhængigt af fo -
 Ekstremt stærk nano-twinned ren nikkel med ekstrem fin tvillingtykkelseTypisk mikrostruktur af aflejret NT-Ni med en ekstrem fin tvillingtykkelse. (A) Tredimensionel struktur af NT-Ni sammensat af plan-view og tværsnit af lysfelt TEM-billeder. (B) Fordelinger af tvilling
Ekstremt stærk nano-twinned ren nikkel med ekstrem fin tvillingtykkelseTypisk mikrostruktur af aflejret NT-Ni med en ekstrem fin tvillingtykkelse. (A) Tredimensionel struktur af NT-Ni sammensat af plan-view og tværsnit af lysfelt TEM-billeder. (B) Fordelinger af tvilling -
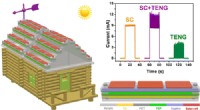 Udnyttelse af sol- og vindenergi i én enhed kan drive tingenes internetKredit:American Chemical Society Tingenes Internet kunne gøre byer klogere ved at forbinde et omfattende netværk af små kommunikationsenheder for at gøre livet mere effektivt. Men alle disse maski
Udnyttelse af sol- og vindenergi i én enhed kan drive tingenes internetKredit:American Chemical Society Tingenes Internet kunne gøre byer klogere ved at forbinde et omfattende netværk af små kommunikationsenheder for at gøre livet mere effektivt. Men alle disse maski
- Californien planlægger at øge vandforsyningen, da tørken bider
- Hvordan 'Jurassic Park' ændrede filmproduktion og vores syn på dinosaurer
- Forklarer:Hvorfor gravitationsbølgeforskere vandt en Nobel
- Kan økologiske plantebeskyttelsesmidler skade afgrøder?
- Ingeniør-klinikerteamet bruger aktive rynker til at holde syntetiske transplantater rene
- NASA dækker orkanen Isaacs flosset center


