Rationelt design af mRNA nanovaccine til cancerimmunterapi
Messenger RNA (mRNA) vacciner revolutionerer behandlingen af kræft. De kan udvikles fleksibelt på kort tid, hvilket muliggør forbigående ekspression af flere antigener for sikker og effektiv immunisering. En mangfoldighed af mRNA-vacciner udforskes i klinikken til gavn for patienter med cancer.
Imidlertid er translationen af mRNA-vacciner stadig hæmmet af flertrins leveringsbarrierer, før stærk immunitet påbegyndes, herunder hurtig clearance, dårlig målretning mod lymfoide organer og dendritiske celler, katalytisk hydrolyse og svag evne til at passere gennem phospholipid-dobbeltlag. Derudover kan vaccination med mRNA alene næppe inducere stærke immunresponser i fravær af adjuvanser. Det er fortsat udfordrende at forbedre cytosolisk levering af mRNA og fremme dets in vivo-vaccinationseffektivitet i kombination med adjuvanser.
I de seneste årtier er et stort antal nanobærere blevet rapporteret at fremme transfektionseffektiviteten af nukleinsyrelægemidler eller levere lægemidler til lymfeknuder. Disse undersøgelser giver værdifulde egenskaber, herunder størrelse, overfladeladning, modifikation, reaktionsevne, komponenter og cytotoksicitet for at nå målet om lymfeknudedræning eller cytosolisk adgang.
Maskinlæringsteknikker giver kraftfulde værktøjer til at udforske de fysisk-kemiske egenskaber og biologiske egenskaber ved disse nanopartikler og letter design af nanobærere med høj effektivitet. Almindeligvis blev maskinlæringsmodeller trænet, udvalgt og optimeret med høj kvalitet og massive datasæt fra beregninger og high-throughput eksperimentelle data, og de guider igen det rationelle design, screening og optimering af nanocarriers.
Ved at udnytte eksisterende nanocarriers databaser kan maskinlæring give indsigt i rationelt design af nanovacciner med høj effektivitet.
I en ny forskningsartikel offentliggjort i National Science Review , brugte forskere fra det kinesiske videnskabsakademi og Shanghai Jiao Tong University maskinlæring til at guide det rationaliserede design af mRNA nanovacciner. Denne undersøgelse identificerede nøgleparametrene for nanovacciner til effektiv levering af mRNA og cGAMP baseret på en maskinlæringsmodel fra Nanocarrier-databasen.
mRNA/cGAMP nanokomplekserne baseret på phenylboronsyre podet polyethylenimin blev fremstillet og yderligere indkapslet med anioniske lipider for at opnå nanovaccinen.
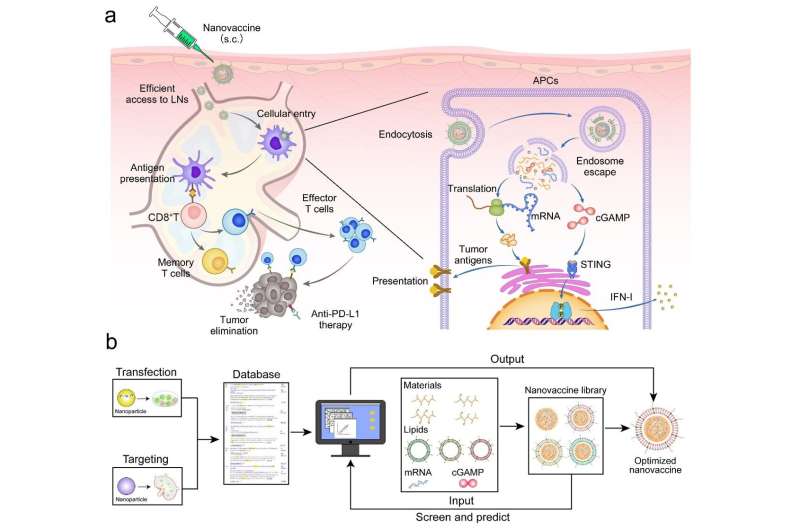
(1) Den negative overfladeladning af nanovaccinen reducerer interaktionen med negativt ladede glycosaminoglycaner i matrix og forbedrer akkumulering i lymfeknuderne.
(2) Nanovaccinen, efter at være blevet internaliseret af de antigen-præsenterende celler (APC'er) i lymfeknuderne, fremmer frigivelsen af mRNA og cGAMP fra endosomerne til cytoplasmaet, hvilket aktiverer STING-vejen og inducerer præsentationen af tumorantigener.
(3) Aktiveringen af STING-vejen fremmer frigivelsen af IFN-I, som aktiverer T-celle-immunrespons for at dræbe tumorceller og hæmme tumorvækst og metastase. Sammenlignet med mRNA alene viste den terapeutiske strategi baseret på denne nanovaccine stærkere antitumoreffekter i modeller for melanom og kolorektal cancer.
Artiklen er publiceret i tidsskriftet National Science Review .
Flere oplysninger: Lei Zhou et al., STING-agonist-boostet mRNA-immunisering via intelligent design af nanovacciner til forbedring af cancerimmunterapi, National Science Review (2023). DOI:10.1093/nsr/nwad214
Leveret af Science China Press
 Varme artikler
Varme artikler
-
 Hvad verdens mindste monstertruck afslørerOhio Universitys monstertruck i nanostørrelse førte til et mærkeligt fund. Kredit:Eric Masson, Ph.D. Verdens korteste løb efter distance - en brøkdel af bredden af et menneskehår - blev kørt på
Hvad verdens mindste monstertruck afslørerOhio Universitys monstertruck i nanostørrelse førte til et mærkeligt fund. Kredit:Eric Masson, Ph.D. Verdens korteste løb efter distance - en brøkdel af bredden af et menneskehår - blev kørt på -
 En biomimetisk membran til afsaltning af havvand i industriel skalaKunstige vandkanaler indsat i en polyamidmembran © Mihail Barboiu, Institut Européen des Membranes. Kredit:CNRS/ENSC Montpellier/University of Montpellier Behandling af havvand, herunder dens stor
En biomimetisk membran til afsaltning af havvand i industriel skalaKunstige vandkanaler indsat i en polyamidmembran © Mihail Barboiu, Institut Européen des Membranes. Kredit:CNRS/ENSC Montpellier/University of Montpellier Behandling af havvand, herunder dens stor -
 Fremstilling af grafenadditiv til fleksibel og printbar elektronikKredit:CC0 Public Domain Forskning ledet af Kansas State Universitys Suprem Das, assisterende professor i industri- og produktionssystemteknik, i samarbejde med Christopher Sørensen, universitets
Fremstilling af grafenadditiv til fleksibel og printbar elektronikKredit:CC0 Public Domain Forskning ledet af Kansas State Universitys Suprem Das, assisterende professor i industri- og produktionssystemteknik, i samarbejde med Christopher Sørensen, universitets -
 Zero gravitation graphene lover succes i rummetProfessor Ferrari under flyvningen. Kredit:University of Cambridge I en række spændende eksperimenter, Cambridge -forskere oplevede vægtløshed ved at teste grafens anvendelse i rummet. Arbejder s
Zero gravitation graphene lover succes i rummetProfessor Ferrari under flyvningen. Kredit:University of Cambridge I en række spændende eksperimenter, Cambridge -forskere oplevede vægtløshed ved at teste grafens anvendelse i rummet. Arbejder s
- Hvordan laver man et fælde til gule jakker
- De første oceaner kan have været sure
- Et cellulært gennembrud:Højtydende CRISPR uden virale vektorer
- Pinpoint laseropvarmning skaber en malstrøm af magnetiske nanoteksturer
- Er glasovergangen drevet af termodynamik?
- Nuklear scanningsteknik vil bringe fordele til mineindustrien


