Hvad er oxideret i en galvanisk celle lavet med sølv og nikkel elektroloder?
Den overordnede reaktion for denne celle er:
$$Ni(s) + 2Ag^+(aq) → Ni^{2+}(aq) + 2Ag(s)$$
I denne reaktion oxideres nikkelmetal fra en neutral tilstand til en +2 oxidationstilstand, mens sølvioner reduceres fra en +1 oxidationstilstand til en neutral tilstand.
Derfor er nikkel det stof, der oxideres i denne galvaniske celle.
Sidste artikelHvilke metaller er fleksible?
Næste artikelHvilken løsning kan du bruge til at omkrystallisere et Mn-salen-kompleks?
 Varme artikler
Varme artikler
-
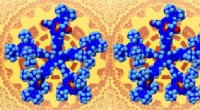 Oprustning af maskiner i nanoskalaEt tog af molekylære tandhjul sammensat af stjerneformede molekyler. Kredit:Gwénaël Rapenne (NAIST og UPS) Geartog er blevet brugt i århundreder til at omsætte ændringer i gearets rotationshastigh
Oprustning af maskiner i nanoskalaEt tog af molekylære tandhjul sammensat af stjerneformede molekyler. Kredit:Gwénaël Rapenne (NAIST og UPS) Geartog er blevet brugt i århundreder til at omsætte ændringer i gearets rotationshastigh -
 Fysikere opfinder intelligent kvantesensor for lysbølgerDenne kunstneriske gengivelse skildrer den intelligente sanseproces af todimensionelle materialer kaldet moiré-metamaterialer. Metamaterialets kvantegeometriske egenskaber bestemmer, hvordan det reage
Fysikere opfinder intelligent kvantesensor for lysbølgerDenne kunstneriske gengivelse skildrer den intelligente sanseproces af todimensionelle materialer kaldet moiré-metamaterialer. Metamaterialets kvantegeometriske egenskaber bestemmer, hvordan det reage -
 Hvordan guldnanopartikler kunne forbedre lagring af solenergiNår de udsættes for sollys, stjerneformede guldnanopartikler belagt med en halvleder muliggør effektiv produktion af brint fra vand. Kredit:Ashley Pennington/Rutgers University-New Brunswick Stjer
Hvordan guldnanopartikler kunne forbedre lagring af solenergiNår de udsættes for sollys, stjerneformede guldnanopartikler belagt med en halvleder muliggør effektiv produktion af brint fra vand. Kredit:Ashley Pennington/Rutgers University-New Brunswick Stjer -
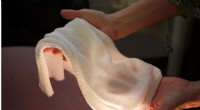 Forskere udvikler det første stof til automatisk at afkøle eller isolere afhængigt af forholdeneDette nye stof, der er udviklet af University of Maryland-forskerne YuHuang Wang og Ouyang Min, er det første tekstil, der automatisk ændrer egenskaber for at fange eller frigive varme afhængigt af fo
Forskere udvikler det første stof til automatisk at afkøle eller isolere afhængigt af forholdeneDette nye stof, der er udviklet af University of Maryland-forskerne YuHuang Wang og Ouyang Min, er det første tekstil, der automatisk ændrer egenskaber for at fange eller frigive varme afhængigt af fo
- Hvordan man laver ting float i vand
- Dage efter jordskælvet i Idahos, eksperter søger svar om historisk, uventet hændelse
- Google appellerer en bøde på 5 milliarder dollars i EU i Android-antitrustsag
- Er printerblæk biologisk nedbrydeligt?
- ATLAS-eksperiment måler lysspredning på lys og begrænser axion-lignende partikler
- Kræftlægemidler kører en tur på smarte guld -nanoshells


