Bohr -modellen:hurtigt udskiftet, men aldrig glemt
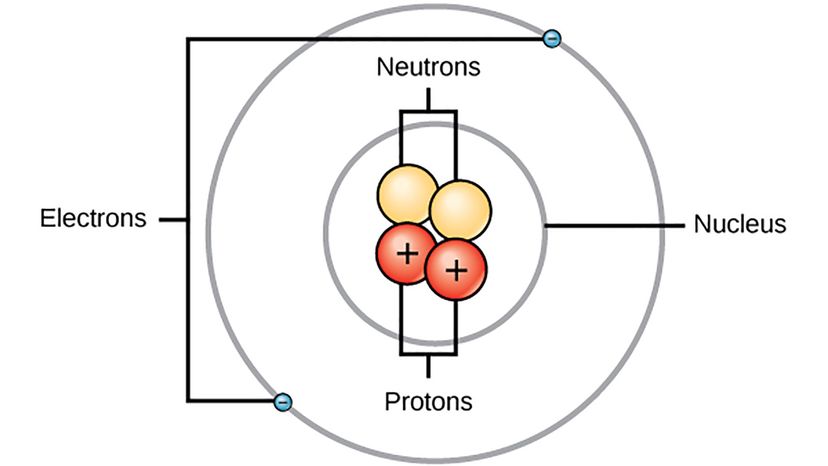 Bohrs model af atomet. Wikimedia Commons (CC BY 4.0)
Bohrs model af atomet. Wikimedia Commons (CC BY 4.0) Du kan søge efter et billede af et atom på internettet, og du finder et, selvom ingen faktisk har set et atom før. Men vi har et skøn over, hvordan et enkelt atom ser ud på grund af arbejdet fra en flok forskellige forskere som den danske fysiker Niels Bohr.
Atomer er byggestenene i materie - et enkelt atom af ethvert enkelt element er den mest grundlæggende enhed i naturen, der stadig overholder de fysiske regler, vi kan observere i hverdagen (de subatomære partikler, der udgør atomer har deres egne særlige regler) . Forskere formodede atomer eksisterede i lang tid, før de kunne konceptualisere deres struktur - selv de gamle grækere regnede med, at universets sag bestod af komponenter, der var så små, at de ikke kunne opdeles i noget mindre, og de kaldte disse grundlæggende enheder atomos , hvilket betyder "udelt". I slutningen af 1800 -tallet, man forstod, at kemiske stoffer kunne nedbrydes til atomer, som var meget små og atomer af forskellige grundstoffer havde en forudsigelig vægt.
Men derefter, i 1897, Den britiske fysiker J.J. Thomson opdagede elektroner-negativt ladede partikler inde i atomer, som alle havde brugt den store del af et århundrede på at tro var helt udelelige-som de mindste ting, der fandtes. Thomson antog bare, at der fandtes elektroner, men han kunne ikke finde ud af, hvordan elektroner passer ind i et atom. Hans bedste gæt var "blommebudding -modellen, "som skildrede atomet som en positivt ladet tærte besat med negativt ladede områder spredt rundt som frugt i en gammeldags dessert.
"Elektroner viste sig at være negative elektriske, og alle med samme masse og meget lille sammenlignet med atomer, "siger Dudley Herschbach, en Harvard -kemiker, der delte Nobelprisen i kemi i 1986 for sine "bidrag vedrørende dynamikken i kemiske elementære processer, "i en e -mail." Ernest Rutherford opdagede kernen i 1911. Kerner var positive elektriske, med forskellige masser, men meget større end elektroner, alligevel meget lille i størrelse. "
Et kæmpe spring fremad
Niels Bohr var Rutherfords studerende, der overtog hans mentors projekt med at tyde atomets struktur i 1912. Det tog ham kun et år at komme med en arbejdsmodel af et brintatom.
"Bohrs model fra 1913 for brintatomet havde cirkulære elektronbaner omkring protonen - som jordens kredsløb omkring solen, "siger Herschbach." Bohr havde brugt et simpelt og regelmæssigt mønster for brintatomets spektrum, som var fundet af Johann Balmer i 1885. Han gjorde også brug af ideen om kvanteideen, fundet af Max Planck i 1900. "
I 1913, Bohrs model var et kæmpe spring fremad, fordi den inkorporerede funktioner i den nyfødte kvantemekanik i beskrivelsen af atomer og molekyler. Det år, han udgav tre artikler om forfatningen af atomer og molekyler:Den første og mest berømte var afsat til hydrogenatomet, og de to andre beskrev nogle grundstoffer med flere elektroner, ved at bruge sin model som ramme. Den model, han foreslog for brintatomet, havde elektroner, der bevægede sig rundt om kernen, men kun på specielle spor med forskellige energiniveauer. Bohr antog, at der blev udsendt lys, da en elektron sprang fra et højere energispor til et lavere energispor - det var det, der fik brint til at lyse i et glasrør. Han fik brint rigtigt, men hans model var lidt glitchy.
"Modellen formåede ikke at forudsige den rigtige værdi af jordtilstandsenergierne for mange elektronatomer og molekylernes bindingsenergi-selv for de enkleste 2-elektron-systemer, såsom heliumatomet eller et brintmolekyle, "siger Anatoly Svidzinsky, en professor i Institute for Quantum Science and Engineering ved Texas A&M, i et e -mailinterview. "Så, allerede i 1913, det var klart, at Bohrs model ikke er helt korrekt. Selv for brintatomet, Bohrs model forudsiger forkert, at atomets grundtilstand besidder et nul -orbitalt vinkelmoment. "
Nobelprisen 1922
Hvilken, selvfølgelig, giver måske ikke meget mening for dig, hvis du ikke er en kvantefysiker. Imidlertid, Bohrs model blev hurtigt sporet til at modtage en nobelpris i fysik i 1922. Men selvom Bohr cementerede sit ry i fysikens verden, forskere forbedrede hans model:
"Bohrs model for brintatomet blev forbedret af Arnold Sommerfeld i 1916, "siger Herschbach." Han fandt elliptiske baner, der tegnede sig for spektralinjer i nærheden af dem, der var kommet fra cirkulære baner. Bohr-Sommerfeld-modellen for brintatomet er grundlæggende, men kvante og relativitet blev store aspekter. "
Mellem 1925 og 1928, Werner Heisenberg, Max Born, Wolfgang Pauli, Erwin Schrodinger og Paul Dirac udviklede disse aspekter langt ud over Bohrs atommodel, men hans er langt den mest anerkendte model af et atom. Atommodellerne kvantefysik har givet os mindre at ligne en sol omgivet af elektronplaneter og mere som moderne kunst. Det er sandsynligt, at vi stadig bruger Bohr -modellen, fordi det er en god introduktion til begrebet atom.
"I 1913, Bohrs model demonstrerede, at kvantisering er en rigtig vej at gå i beskrivelsen af mikroverdenen, "siger Svidzinsky." Således, Bohrs model viste forskere en retning til at søge og stimulerede videre udvikling af kvantemekanik. Hvis du kender stien, så vil du før eller siden finde den rigtige løsning på problemet. Man kan tænke på Bohrs model som et af retningsskiltene langs en vandresti ind i kvanteverdenen. "
Nu er det interessantNiels Bohrs far, Christian Bohr, blev nomineret til tre forskellige nobelpriser i medicinens fysiologi, selvom han aldrig vandt.
Sidste artikelBohr -modellen:hurtigt udskiftet, men aldrig glemt
Næste artikelPareidolia:Hvorfor ser vi ansigter i næsten alt
 Varme artikler
Varme artikler
-
 Forskellen mellem Røde og Hvide BlodcellerBlod består af tre dele: Røde blodlegemer, hvide blodlegemer og blodplader. Røde blodlegemer er ansvarlige for iltleveringen fra lungerne til vævet i kroppen. Hvide blodlegemer er en del af immunsyste
Forskellen mellem Røde og Hvide BlodcellerBlod består af tre dele: Røde blodlegemer, hvide blodlegemer og blodplader. Røde blodlegemer er ansvarlige for iltleveringen fra lungerne til vævet i kroppen. Hvide blodlegemer er en del af immunsyste -
 Hvor er grænsen mellem fandom og besættelse?Deltagere klædt i forskellige kostumer deltager i Wizard World Chicago Comic Con 2016. Bilgin S. Sasmaz/Anadolu Agency/Getty Images Da Arthur Conan Doyle skabte den fiktive detektiv Sherlock Holmes i
Hvor er grænsen mellem fandom og besættelse?Deltagere klædt i forskellige kostumer deltager i Wizard World Chicago Comic Con 2016. Bilgin S. Sasmaz/Anadolu Agency/Getty Images Da Arthur Conan Doyle skabte den fiktive detektiv Sherlock Holmes i -
 Generelle egenskaber ved ProtistaProtister er en unik gruppe af organismer, der omfatter et rige i klassificeringen af levende ting. De andre kongeriger er Eubacteria, Archaebacteria, Svampe, Planter og Dyr. Kongeriget Protista ind
Generelle egenskaber ved ProtistaProtister er en unik gruppe af organismer, der omfatter et rige i klassificeringen af levende ting. De andre kongeriger er Eubacteria, Archaebacteria, Svampe, Planter og Dyr. Kongeriget Protista ind -
 10 måder at narre dig selv til at være gladSheriffens stedfortrædere dukker op for at smide dig ud af dit afskærmede hjem? Du har brug for den bærbare lykkegenerator. Justin Sullivan/Getty Images Der er mange ulykkelige mennesker, der trasker
10 måder at narre dig selv til at være gladSheriffens stedfortrædere dukker op for at smide dig ud af dit afskærmede hjem? Du har brug for den bærbare lykkegenerator. Justin Sullivan/Getty Images Der er mange ulykkelige mennesker, der trasker


