Ny undersøgelse fremhæver første infektion af menneskelige celler under rumflyvning
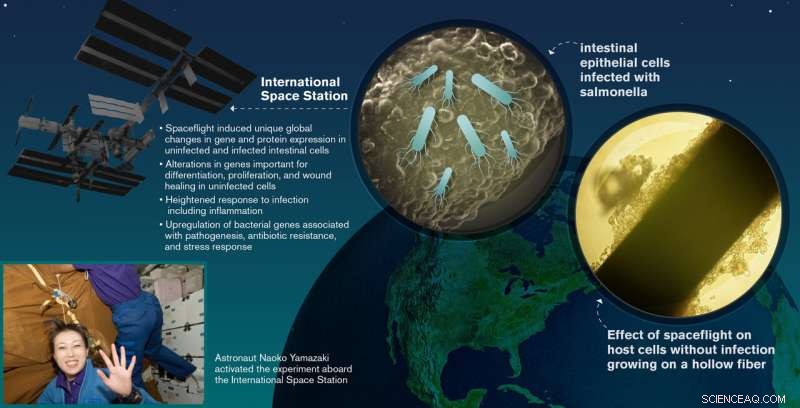
Infektion af humane tarmepitelceller med Salmonella Typhimurium under rumflyvning ombord på NASA Space Shuttle-mission STS-131. Kredit:Shireen Dooling for Biodesign Institute ved Arizona State University
Astronauter står over for mange udfordringer for deres helbred, på grund af de usædvanlige forhold ved rumflyvning. Blandt disse er en række infektiøse mikrober, der kan angribe deres undertrykte immunsystem.
Nu, i den første undersøgelse af sin art, Cheryl Nickerson, hovedforfatter Jennifer Barrila og deres kolleger beskriver infektionen af menneskelige celler med tarmpatogenet Salmonella Typhimurium under rumflyvning. De viser, hvordan mikrogravitationsmiljøet under rumflyvning ændrer den molekylære profil af menneskelige tarmceller, og hvordan disse ekspressionsmønstre ændres yderligere som reaktion på infektion. I en anden første, forskerne var også i stand til at påvise molekylære ændringer i det bakterielle patogen, mens de var inde i de inficerede værtsceller.
Resultaterne giver frisk indsigt i infektionsprocessen og kan føre til nye metoder til at bekæmpe invasive patogener under rumflyvning og under mindre eksotiske forhold her på jorden.
Resultaterne af deres indsats vises i det aktuelle nummer af tidsskriftet Nature Publishing Group npj Mikrotyngdekraft .
Missionskontrol
I undersøgelsen, humane tarmepitelceller blev dyrket ombord på rumfærgen mission STS-131, hvor en undergruppe af kulturerne enten var inficeret med Salmonella eller forblev som uinficerede kontroller.
Den nye forskning afslørede globale ændringer i RNA- og proteinekspression i humane celler og RNA-ekspression i bakterieceller sammenlignet med jordbaserede kontrolprøver og forstærker holdets tidligere resultater om, at rumflyvning kan øge potentialet for smitsomme sygdomme.
Nickerson og Barrila, forskere i Biodesign Center for Fundamental and Applied Microbiomics, sammen med deres kolleger, har brugt rumflyvning som et unikt eksperimentelt værktøj til at studere, hvordan ændringer i fysiske kræfter, som dem, der er forbundet med mikrogravitationsmiljøet, kan ændre responsen fra både værten og patogenet under infektion. Nickerson er også professor ved School of Life Sciences ved ASU.
I en tidligere serie af banebrydende rumflyvninger og jordbaserede rumflyvningsanaloge undersøgelser, Nickersons team demonstrerede, at rumflyvningsmiljøet kan intensivere de sygdomsfremkaldende egenskaber eller virulensen af patogene organismer som Salmonella på måder, der ikke blev observeret, da den samme organisme blev dyrket under konventionelle forhold i laboratoriet.
Undersøgelserne gav fingerpeg om de underliggende mekanismer bag den øgede virulens, og hvordan den kan tæmmes eller overlistes. Imidlertid, disse undersøgelser blev udført, da kun Salmonella blev dyrket i rumflyvning, og infektionerne blev udført, da bakterierne blev returneret til Jorden.
"Vi sætter pris på den mulighed, som NASA gav vores team til at studere hele infektionsprocessen i rumflyvning, som giver ny indsigt i mekanobiologien af infektionssygdomme, der kan bruges til at beskytte astronauters sundhed og mindske risikoen for infektionssygdomme, Nickerson siger om den nye undersøgelse. "Dette bliver stadig vigtigere, efterhånden som vi går over til længere menneskelige udforskningsmissioner, der er længere væk fra vores planet."
Undersøge en kendt modstander
Salmonella-stammer, der vides at inficere mennesker, fortsætter med at hærge samfundet, som de har gjort siden oldtiden, forårsager omkring 1,35 millioner fødevarebårne infektioner, 26, 500 indlæggelser, og 420 dødsfald i USA hvert år, ifølge Centers for Disease Control. Patogenet kommer ind i menneskekroppen gennem indtagelse af forurenet mad og vand, hvor det hæfter og trænger ind i tarmvæv. Infektionsprocessen er en dynamisk dans mellem vært og mikrobe, dens rytme dikteret af de biologiske og fysiske signaler, der findes i vævets miljø.
På trods af årtiers intensiv forskning, videnskabsmænd har stadig meget at lære om subtiliteterne ved patogen infektion af menneskelige celler. Invasive bakterier som Salmonella har udviklet sofistikerede modforanstaltninger til menneskets forsvar, lader dem blomstre under fjendtlige forhold i menneskets mave og tarm for snigende at undslippe immunsystemet, gør dem meget effektive sygdomsmidler.
Problemet er af særlig medicinsk bekymring for astronauter under rumflyvningsmissioner. Deres immunsystem og mave-tarmfunktion er ændret af rumfartens strabadser, mens virkningerne af lav tyngdekraft og andre variabler i rumflyvningsmiljøet kan intensivere de sygdomsfremkaldende egenskaber hos blaffermikrober, som Salmonella. Denne kombination af faktorer udgør enestående risici for rumrejsende, der arbejder hundredvis af kilometer over jorden – langt væk fra hospitaler og passende lægebehandling.
Efterhånden som teknologien udvikler sig, det forventes, at rumrejser vil blive hyppigere - til udforskning af rummet, biovidenskabelig forskning, og endda som en fritidsaktivitet (for dem, der har råd). Yderligere, udvidede missioner med menneskelige besætninger er i horisonten for NASA og måske rumfartsvirksomheder som SpaceX, herunder rejser til Månen og Mars. En manglende evne til at holde bakterieinfektioner i skak kan få alvorlige konsekvenser.
Hide and Seq
I den aktuelle undersøgelse, humane tarmepitelceller, det primære mål for invasive Salmonella-bakterier, blev inficeret med Salmonella under rumflyvning. Forskerne var ivrige efter at undersøge, hvordan rumflyvningsindstillingen påvirkede transskriptionen af menneskeligt og bakterielt DNA til RNA, såvel som ekspressionen af den resulterende suite af humane proteiner produceret ud fra RNA-koden, produkter af en proces kendt som oversættelse.
Forskningen involverede en nøje undersøgelse af transkriptionelle profiler af både den patogene Salmonella og de menneskelige celler, de angriber, såvel som proteinekspressionsprofilerne for de menneskelige celler for at måle virkningerne af rumflyvningsmiljøet på vært-patogen-dynamikken.
For at opnå dette, forskere brugte en revolutionerende metode kendt som dual RNA-Seq, som anvendte dyb sekventeringsteknologi for at muliggøre deres evaluering af værts- og patogenadfærd under mikrogravitation under infektionsprocessen og tillod en sammenligning med holdets tidligere eksperimenter udført ombord på rumfærgen.
Værts- og patogendata indvundet fra rumflyvningseksperimenter blev sammenlignet med dem, der blev opnået, når celler blev dyrket på jorden under identiske hardware- og kulturbetingelser (f. medier, temperatur).
Jord og himmel
Tidligere undersøgelser af Nickerson og hendes kolleger har vist, at jordbaserede rumflyvningsanalogkulturer af Salmonella udviste globale ændringer i deres transkriptionelle og proteomiske (protein) ekspression, øget virulens, og forbedret stressmodstand - resultater svarende til dem, der blev frembragt under deres eksperimenter på STS-115 og STS-123 rumfærgemissioner.
Imidlertid, disse tidligere rumflyvningsundersøgelser blev udført, da kun Salmonella blev dyrket i rumflyvning, og infektionerne blev udført, da bakterierne blev returneret til Jorden.
I modsætning, den nye undersøgelse udforsker for første gang, en co-kultur af menneskelige celler og patogen under rumflyvning, giver et unikt vindue ind i infektionsprocessen. Eksperimentet, kaldet STL-IMMUNE, var en del af Space Tissue Loss nyttelasten båret ombord på STS-131, en af de sidste fire missioner af rumfærgen før dens pensionering.
De humane tarmepitelceller blev sendt ud i rummet (eller holdt i et laboratorium på Kennedy Space Center for jordkontrol) i tredimensionelle (3-D) vævskultursystemer kaldet hulfiberbioreaktorer. Hulfiberbioreaktorerne indeholdt hver hundrede af små, porøse halmlignende fibre belagt med kollagen, hvorpå tarmcellerne fæstede sig og voksede. Disse bioreaktorer blev opretholdt i cellekulturmodulet, et automatiseret hardwaresystem, der pumpede varmt, iltede cellekulturmedier gennem de små fibre for at holde cellerne sunde og i vækst, indtil de var klar til infektion med Salmonella.
En gang i kredsløb, astronauter ombord på STS-131 aktiverede hardwaren. Elleve dage senere, S. Typhimurium-celler blev automatisk injiceret i en delmængde af hulfiberbioreaktorerne, hvor de stødte på deres mål - et lag af menneskelige epitelceller.
RNA-Seq og proteomiske profiler viste signifikante forskelle mellem uinficerede tarmepitelkulturer i rummet kontra dem på jorden. Disse ændringer involverede store proteiner, der er vigtige for cellestrukturen, såvel som gener, der er vigtige for at opretholde den intestinale epitelbarriere, celledifferentiering, spredning, sårheling og kræft. Baseret på deres profiler, uinficerede celler udsat for rumflyvning kan vise en reduceret kapacitet til spredning, i forhold til jordkontrolkulturer.
Infektioner langt hjemmefra
Humane tarmepitelceller fungerer som kritiske vagtposter for medfødt immunfunktion. Resultaterne af eksperimentet viste, at rumflyvning kan forårsage globale ændringer af transkriptomet og proteomet af humane epitelceller, både inficerede og uinficerede.
Under rumflyvning, 27 RNA-transkripter blev unikt ændret i tarmceller som reaktion på infektion, endnu en gang etablere den unikke indflydelse fra rumfartsmiljøet på vært-patogen-interaktionen. Forskerne observerede også 35 transkripter, som almindeligvis blev ændret i både rumbaserede og jordbaserede celler, med 28 gener reguleret i samme retning. Disse resultater bekræftede, at i det mindste en delmængde af de infektionsbiosignaturer, der vides at forekomme på Jorden, også forekommer under rumflyvning. Sammenlignet med uinficerede kontroller, inficerede celler i begge miljøer viste genregulering forbundet med inflammation, en signatureffekt af Salmonella-infektion.
Bakterielle transkripter blev også samtidig påvist i de inficerede værtsceller og indikerede opregulering af gener forbundet med patogenese, herunder antibiotikaresistens og stressreaktioner.
Resultaterne hjælper med at bane vejen for en forbedret indsats for at beskytte astronauternes sundhed, måske gennem brug af kosttilskud eller probiotiske mikrober. Igangværende undersøgelser af denne art, skal udføres ombord på den internationale rumstation og andre rumhabitater, skal yderligere belyse de mange mysterier forbundet med patogen infektion og den brede vifte af menneskelige sygdomme, som de er ansvarlige for.
"Før vi begyndte denne undersøgelse, vi havde omfattende data, der viste, at rumflyvning fuldstændigt omprogrammerede Salmonella på alle niveauer for at blive et bedre patogen, " siger Barrila. "Separat, vi vidste, at rumflyvning også påvirkede adskillige vigtige strukturelle og funktionelle træk ved menneskelige celler, som Salmonella normalt udnytter under infektioner på jorden. Imidlertid, der var ingen data, der viste, hvad der ville ske, når begge celletyper mødtes i mikrogravitationsmiljøet under infektion. Vores undersøgelse indikerer, at der er nogle ret store ændringer i det molekylære landskab i tarmepitel som reaktion på rumflyvning, og dette globale landskab ser ud til at blive yderligere ændret under infektion med Salmonella."
 Varme artikler
Varme artikler
-
 Astronomer opdager brintkorona fra Jupiters måne EuropaJupiters iskolde måne Europa. Kredit:NASA/JPL-Caltech/SETI Institute (Phys.org) - Ved hjælp af Hubble -rumteleskopet (HST), astronomer har opdaget en atomær brintkorona omkring Jupiters iskolde må
Astronomer opdager brintkorona fra Jupiters måne EuropaJupiters iskolde måne Europa. Kredit:NASA/JPL-Caltech/SETI Institute (Phys.org) - Ved hjælp af Hubble -rumteleskopet (HST), astronomer har opdaget en atomær brintkorona omkring Jupiters iskolde må -
 XMM-Newton afslører kæmpe flare fra en lille stjerneKunstnerens indtryk af en L dværgstjerne, en stjerne med så lille masse, at den kun er lige over grænsen til faktisk at være en stjerne, fanget i færd med at udsende et enormt superudbrud af røntgenst
XMM-Newton afslører kæmpe flare fra en lille stjerneKunstnerens indtryk af en L dværgstjerne, en stjerne med så lille masse, at den kun er lige over grænsen til faktisk at være en stjerne, fanget i færd med at udsende et enormt superudbrud af røntgenst -
 Hvor mange planeter er der i galaksen?Kunstnerens indtryk af Mælkevejsgalaksen. Baseret på nuværende estimater og exoplanetdata, det menes, at der kan være titusinder af milliarder af beboelige planeter derude. Kredit:NASA På en klar
Hvor mange planeter er der i galaksen?Kunstnerens indtryk af Mælkevejsgalaksen. Baseret på nuværende estimater og exoplanetdata, det menes, at der kan være titusinder af milliarder af beboelige planeter derude. Kredit:NASA På en klar -
 Hubble fanger kosmisk fyrværkeri i ultravioletKredit:Hubble Space Telescope Hubble tilbyder en speciel udsigt over dobbeltstjernesystemet Eta Carinaes ekspanderende gasser, der lyser i rødt, hvid, og blå. Dette er det højeste opløsning billed
Hubble fanger kosmisk fyrværkeri i ultravioletKredit:Hubble Space Telescope Hubble tilbyder en speciel udsigt over dobbeltstjernesystemet Eta Carinaes ekspanderende gasser, der lyser i rødt, hvid, og blå. Dette er det højeste opløsning billed
- Opdager og krymper børsterne af polyelektrolytbørster
- Videnskabsmand begynder at udvikle instrument til at finde udenjordiske bakterier
- Juicing teknik kan påvirke sundheden af friskpresset juice
- Hvordan man opbygger en Otter Shoebox Habitat
- Omkostningerne til COVID-19-svindel vil sandsynligvis stige betydeligt, rapporten afsluttes
- Det oversvømmede Venedig forberedte sig på flere oversvømmelser, stærke vinde


