Cellesignaler, der udløser sårheling, er overraskende komplekse
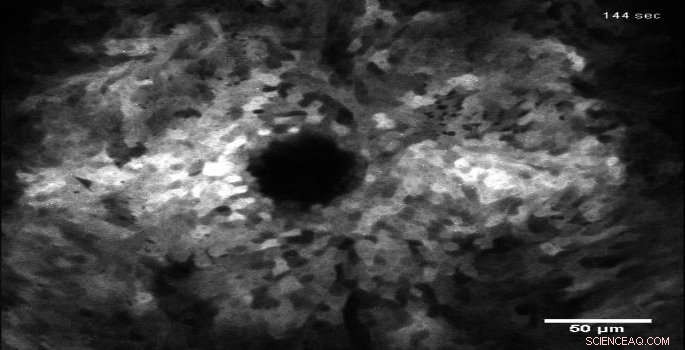
Fluorescens efter et sår i levende epitelvæv viser spredningen af calciumsignaler, der udløser heling. Kredit:Hutson Laboratory, Vanderbilt University
I en skarp og spids verden, sårheling er en kritisk og fantastisk proces. På trods af en enorm mængde videnskabelige undersøgelser, mange fremragende mysterier omgiver stadig den måde, hvorpå celler i levende væv reagerer på og reparerer fysiske skader.
Et fremtrædende mysterium er præcis, hvordan sårheling udløses:En bedre forståelse af denne proces er afgørende for at udvikle nye og forbedrede metoder til behandling af sår af alle typer.
Ved hjælp af en ultrahurtig, ultrapræcis ultraviolet laser, et team af fysikere og biologer ved Vanderbilt University har taget et vigtigt skridt i retning af at forstå arten af disse triggersignaler. Deres nye indsigt er beskrevet i et papir med titlen "Flere mekanismer driver calciumsignaldynamik omkring laserinducerede epitelsår" udgivet 3. oktober af Biofysisk Journal .
Tidligere forskning havde fastslået, at calciumioner spiller en central rolle i sårrespons. Det er ikke overraskende, fordi calciumsignalering har indflydelse på næsten alle aspekter af cellelivet. Så, forskerne-ledet af professor i fysik og biologiske videnskaber Shane Hutson og lektor i celle- og udviklingsbiologi Andrea Page-McCaw-målrettede celler på bagsiden af frugtflue-pupper, der udtrykte et protein, der fluorescerer i nærvær af calciumioner. Dette gjorde det muligt for dem at spore ændringer i calciumionkoncentrationer i cellerne omkring sår i levende væv (i modsætning til cellekulturer, der blev brugt i mange tidligere sårresponsstudier) og gøre det med en hidtil uset, millisekund præcision.
Holdet skabte mikroskopiske sår i puppernes epitelag ved hjælp af en laser, der kan fokuseres ned til et punkt, der er lille nok til at slå mikroskopiske huller i individuelle celler (mindre end en milliondel af en meter). Laserens præcision tillod dem at skabe gentagelige og kontrollerbare sår. De fandt ud af, at selv den korteste af pulser i området nanosekund til femtosekund frembragte en mikroskopisk eksplosion kaldet en kavitationsboble, der var kraftig nok til at beskadige nærliggende celler.
"Som resultat, den skade, laserpulserne frembringer, ligner ganske meget et punkteringssår omgivet af et knust sår - stump krafttrauma i retsmedicin - så vores observationer bør gælde for de fleste almindelige sår, "sagde første forfatter Erica Shannon, en doktorand i udviklingsbiologi.
Forskerne testede to fremherskende hypoteser for sårresponsudløseren. Den ene er, at beskadigede og døende celler frigiver proteiner i den ekstracellulære væske, som omgivende celler fornemmer, får dem til at øge deres interne calciumniveauer. Dette øgede calciumkoncentrationen, på tur, udløser deres transformation fra en statisk til en mobil form, så de kan begynde at forsegle såret. Den anden hypotese foreslår, at triggersignalet spredes fra celle til celle gennem gap junctions, specialiserede intercellulære forbindelser, der direkte forbinder to celler på punkter, hvor de berører. Disse er mikroskopiske porte, der tillader naboceller at udveksle ioner, molekyler og elektriske impulser hurtigt og direkte.
"Det, der er ekstremt spændende, er, at vi fandt beviser for, at celler bruger begge mekanismer, "sagde Shannon." Det viser sig, at celler har en række forskellige måder at signalere skade på. Dette kan give dem mulighed for at skelne mellem forskellige slags sår. "Eksperimenterne afslørede, at dannelsen af et sår genererer en kompleks række calciumsignaler i det omgivende væv:
- Først kommer en hurtig tilstrømning af calcium ind i cellerne umiddelbart omkring såret. Dette matcher kavitationsboblens fodaftryk. Calciumniveauer i den ekstracellulære væske er meget højere end de er i cellerne. På grund af den hurtighed, hvormed den sker (mindre end en tiendedel af et sekund) hævder forskerne, at denne tilstrømning er forårsaget af mikrotår i cellemembraner, der er flået op af mikroeksplosionens kraft;
- Næste, en kortvarig, kortsigtet bølge spredes gennem raske naboceller. Jo større såret, jo hurtigere bølgen spreder sig. Hastigheden, hvormed bølgen bevæger sig, tyder på, at den bevæger sig gennem gap -junctions og består enten af calciumioner eller et andet lille signalmolekyle.
- Cirka 45 sekunder efter såringen vises en anden bølge. Denne bølge bevæger sig meget langsommere end den første bølge, men spreder sig betydeligt længere. Forskerne tolker dette til at betyde, at det spredes af større molekyler, sandsynligvis særlige signalproteiner, der diffunderer langsommere end ioner. Imidlertid, de advarer om, at yderligere eksperimenter er nødvendige for at bekræfte denne formodning. Den anden bølge opstår kun, når celler dræbes, ikke når de bare er beskadiget, tyder på, at det er afhængigt af skadens omfang.
- De to første bølger spredte sig relativt symmetrisk gennem vævet. Efter den anden bølge, imidlertid, området med høj calciumkoncentration begynder at sende "blusser" - retningstrømme af calciumoptagelse, der spredes længere ind i det omgivende væv. Hver bluss varer i snesevis af sekunder, og nye blusser starter fortsat i mere end 30 minutter efter skaden.
"Når vi forstår disse udløsermekanismer, det skal være muligt at finde måder at stimulere sårhelingsprocessen hos mennesker med tilstande, som diabetes, der bremser processen eller endda for at fremskynde normal sårheling, "sagde Hutson.
Sidste artikelDesigner biosensor kan påvise antibiotikaproduktion af mikrober
Næste artikelFlagermus og insekter kæmper i troperne
 Varme artikler
Varme artikler
-
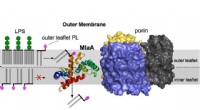 Betydningen af asymmetri i bakterierBilledet viser rensning af den ydre membran med MlaA. MlaA, som i cellen er bundet til et andet ydre membranprotein kaldet porin, fjerner ydre folderfosfolipider og fungerer som en membranstøvsuger, d
Betydningen af asymmetri i bakterierBilledet viser rensning af den ydre membran med MlaA. MlaA, som i cellen er bundet til et andet ydre membranprotein kaldet porin, fjerner ydre folderfosfolipider og fungerer som en membranstøvsuger, d -
 Hvorfor dræber vi?Er drab en del af den menneskelige natur? © iStockphoto.com/Thinkstock William Shakespeares Hamlet proklamerede, Hvilket stykke arbejde er en mand, hvor ædel i fornuften, hvor uendelig i fakulteter,
Hvorfor dræber vi?Er drab en del af den menneskelige natur? © iStockphoto.com/Thinkstock William Shakespeares Hamlet proklamerede, Hvilket stykke arbejde er en mand, hvor ædel i fornuften, hvor uendelig i fakulteter, -
 Taq-polymerasens rolle i PCRAt fremstille kopier af DNA kræver enzymer kaldet DNA-polymeraser. Disse enzymer bevarer et genom under replikation. Før 1960erne havde forskerne ikke en varmestabil DNA-polymerase til brug for at fre
Taq-polymerasens rolle i PCRAt fremstille kopier af DNA kræver enzymer kaldet DNA-polymeraser. Disse enzymer bevarer et genom under replikation. Før 1960erne havde forskerne ikke en varmestabil DNA-polymerase til brug for at fre -
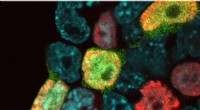 (Gen)erhvervelse af potentialet til at blive altFluorescensbillede af museembryonale stamceller (kerner i blåt) inklusive 2 cellelignende celler (grønne) og den nye population af overgangsceller (rød). Kredit:Helmholtz Zentrum München/IES En ny
(Gen)erhvervelse af potentialet til at blive altFluorescensbillede af museembryonale stamceller (kerner i blåt) inklusive 2 cellelignende celler (grønne) og den nye population af overgangsceller (rød). Kredit:Helmholtz Zentrum München/IES En ny
- Forbedret matematisk model hjælper med at forklare forskellige lotusbladtyper
- Hvad er et pentagonalt prisme?
- Forskere finder konformationsforstyrrelser, der indstiller ladningsbærermobilitet i 2-D perovskitte…
- Fjernelse af CO2 fra luften, der er nødvendig for at sikre børns fremtid
- Ny dual-propeller drone kan flyve dobbelt så lang
- Folk stoler på beslutninger truffet af grupper, men informationsmarkederne er mere nøjagtige


