I kampen mod viral infektion, stavning tæller
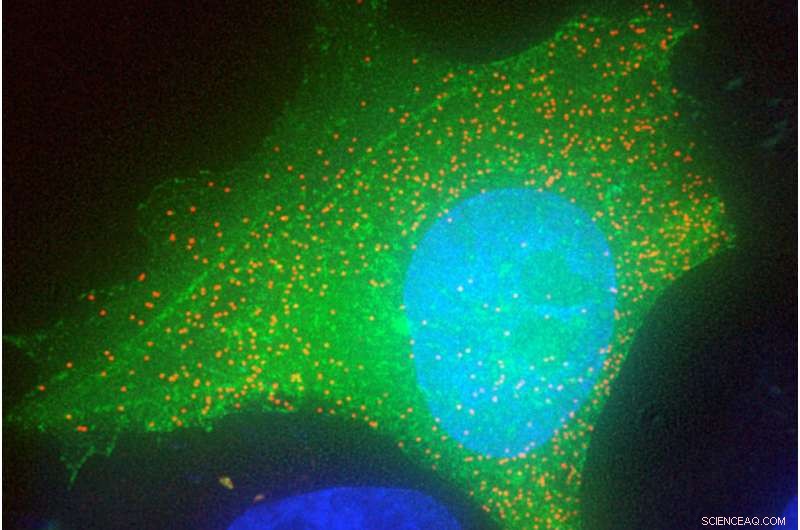
En menneskelig celle (grøn) inficeret med HIV (rød). Kredit:Laboratory of Retrovirology ved Rockefeller University/Nature
I millioner af år, mennesker og vira har engageret sig i et konstant tovtrækkeri:efterhånden som vores celler udvikler nye måder at forsvare os mod vores virale fjender, disse patogener får igen nye egenskaber for at omgå disse forsvar.
Nu, Forskere har fundet ud af, at en vigtig lighed mellem vores gener og generne fra mange vira - en måde at stave den genetiske kode på - sandsynligvis har givet vira mulighed for at undvige vores cellulære forsvar. Paul Bieniasz, en Rockefeller professor og Howard Hughes Medical Institute Investigator, der ledede arbejdet, siger, at det begyndte som et forsøg på at forstå, hvordan det virale genom påvirker HIV's smitsomme styrke, virus, der forårsager AIDS.
Rapporteret i Natur , hans laboratoriums seneste resultater giver indsigt i vores cellulære forsvarsmekanismer, og foreslå nye veje til vaccineudvikling.
Overraskende nok, det hele kommer ned til et spørgsmål om stavning.
Der er en håndfuld ord i det engelske sprog, hvis stavemåder kan variere uden at ændre deres betydning:farve og farve, for eksempel, eller rejsende og rejsende. Vores genom er ikke anderledes:der er mange forskellige måder at stave den molekylære kode, der udgør vores gener, uden at ændre de proteiner, disse gener producerer. Men Bieniasz og hans kolleger fandt ud af, at for HIV og andre vira, visse stavemåder, eller specifikke varianter i den genetiske kode, er kritiske for viral replikation og infektion.
To tilstødende bogstaver, tabt i evolutionen
Alle genomer er strenge af små molekyler, kendt som baser, der er repræsenteret med bogstaver som C, G, og A. String disse bogstaver ud i en bestemt rækkefølge, og de staver et ord, eller gen, der producerer et bestemt protein. I forsøget på at identificere dele af HIV-genomet, der muliggør infektion, forskerne genererede mutante versioner af virussen. Men i stedet for at ændre proteinerne, der er stavet gennem dets genetiske bogstaver, de indførte alternative stavemåder for generne, holde proteinerne uændrede.
Forskerholdet fandt ud af, at nogle af disse virale mutanter ikke var i stand til at vokse og replikere. "Intuitivt, dette er uventet, fordi alle proteinerne - virussens arbejdsheste - er nøjagtig ens, " forklarer Bieniasz.
De defekte mutante vira havde én ting til fælles, dog:de indeholdt alle flere forekomster af en bestemt tobogstavssekvens:CG.
Den sekvens på to bogstaver virker ikke som en voldsomt usandsynlig hændelse. Der er kun fire bogstaver i den genetiske kode, så sandsynligheden for at finde to bogstaver sammen er høj - 1 ud af 16, for at være præcis. Og stadigvæk, ved et mærkeligt sammenfald af evolution, CG-sekvensen er sjælden i humant DNA. Når den placeres side om side, bogstavet C kan modificeres i en kemisk reaktion, der i sidste ende fører til, at det erstattes med et andet bogstav.
"På grund af dette evolutionære tab, det menneskelige genom har nu omkring 80 procent færre CG-sekvenser, end vi tilfældigt ville forvente, " forklarede kandidatstuderende Matthew A. Takata, hovedforfatter af det nye papir.
Et bull's eye for immunsystemet
Vi mennesker er ikke alene om at mangle CG-sekvenser:normal HIV og mange andre vira mangler også dem, men af forskellige årsager. "Mange virale genomer kan ikke gennemgå den samme kemiske modifikationsproces, som hvirveldyrgenomer som vores egen har oplevet, " sagde Bieniasz. "Dette fik os til at spørge:Hvordan og hvorfor mistede HIV og andre vira deres CG-sekvenser?"
Forskerne antog, at et cellulært overvågningssystem kunne eksistere til at identificere og ødelægge CG-sekvenser, derved forhindre virusinfektion. Bieniasz, Takata, og forskerholdet udnyttede ny genredigeringsteknologi til at søge efter proteiner, der kunne tjene som en sådan forsvarsmekanisme. De fandt ud af, at i menneskelige celler, et antiviralt protein kaldet "ZAP" (Zink-finger Antiviral Protein) kan genkende molekyler, der har mange CG-sekvenser. ZAP binder til sekvenserne, identificere dem som mærket af en fremmed angriber. Disse virale genomer ødelægges derefter.
Resultaterne giver indsigt i, hvad der fik HIV og andre vira til at miste deres CG-sekvenser over tid. Disse vira har sandsynligvis tilpasset sig pattedyrs forsvarsmekanismer, udvikler sig til at fjerne CG-sekvenser og undgå overvågning af ZAP.
Selvom mange dyrevira som HIV indeholder få CG-sekvenser, og derfor ikke blive ødelagt af ZAP, forskerne spekulerer i, at proteinet stadig tjener til at beskytte os mod andre patogener. "Dens aktivitet gør det muligt for celler at genkende fremmede angribere som 'ikke-selv', '" Bieniasz siger, "og kan yde forsvar mod vira fra andre arter, såsom bidende insekter, hvis genomer stadig har et højt antal CG-sekvenser."
Praktisk talt, opdagelsen kan være nyttig til at udvikle de svækkede, eller dæmpet, vira, der ofte bruges til fremstilling af vacciner. Ved gensplejsning af en virus til at indeholde et øget antal CG-sekvenser, forskere kunne potentielt komme med en version, der ville få folks immunsystem til at producere immunitet mod patogenet uden faktisk at gøre dem syge.
"Omkodning af en virus med mange yderligere CG-sekvenser, " siger Takata, "formentlig vil være en effektiv, justerbar og stort set irreversibel måde at dæmpe den på, gør vaccineudvikling hurtigere og sikrere."
 Varme artikler
Varme artikler
-
 Videnskaben går tættere på at forklare den vredes fuldeAlkohol ændrer funktionen af præfrontal cortex, den del af vores hjerner, der er ansvarlig for at regulere social adfærd og aggression. Matt Cardy/Getty Images Du ved, at du har den ven-lad os kald
Videnskaben går tættere på at forklare den vredes fuldeAlkohol ændrer funktionen af præfrontal cortex, den del af vores hjerner, der er ansvarlig for at regulere social adfærd og aggression. Matt Cardy/Getty Images Du ved, at du har den ven-lad os kald -
 Hvorfor er kvælstof vigtig for levende ting?Kvælstof er vigtigt for alle levende ting, fordi det er en væsentlig del af aminosyrer, som er byggestenene til proteiner og af nukleinsyrer, såsom DNA, som overfører genetisk information til efterføl
Hvorfor er kvælstof vigtig for levende ting?Kvælstof er vigtigt for alle levende ting, fordi det er en væsentlig del af aminosyrer, som er byggestenene til proteiner og af nukleinsyrer, såsom DNA, som overfører genetisk information til efterføl -
 Hvordan Snapdragons holder deres farve:Skiltetrick afslører evolutionær mekanismeSnapdragons (Antirrhinum majus) i den nysgerrige hybridzone i Pyraneerne. Kredit:Professor Enrico Coen En undersøgelse af farvemønstre blandt vilde blomster i en bjergdal har givet et fingerpeg om
Hvordan Snapdragons holder deres farve:Skiltetrick afslører evolutionær mekanismeSnapdragons (Antirrhinum majus) i den nysgerrige hybridzone i Pyraneerne. Kredit:Professor Enrico Coen En undersøgelse af farvemønstre blandt vilde blomster i en bjergdal har givet et fingerpeg om -
 Ved hjælp af moderne genomik til at gøre alligatorskæl til fuglelignende fjerNormale embryonale skalaer (venstre) sammenlignet med det aflange fjerlignende vedhæng efter genetisk manipulation (højre). Kredit:USC Ved første øjekast, de fleste mennesker ville ikke tro, at al
Ved hjælp af moderne genomik til at gøre alligatorskæl til fuglelignende fjerNormale embryonale skalaer (venstre) sammenlignet med det aflange fjerlignende vedhæng efter genetisk manipulation (højre). Kredit:USC Ved første øjekast, de fleste mennesker ville ikke tro, at al
- Geobiolog Roger indkalder til at finde organisk stof på Mars
- Teknik kan gøre det lettere at bruge mRNA til at behandle sygdom eller levere vacciner
- Trump retter sig mod Amazon igen i nye tweets
- 5 mindeværdige NASA -missionvideoer
- Hvad er hydrenes værdi?
- Undersøgelse undersøger radioegenskaber af supernova-rest G107.0+9.0


