Forskere udvikler nyt værktøj til målrettet cellekontrol

Kredit:Pixabay/CC0 Public Domain
Takket være nye RNA-vacciner har vi mennesker været i stand til at beskytte os selv utroligt hurtigt mod nye vira som SARS-CoV-2, den virus, der forårsager COVID-19. Disse vacciner indsætter et stykke kortvarigt genetisk materiale i kroppens celler, som derefter læser dens kode og udskiller et specifikt protein - i dette tilfælde afslørende "spidser", der fastgør ydersiden af coronavirussen - der sætter immunsystemet i stand til at bekæmpe fremtidige angribere .
Teknikken er effektiv og lover alle slags terapier, siger Eerik Kaseniit, ph.d. studerende i bioingeniør ved Stanford. I øjeblikket kan denne slags RNA-terapier dog ikke fokusere på specifikke celler. Når de først er injiceret i kroppen, laver de vilkårligt det kodede protein i hver celle, de kommer ind i. Hvis du vil bruge dem til kun at behandle én slags celler – som dem inde i en kræftsvulst – skal du have noget mere præcist.
Kaseniit og hans rådgiver, assisterende professor i kemiteknik Xiaojing Gao, har muligvis fundet en måde at gøre dette muligt på. De har skabt et nyt værktøj kaldet en RNA "sensor" - en streng af laboratoriefremstillet RNA, der kun afslører dets indhold, når det kommer ind i bestemte væv i kroppen. Metoden er så nøjagtig, at den kan være hjemme i både celletyper og celletilstande og kun aktiveres, når dens målcelle skaber et bestemt RNA, siger Gao. Parret offentliggjorde deres resultater 5. oktober i tidsskriftet Nature Biotechnology .
"For første gang kan du direkte få kun de interesserede celler til at producere et protein under meget specifikke omstændigheder," tilføjer Gao. "Den slags nøjagtighed var bare ikke tidligere mulig." Det producerede protein kunne være et antigen - et fremmed stof, der fremkalder en immunreaktion - som i tilfælde af vacciner, et enzym, der genopretter funktionen til en ødelagt celle, et fluorescerende protein, der kan bruges til at spore specifikke celler i en forskningsundersøgelse, eller et protein, der udløser celledød for at fjerne patogene eller på anden måde uønskede celler, blandt andre muligheder.
Udnyttelse af immunsystemet
Parrets nye system, kaldet RADAR, består i det væsentlige af to sektioner:en "sensor"-region, der låser sig på specifikke RNA'er i kroppen, og en "nyttelast"-region, som en celle vil læse og omdanne til et protein. De to sektioner er adskilt af et stopkodon, en RNA-sekvensdel, der gør en del af RADARs genetiske kode utilgængelig.
Hvis RADARs sensorregion med succes låser sig fast på sit mål, vil stopkodonet forsvinde, hvilket gør den resterende region - dens "nyttelast" - pludselig læsbar. I teorien kunne denne nyttelast indeholde instruktioner til at lave et hvilket som helst protein, i enhver celletype, til enhver tid.
Processen finder sted takket være et eksisterende sæt enzymer kaldet ADAR (Adenosine Deaminases Acting on RNA) - et biprodukt af et igangværende viralt våbenkapløb, der har raset inde i den menneskelige krop i årtusinder, siger Gao.
Nogle vira, såsom SARS-CoV-2, influenza og norovirus, er blot en proteinskal med RNA indlejret indeni. I processen med at replikere skaber disse vira meget lange strækninger af dobbeltstrenget RNA. Da vira kan have ødelæggende virkninger på kroppen, har vores immunsystem gradvist lært at se de dobbeltstrengede RNA'er som en trussel og vil hurtigt lukke dem ned.
"Det er en slags faresignal - hvis en celle ser dobbeltstrenget RNA, bliver den straks flippet over det," siger Kaseniit.
I en mærkelig drejning af evolutionen laver vores egne kroppe også dobbeltstrenget RNA. Efterhånden som vira har angrebet os gennem årtusinder, gravet ind i vores celler og leget med vores genetiske maskineri, er nogle af deres gener blevet absorberet og inkorporeret i vores DNA. (Det er ikke et lykketræf:Det er sket så mange gange tidligere, at det menneskelige genom i dag er næsten 8 % virus.)
For at løse dette problem udviklede ADAR sig som en slags "test"-system - en måde for kroppen at fortælle, om et stykke dobbeltstrenget RNA er ven eller fjende. Hvis den finder en, der er skabt af vores eget genom, redigerer ADAR det lidt for at få det til at virke mindre truende, hvilket får huller eller huller til at åbne sig mellem de to tråde, som at fjerne et par sting i midten af en stofsøm. Immunsystemet, som har større fisk at stege, ignorerer prompte dette ujævnt udseende RNA og fortsætter med at bekæmpe den virkelige fjende.
RADAR udnytter denne mekanisme. Når dets "sensor"-modul låses på et specifikt målmolekyle (et andet stykke RNA), ser ADAR det resulterende dobbeltstrengede par som en venlig, harmløs variant og redigerer det trofast, så immunsystemet ignorerer det. I processen sletter den det lille molekylære "stop"-tegn, som forskerne indbyggede i midten af RNA-strengen. Når den er fjernet, er nyttelastsektionen af RADAR synlig for cellen, og koden den indeholder omdannes til et protein.
Potentiale for nye programmerbare terapier
Lige nu tester Kaseniit, Gao og deres samarbejdspartnere stadig RADAR i en række forskellige indstillinger, men resultaterne ser lovende ud. Sammen med medforfatterne lektor i kemiteknik Elizabeth Sattely og postdocs Diego Wengier og Will Cody har de endda prøvet det i planter, som ikke naturligt har ADAR-systemer - men efter at have tilføjet ADAR-enzymer til blandingen, var de i stand til at få samme resultater. I fremtiden, siger de, kan fleksibiliteten og præcisionen af RADAR tilbyde et værdifuldt værktøj inden for både forskning og medicin, hvilket giver videnskabsmænd mulighed for at komme ind på specifikke celler i laboratoriet eller levere terapier i kroppen.
"Det er håbet og drømmen om RNA som platform, for du kan bare kode det protein, du vil, ind på et stykke RNA, og celler vil lave det. Nu kan vi med disse kontrolelementer specificere, hvilken målcelle det skal aktiveres i. Det er meget kraftfuldt," siger Kaseniit. + Udforsk yderligere
Nyt RNA-baseret værktøj kan belyse hjernekredsløb, redigere specifikke celler
 Varme artikler
Varme artikler
-
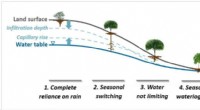 Dybe rødder i planter drevet af jordhydrologiTræ- og planteroddybder varierer, afhængig af klimaet, jord- og vandforhold, herunder regnvandsinfiltration og grundvandsstand. Kredit:Ying Fan Reinfelder/Rutgers University-New Brunswick Søger ef
Dybe rødder i planter drevet af jordhydrologiTræ- og planteroddybder varierer, afhængig af klimaet, jord- og vandforhold, herunder regnvandsinfiltration og grundvandsstand. Kredit:Ying Fan Reinfelder/Rutgers University-New Brunswick Søger ef -
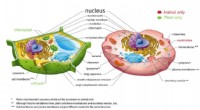 Her er hvordan plante- og dyreceller er forskelligeAlle levende ting, plante og dyr, består af slående lignende mikroskopiske byggesten kaldet celler, de grundlæggende strukturelle og funktionelle enheder i livet. jack0m/Getty images/HowStuffWorks Ud
Her er hvordan plante- og dyreceller er forskelligeAlle levende ting, plante og dyr, består af slående lignende mikroskopiske byggesten kaldet celler, de grundlæggende strukturelle og funktionelle enheder i livet. jack0m/Getty images/HowStuffWorks Ud -
 Saguaro -kaktus er et ikonisk symbol på det amerikanske sydvestSaguaro kaktus ( Carnegiea gigantea ) er den højeste nordamerikanske kaktus og den mest ikoniske i udseende. Frauke Feind/Pixabay Her er en lille kunstopgave:Tag et stykke papir og tegn en kaktus.
Saguaro -kaktus er et ikonisk symbol på det amerikanske sydvestSaguaro kaktus ( Carnegiea gigantea ) er den højeste nordamerikanske kaktus og den mest ikoniske i udseende. Frauke Feind/Pixabay Her er en lille kunstopgave:Tag et stykke papir og tegn en kaktus. -
 Hård debat bruser til live over aflysning af grizzlybjørnejagtGrizzly-trofæjagt er kernen i en voldsom debat i Nordamerika. Kredit:Shutterstock Der er ingen mangel på kontrovers omkring British Columbia-regeringens beslutning om at stoppe jagten på grizzlybj
Hård debat bruser til live over aflysning af grizzlybjørnejagtGrizzly-trofæjagt er kernen i en voldsom debat i Nordamerika. Kredit:Shutterstock Der er ingen mangel på kontrovers omkring British Columbia-regeringens beslutning om at stoppe jagten på grizzlybj
- Nyt kortlægningsværktøj til at understøtte søgningen efter naturbaserede kulstofkreditter af hø…
- Brug af efternavn for mænd mere end kvinder kan være tegn på utilsigtet skævhed
- Kemikalier, der bruges i varmepakker
- Ny algoritme kan hjælpe maskiner med at undgå skader eller funktionsfejl fra resonansfrekvenser
- Måder at minimere skader på hjemmet, før branden opstår
- Billede:Australias sydvestlige hjørne


