En genovervejelse af sygdomme i lyset af faseadskillelse og faseovergang kan være nødvendig
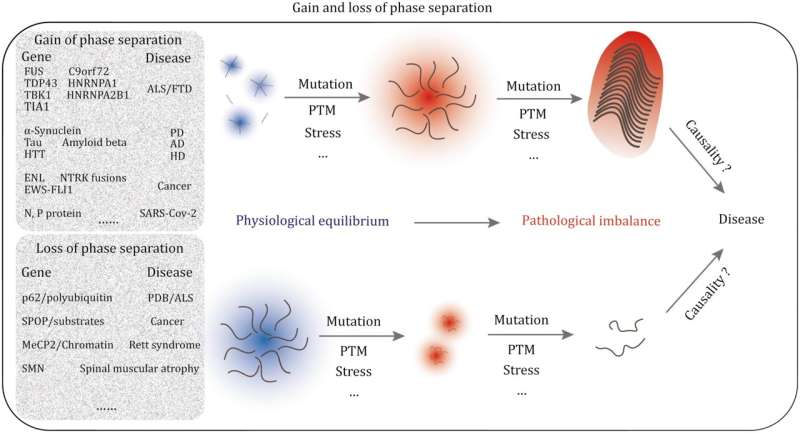
En gennemgang dykker ned i betydningen af biomolekylær kondensation i cellulære processer, indvirkningen af afvigende faseadskillelse på sygdomme som neurodegenerative sygdomme, kræftsygdomme og infektionssygdomme og potentialet for at manipulere faseadskillelse som en terapeutisk strategi.
Neurodegenerative sygdomme som ALS, FTD og andre pålægger globale sundhedssystemer en stadig større byrde. Inden for disse betingelser undergår proteiner såsom TDP-43, FUS, Tau, hnRNPA1, hnRNPA2B1 og polyQ-holdige proteiner unormal faseadskillelse, hvilket udløser irreversible biofysiske ændringer. Optrævlingen af mekanismerne bag afvigende faseadskillelse giver et nyt perspektiv på at forstå begyndelsen og progressionen af neurodegenerative sygdomme.
Ved kræft forstyrrer indviklede genetiske mutationer normale faseadskillelsesprocesser, hvilket fremmer tumordannelse. Bemærkelsesværdige tilfælde inkluderer fusionsgener i leukæmi og fusionsproteiner i sarkomer, der udløser betydelige skift i nedstrøms genregulering og fremmer malign tumorvækst. Målretning af afvigende faseadskillelse er en ny vej til at forstå og potentielt behandle kræft.
Patogener udnytter biomolekylære kondensater til at styrke infektionsevnen, mens værtens immunsystem udnytter faseadskillelse til at identificere og neutralisere patogener. Virale proteiner orkestrerer dannelsen af replikationscentre eller inklusionslegemer, som er afgørende for viral replikation og samling, og forstærker derved viral infektivitet. Forståelse af dynamikken i faseadskillelse under infektion kaster lys over vært-patogen-interaktioner og immunresponser, hvilket potentielt letter udviklingen af antivirale strategier.
Nuværende terapeutiske tilgange retter sig mod både "controllere" og "drivere" af væske-væskefaseseparation (LLPS). Controllere, der omfatter strukturelle proteiner som enzymer, celleoverfladereceptorer og transkriptionsfaktorer, gennemgår regulering via signalveje og post-translationelle modifikationer.
I mellemtiden spiller drivere, såsom specifikke iboende forstyrrede proteiner (IDP'er) og nukleinsyrer, afgørende roller i LLPS. Innovative lægemiddelscreeningsplatforme, som DropScan, lover at identificere forbindelser, der er i stand til at modulere afvigende faseadskillelse i sygdomme som cancer. Dybere indsigt i kondensatbiologi er afgørende for effektivt at manipulere forbigående samlinger til terapeutiske formål.
Gennemgangen konkluderer, at området for biomolekylær kondensation og faseseparation er i hastig udvikling, hvilket giver frisk indsigt i sygdomsmekanismer og potentielle terapeutiske strategier. Igangværende forskning præsenterer lovende perspektiver for transformative terapier, der omformer vores tilgang til sygdomsbehandling og patientpleje. Værket med titlen "Lang vej op:genovervej sygdomme i lyset af faseadskillelse og faseovergang" blev offentliggjort på Protein &Cell .
Flere oplysninger: Mingrui Ding et al., Langt opad:genovervej sygdomme i lyset af faseadskillelse og faseovergang, Protein &Cell (2023). DOI:10.1093/procel/pwad057
Leveret af Higher Education Press
 Varme artikler
Varme artikler
-
 Brændende chili vil holde elefanter i skak, ny undersøgelse finderKredit:University of Stirling Brændende chili kan afskrække elefanter fra at hærge afgrøder i afrikanske og asiatiske samfund, ifølge en ny undersøgelse, der involverede en University of Stirling
Brændende chili vil holde elefanter i skak, ny undersøgelse finderKredit:University of Stirling Brændende chili kan afskrække elefanter fra at hærge afgrøder i afrikanske og asiatiske samfund, ifølge en ny undersøgelse, der involverede en University of Stirling -
 Hvordan arter dannes:Hvad den sammenfiltrede historie om forholdet mellem isbjørne og brunbjørne f…En isbjørnemor og hendes 2-årige unger i det nordvestlige Grønland. Kredit:Øystein Wiig En ny undersøgelse giver et forbedret kig på isbjørnes og brune bjørnes sammenflettede evolutionære historier
Hvordan arter dannes:Hvad den sammenfiltrede historie om forholdet mellem isbjørne og brunbjørne f…En isbjørnemor og hendes 2-årige unger i det nordvestlige Grønland. Kredit:Øystein Wiig En ny undersøgelse giver et forbedret kig på isbjørnes og brune bjørnes sammenflettede evolutionære historier -
 Forståelse af livets samudviklende web som et netværkTukaner, såsom denne grønnæbbede tukan, er store spredere af frø fra nogle tropiske skovtræer, inklusive håndflader. Kredit:John Thompson Samevolution, som opstår, når arter interagerer og tilpass
Forståelse af livets samudviklende web som et netværkTukaner, såsom denne grønnæbbede tukan, er store spredere af frø fra nogle tropiske skovtræer, inklusive håndflader. Kredit:John Thompson Samevolution, som opstår, når arter interagerer og tilpass -
 Hvorfor interseeing kan være det boost, dækafgrøder har brug forEn enårig rajgræsdækafgrøde med mellemfrø etableret under en majskrone i august. Mellemsåning gør det muligt for dækafgrøder at etablere sig før høst uden at skade afgrødeudbyttet. Nyere forskning vis
Hvorfor interseeing kan være det boost, dækafgrøder har brug forEn enårig rajgræsdækafgrøde med mellemfrø etableret under en majskrone i august. Mellemsåning gør det muligt for dækafgrøder at etablere sig før høst uden at skade afgrødeudbyttet. Nyere forskning vis
- Sjældent glasagtigt metal opdaget under søgen efter at forbedre batteriets ydeevne
- NYC borgmester:Udvid kystlinjen for at beskytte byen mod storme
- Tomografisk måling af dielektriske tensorer
- Gamle jægere opholdt sig i det frosne Nordeuropa i stedet for at migrere, beviser fra polarrævekno…
- Forskere vurderer mulige scenarier for økologiske tjenester i Three-River-Source-regionen
- Hvad Jordens tyngdekraft afslører om klimaændringer


