DNA-sekventering: Definition, metoder, eksempler
Nukleotider er de kemiske byggesten i livet og findes i DNA fra levende organismer. Hvert nukleotid består af en sukker, fosfat og en nitrogenholdig base: adenin (A), thymin (T), cytosin (C) og guanin (G). Den specifikke rækkefølge af disse nukleotidbaser bestemmer, hvilke proteiner, enzymer og molekyler der vil blive syntetiseret af cellen.
Bestemmelse af rækkefølgen, eller sekvensen af nukleotider, er vigtig for studiet af mutationer, udvikling, sygdomsprogression, genetisk test, retsmedicinsk undersøgelse og medicin.
Genomik og DNA-sekventering <<> Genomik er studiet af DNA, gener, geninteraktioner og miljøpåvirkninger på gener. Hemmeligheden bag at afsløre den komplekse indre virkning af gener er at være i stand til at identificere deres struktur og placering på kromosomer.
Blåtryk af levende organismer bestemmes af rækkefølgen (eller sekvensen) af nukleinsyrebasepar i DNA. Når DNA replikeres parres adenin med thymin og cytosin med guanin; uoverensstemmende par betragtes som mutationer Siden den dobbelte helix deoxyribonucleinsyre (DNA) molekyle blev konceptualiseret i 1953, er der foretaget dramatiske forbedringer inden for genomik og storskala DNA-sekventering. Forskere arbejder flittigt med at anvende denne nye viden til individualiseret behandling af sygdomme. Samtidig tillader igangværende diskussioner forskere at holde sig foran de etiske implikationer af så hurtigt eksploderende teknologier. DNA-sekventering er processen til at opdage sekvensen af forskellige nukleotidbaser i DNA-fragmenter. Hele gensekventering tillader sammenligning af kromosomer og genomer, der findes i samme og forskellige arter. Kortlægning af kromosomer er nyttigt til videnskabelig forskning. Analyse af mekanismer og struktur for gener, alleler og kromosomale mutationer i DNA-molekyler antyder nye måder at behandle genetiske forstyrrelser og stoppe kræftformet tumorvækst, for eksempel. Frederick Sangers DNA-sekventeringsmetoder fremførte i vid udstrækning området genomik startende i 1970'erne. Sanger følte sig klar til at tackle DNA-sekventering efter vellykket sekventering af RNA, når man studerede insulin. Sanger var ikke den første videnskabsmand, der faldt i DNA-sekventering. Hans smarte DNA-sekventeringsmetoder - udviklet i tandem med kollegerne Berg og Gilbert - vandt imidlertid en nobelpris i 1980. Sangers største ambition var at sekventere store genomer i stor skala, men sekventering af en minuscule bakteriofagens basepar blekede i sammenligning med sekventering af de 3 milliarder basepar i det menneskelige genom. Ikke desto mindre var det at lære at sekvensere hele genomet til en ringe bakteriofag et stort skridt hen imod at sammenstyre hele genomet af mennesker. Fordi DNA og kromosomer består af millioner af basepar, adskiller de fleste sekventeringsmetoder DNA i små tråde, og derefter deles DNA-segmenterne sammen; det tager bare tid eller hurtige, sofistikerede maskiner. Sanger vidste den potentielle værdi af sit arbejde og samarbejdede ofte med andre forskere, der delte hans interesser i DNA, molekylærbiologi og livsvidenskab. Selvom langsomt og dyrt sammenlignet med nutidens sekventeringsteknologier, blev Sanger's DNA-sekventeringsmetoder rost på det tidspunkt. Efter forsøg og fejl fandt Sanger den hemmelige biokemiske "opskrift" til at adskille DNA-strenge, skabe mere DNA og identificere rækkefølgen af nukleotider i et genom. Materialer af høj kvalitet kan let købes til brug i laboratorium undersøgelser: Sanger regnede ud hvordan man skærer DNA i små segmenter ved hjælp af enzymet DNA-polymerase. Han lavede derefter mere DNA fra en skabelon og indsatte radioaktive sporstoffer i det nye DNA for at afgrænse sektioner af de adskilte strenge. Han erkendte også, at enzymet havde brug for en primer, der kunne binde til et specifikt sted på skabelonstrengen. I 1981 gjorde Sanger igen historie ved at finde ud af genomet til mitokondrialt DNA's 16.000 basepar. En anden spændende udvikling var haglegeværmetoden, der tilfældigt samplede og sekventerede op til 700 basepar ad gangen. Sanger er også kendt for sin anvendelse af dideoxy-metoden (dideoxynukleotid), der indsætter et kædeterminerende nukleotid under DNA-syntese for at markere sektioner af DNA til analyse.Dideoxynukleotider forstyrrer DNA-polymeraseaktivitet og forhindrer nukleotider i at bygge videre på en streng DNA. Temperaturen skal justeres omhyggeligt under hele sekventeringsprocessen. Først sættes kemikalier til et rør og opvarmes for at afdække (denaturere) det dobbeltstrengede DNA-molekyle. Derefter afkøles temperaturen, så primeren kan binde. Derefter hæves temperaturen for at tilskynde til optimal DNA-polymerase (enzym) aktivitet. Polymerase bruger typisk de tilgængelige normale nucleotider, som er tilsat ved en højere koncentration. Når polymerase kommer til et "kædeterminerende" farvestofbundet nukleotid, stopper polymerasen, og kæden ender der, hvilket forklarer, hvorfor de farvede nukleotider kaldes "kædeterminerende" eller "terminatorer." Processen fortsætter mange, mange gange. Til sidst er det farvestofbundne nukleotid anbragt i hver enkelt position af DNA-sekvensen. Gelelektroforese og computerprogrammer kan derefter identificere farvestoffarverne på hver af DNA-strengene og finde ud af hele sekvensen af DNA baseret på farvestoffet, farvestoffets placering og længden af strengene. Sekvensering med høj kapacitet - generelt omtalt som næste generations sekvensering Næste generation af sekventeringsmetoder kan håndtere DNA-analyse med højt volumen uden det ekstra trin til amplifikation eller kloning til få nok DNA til sekventering. DNA-sekventeringsmaskiner kører flere sekventeringsreaktioner på én gang, hvilket er billigere og hurtigere. I det væsentlige kører den nye DNA-sekventeringsteknologi hundredevis af Sanger-reaktioner på en lille, let læselig mikrochip, der derefter køres gennem en computer program, der samler sekvensen. Teknikken læser kortere DNA-fragmenter, men det er stadig hurtigere og mere effektivt end Sangers sekvenseringsmetoder, så selv store projekter kan hurtigt afsluttes. Human Genome Project, afsluttet i 2003, er en af de mest berømte sekventeringsundersøgelser, der er gjort til dato. Ifølge en artikel i 2018 i Science News Institute kortlagde projektet det humane genom med succes en sammensat prøve taget fra anonyme bloddonorer. Human Genome Project er baseret på bakterielt kunstigt kromosom (BAC) -baserede) sekventeringsmetoder til kortlægning af basepar. Teknikken anvendte bakterier til at klone DNA-fragmenter, hvilket resulterede i store mængder DNA til sekventering. Klonerne blev derefter reduceret i størrelse, anbragt i en sekventeringsmaskine og samlet til strækninger, der repræsenterede humant DNA. Nye opdagelser inden for genomik ændrer dybtgående fremgangsmåder til sygdomsforebyggelse, detektion og behandling. Regeringen har forpligtet milliarder af dollars til DNA-forskning. Retshåndhævelse er afhængig af DNA-analyse for at løse sager. DNA-testsæt kan købes til hjemmebrug til forskning i aner og identificere genvarianter, der kan udgøre sundhedsmæssige risici: Nye teknologier har ofte muligheden for social fordel samt skade; eksempler inkluderer funktionsdygtige atomkraftværker og masseødelæggelsesvåben. DNA-teknologier er også forbundet med risici. Følelsesmæssige bekymringer omkring DNA-sekventerings- og genredigeringsværktøjer som CRISPR inkluderer frygt for, at teknologien kan lette menneskelig kloning eller føre til mutante transgene dyr, der er skabt af en rogue forsker. Oftere har etiske spørgsmål relateret til DNA-sekventering at gøre med informeret samtykke. Let adgang til DNA-test direkte til forbruger betyder, at forbrugere muligvis ikke helt forstår, hvordan deres genetiske information vil blive brugt, opbevaret og delt. Lækfolk er måske ikke følelsesmæssigt klar til at lære om deres mangelfulde genetiske varianter og sundhedsrisici. Tredjeparter såsom arbejdsgivere og forsikringsselskaber kan potentielt diskriminere personer, der bærer mangelfulde gener, der kan give anledning til alvorlige medicinske problemer.
.
Definition af DNA-sekventering
DNA Sequencing: Early Research
Grundlæggende om DNA-rækkefølge -
Metoder til DNA-sekventering: Sanger Methods
DNA-sekventeringstrin
Fremskridt inden for DNA-sekventeringsteknologi
- bruger nye fremskridt og teknologier til at sekvensere nukleotidbaser hurtigere og billigt end nogensinde før. En DNA-sekventeringsmaskine kan let håndtere store DNA-strækninger. Faktisk kan hele genomerne udføres i løbet af timer i stedet for år med Sangers sekventeringsteknikker.
The Human Genome Project
består det humane genom af cirka 46.831 gener, hvilket var en formidabel udfordring til sekvensen. Topforskere fra hele verden brugte næsten 10 år på at samarbejde og konsultere. Under ledelse af National Human Genome Research
Andre DNA-sekvenseksempler
Etiske implikationer af DNA-sekventering
Sidste artikelGenetisk modifikation: Definition, typer, proces, eksempler
Næste artikelOrganisme: Definition, typer, egenskaber og eksempler
 Varme artikler
Varme artikler
-
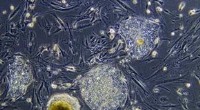 Hvorfor ville forskere gerne oprette et hybrid menneske-ko-embryo?Mikroskopisk 10x visning af en koloni af embryonale stamceller (stamcellekolonierne er de afrundede, tætte cellemasser.) Foto høflighed University of Wisconsin Board of Regents Denne uge, en gruppe L
Hvorfor ville forskere gerne oprette et hybrid menneske-ko-embryo?Mikroskopisk 10x visning af en koloni af embryonale stamceller (stamcellekolonierne er de afrundede, tætte cellemasser.) Foto høflighed University of Wisconsin Board of Regents Denne uge, en gruppe L -
 Bliver din hjerne træt som resten af din krop?Hvem har ikke følt hjerneflugt efter en stressende dag på kontoret? PeopleImages/Getty Images Hvem blandt os har ikke oplevet mental træthed efter at have arbejdet en lang dag, tage finalerne eller k
Bliver din hjerne træt som resten af din krop?Hvem har ikke følt hjerneflugt efter en stressende dag på kontoret? PeopleImages/Getty Images Hvem blandt os har ikke oplevet mental træthed efter at have arbejdet en lang dag, tage finalerne eller k -
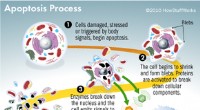 Hvad er apoptose?Apoptosediagram © 2010 HowStuffWorks.com Der er to måder, hvorpå en celle kan dø:nekrose og apoptose. Nekrose opstår, når en celle er beskadiget af en ekstern kraft, såsom gift, en kropsskade, en i
Hvad er apoptose?Apoptosediagram © 2010 HowStuffWorks.com Der er to måder, hvorpå en celle kan dø:nekrose og apoptose. Nekrose opstår, når en celle er beskadiget af en ekstern kraft, såsom gift, en kropsskade, en i -
 Glykolyse: Definition, trin, produkter og reaktanterI overensstemmelse med de grundlæggende fysiske love har alle levende ting brug for energi fra miljøet i en eller anden form for at opretholde livet. Det er klart, at forskellige organismer har udvikl
Glykolyse: Definition, trin, produkter og reaktanterI overensstemmelse med de grundlæggende fysiske love har alle levende ting brug for energi fra miljøet i en eller anden form for at opretholde livet. Det er klart, at forskellige organismer har udvikl


