Hvad er valenscelle?
Her er en sammenbrud:
* Elektroner: Negativt ladede partikler, der kredserer kernen i et atom.
* Elektronskaller: Regioner omkring kernen, hvor elektroner findes med forskellige energiniveauer. Jo højere skalnummer, jo længere er fra kernen, og jo højere er energiniveauet.
* Valence Shell: Den yderste elektronskal, der indeholder valenselektroner.
Hvorfor er valensskallen vigtig?
* Kemisk binding: Valenselektroner er dem, der er involveret i dannelse af kemiske bindinger med andre atomer. De kan deles (kovalent binding) eller overføres (ionisk binding).
* Kemisk reaktivitet: Antallet af valenselektroner bestemmer en atoms tendens til at vinde, miste eller dele elektroner, der dikterer dens reaktivitet. For eksempel har elementer med en valenselektron en tendens til at miste det og blive positivt ladede ioner, mens elementer med syv valenselektroner har en tendens til at få en elektron og blive negativt ladede ioner.
* Forudsigelse af kemisk adfærd: Ved at forstå konfigurationen af valenselektroner kan vi forudsige, hvordan et element vil opføre sig i kemiske reaktioner.
Eksempel:
Overvej elementet natrium (NA). Det har en valenselektron i sin yderste skal (3S¹). Denne enkelt elektron går let tabt, hvilket gør natrium meget reaktiv og sandsynligvis danner en positiv ion (Na+).
Kortfattet:
Valensskallen er afgørende for at forstå, hvordan atomer interagerer med hinanden, og hvordan elementer opfører sig i kemiske reaktioner. Det er et grundlæggende koncept inden for kemi, der giver os mulighed for at forudsige og forklare egenskaberne og reaktionerne fra forskellige elementer.
Sidste artikelHvad betyder DNA -replikation?
Næste artikelHvad er funktionen af orbicularis oris?
 Varme artikler
Varme artikler
-
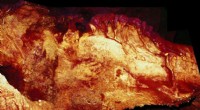 Neanderthalere var faktisk forhistoriske PicassosDette panel i Maltravieso Cave i Spanien viser nogle håndstenciler. Forskere har dateret det til mindst 64, 000 år siden og fastslog, at det må have været lavet af en neandertaler. H. Collado/Universi
Neanderthalere var faktisk forhistoriske PicassosDette panel i Maltravieso Cave i Spanien viser nogle håndstenciler. Forskere har dateret det til mindst 64, 000 år siden og fastslog, at det må have været lavet af en neandertaler. H. Collado/Universi -
 Forskere udforsker sandart til akvakulturDen anden del af den Montello-baserede sandart aquaponics-ligning er salatstativer, fodret med vand beriget med næringsstofferne i fiskeaffald. Kredit:Aaron Conklin Mere end tusind sandart er i de
Forskere udforsker sandart til akvakulturDen anden del af den Montello-baserede sandart aquaponics-ligning er salatstativer, fodret med vand beriget med næringsstofferne i fiskeaffald. Kredit:Aaron Conklin Mere end tusind sandart er i de -
 Nye rammer for at udlede mikrobielle interaktionerKredit:CC0 Public Domain Afgørelse af de underliggende økologiske netværk i mikrobielle samfund er vigtig for at forstå deres struktur og reaktioner på eksterne stimuli. Men det kan være meget udf
Nye rammer for at udlede mikrobielle interaktionerKredit:CC0 Public Domain Afgørelse af de underliggende økologiske netværk i mikrobielle samfund er vigtig for at forstå deres struktur og reaktioner på eksterne stimuli. Men det kan være meget udf -
 Pattedyrs hjerner identificerer typen af duft hurtigere end engang troedeKredit:CC0 Public Domain Det tager mindre end en tiendedel af et sekund-en brøkdel af den tid, man tidligere troede-for lugtesansen at skelne mellem en lugt og en anden, viser nye forsøg med mus.
Pattedyrs hjerner identificerer typen af duft hurtigere end engang troedeKredit:CC0 Public Domain Det tager mindre end en tiendedel af et sekund-en brøkdel af den tid, man tidligere troede-for lugtesansen at skelne mellem en lugt og en anden, viser nye forsøg med mus.
- Hvornår er potentiel energi 0?
- Hvorfor er Grand Canyon vigtig for forskere, der studerer Jorden forbi?
- Deling af elektrisk scooter bevæger sig ind i hurtigbanen
- Kan du se andre planeter med et teleskop?
- Klimaændringer forventes at bringe flere ekstremer til det indre af det sydlige Californien
- Hvilken type sediment består hovedsageligt skallerne og radiolarians?


