Hvordan beskriver du en Daniell -celle?
Komponenter:
* to halvceller:
* anode: Sammensat af en zinkelektrode nedsænket i en zinksulfatopløsning (ZnSO₄). Zink oxideres ved anoden og frigiver elektroner i det ydre kredsløb.
* katode: Sammensat af en kobberelektrode nedsænket i en kobbersulfatopløsning (cuso₄). Kobberioner (cu²⁺) i opløsningen reduceres ved katoden og accepterer elektroner fra det ydre kredsløb.
* saltbro: En porøs barriere, der forbinder de to halvceller. Det giver strømmen af ioner mulighed for at opretholde elektrisk neutralitet i opløsningerne og forhindre opbygning af ladning, der ville stoppe reaktionen.
* eksternt kredsløb: En ledning, der forbinder anoden og katoden, hvilket giver elektroner mulighed for at strømme fra anoden til katoden.
reaktion:
Den samlede reaktion i en Daniell -celle er:
Zn (s) + Cu²⁺ (aq) → Zn²⁺ (aq) + cu (s)
* anode (oxidation): Zn (S) → Zn²⁺ (aq) + 2e⁻
* katode (reduktion): Cu²⁺ (aq) + 2e⁻ → cu (s)
hvordan det fungerer:
1. zinkatomer ved anoden mister elektroner og blive zinkioner (Zn²⁺), der opløses i zinksulfatopløsningen.
2. elektroner flyder gennem det eksterne kredsløb fra anoden til katoden.
3. og reduceres til kobberatomer, der deponeres på kobberelektroden.
4. Saltbroen giver ioner mulighed for at strømme mellem halvcellerne At opretholde elektrisk neutralitet. Dette forhindrer opbygning af positiv ladning i zinkhalvcelle og negativ ladning i kobberhalvcelle.
Egenskaber:
* producerer en stabil spænding på omkring 1,1 volt.
* har en relativt lang levetid.
* ikke-genopladelig. Når zinkelektroden er konsumeret, holder cellen op med at fungere.
Ansøgninger:
* Historisk set blev Daniell -celler brugt som en praktisk elektricitetskilde.
* I dag bruges de hovedsageligt i uddannelsesmæssige omgivelser At demonstrere principperne for elektrokemi.
Kortfattet:
Daniell -cellen er et simpelt, men alligevel vigtigt eksempel på en elektrokemisk celle, der omdanner kemisk energi til elektrisk energi. Det viser principperne for oxidationsreduktionsreaktioner, elektronstrøm og ionisk transport, hvilket giver en grundlæggende forståelse af, hvordan batterier fungerer.
 Varme artikler
Varme artikler
-
 Hvordan undertrykker CRABS CLAW TORNADO 2 i planteudviklingDobbeltmutanter formår ikke at afslutte blomstermeristem og fortsætter med at producere ekstra blomsterorganer. Kredit:Toshiro Ito Mange basisfødevarer som korn og frugter stammer fra blomstrende
Hvordan undertrykker CRABS CLAW TORNADO 2 i planteudviklingDobbeltmutanter formår ikke at afslutte blomstermeristem og fortsætter med at producere ekstra blomsterorganer. Kredit:Toshiro Ito Mange basisfødevarer som korn og frugter stammer fra blomstrende -
 Ny teknik gennemsøger genomet for gener, der bekæmper sygdomMIT-forskere har tilpasset CRISPR genom-redigeringssystemet til at identificere gener, der beskytter celler mod et protein forbundet med Parkinsons sygdom. Kredit:Jose-Luis Olivares/MIT Ved hjælp
Ny teknik gennemsøger genomet for gener, der bekæmper sygdomMIT-forskere har tilpasset CRISPR genom-redigeringssystemet til at identificere gener, der beskytter celler mod et protein forbundet med Parkinsons sygdom. Kredit:Jose-Luis Olivares/MIT Ved hjælp -
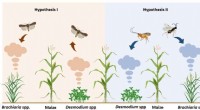 Hvordan push-pull ledsagende afgrøder hjælper med at håndtere den ødelæggende efterårshærormSkematisk repræsentation af et Push-Pull felt og forskningshypoteserne:(1) Ledsagende planteflygtige stoffer [Desmodium spp. mellemafgrøder (grønbladede desmodium, D. intortum eller sølvbladedesmodium
Hvordan push-pull ledsagende afgrøder hjælper med at håndtere den ødelæggende efterårshærormSkematisk repræsentation af et Push-Pull felt og forskningshypoteserne:(1) Ledsagende planteflygtige stoffer [Desmodium spp. mellemafgrøder (grønbladede desmodium, D. intortum eller sølvbladedesmodium -
 Retten godkender at dræbe en type ugle for at se effekten på andre uglerI denne 13. dec. 2017 foto, en sprosset hunugle sidder på en gren i de skovklædte bakker uden for Philomath, En føderal appeldomstol i San Francisco har stadfæstet en plan fra dyrelivsembedsmænd om at
Retten godkender at dræbe en type ugle for at se effekten på andre uglerI denne 13. dec. 2017 foto, en sprosset hunugle sidder på en gren i de skovklædte bakker uden for Philomath, En føderal appeldomstol i San Francisco har stadfæstet en plan fra dyrelivsembedsmænd om at


