Hvilket eksperiment viser, hvordan PH påvirker enzymer?
eksperimentet
1. Materialer:
* enzym: Du har brug for et enzym, der er let at arbejde med. Et populært valg er katalase , som findes i mange levende ting (som kartofler eller lever). Det nedbryder hydrogenperoxid (H₂O₂) i vand og ilt.
* Hydrogenperoxid: Underlaget for katalase.
* buffere: Løsninger, der modstår ændringer i pH. Du har brug for en række buffere for at skabe forskellige pH -niveauer. Almindelige valg er:
* phosphatbuffer: For pH-område 6-8
* Citratbuffer: For pH-område 3-6
* Tris -buffer: For pH-område 7-9
* Testrør: For at holde reaktionsblandingerne.
* Graduerede cylindre: At måle væsker nøjagtigt.
* termometer: For at sikre, at alle reaktioner forekommer ved den samme temperatur.
* måleenhed: Dette kan være en:
* gradueret cylinder For at måle mængden af produceret iltgas.
* spektrofotometer For at måle faldet i hydrogenperoxidkoncentration over tid (mere avanceret).
2. Procedure:
1. Forbered dine buffere: Opret en række buffere med forskellige pH -niveauer (f.eks. Ph 4, 5, 6, 7, 8).
2. Opret dine reaktionsblandinger: I separate testrør skal du kombinere følgende:
* Et specifikt volumen af din valgte bufferopløsning.
* Et fast volumen af enzymopløsningen (katalase).
* Et fast volumen af brintperoxidopløsning.
3. kontrol: Opret en kontrolreaktion med de samme ingredienser, men ved hjælp af destilleret vand i stedet for en buffer. Dette vil hjælpe med at bestemme, om selve bufferen påvirker reaktionen.
4. inkuber: Placer alle testrørene i et vandbad eller inkubator for at opretholde en konstant temperatur (ca. 25 ° C).
5. observere: Registrer reaktionshastigheden. Dette kan gøres af:
* Måling af mængden af produceret iltgas: Observer dannelsen af bobler i reagensglaset, og brug en gradueret cylinder til at måle mængden af gas, der er produceret over en bestemt tidsperiode.
* Måling af faldet i brintperoxidkoncentration: Brug et spektrofotometer til at måle absorbansen af brintperoxid ved specifikke bølgelængder.
6. Gentag: Gentag eksperimentet med det samme enzym- og substratkoncentrationer, men brug forskellige pH -buffere for at se, hvordan reaktionshastigheden ændres.
3. Forventede resultater:
* optimal pH: Du skal finde ud af, at enzymet har en optimal pH, hvor det fungerer bedst. Dette er pH, hvor enzymets aktive sted har den rigtige form til at binde til underlaget effektivt.
* Nedsat aktivitet: Ved pH -niveauer over eller under det optimale vil enzymets aktivitet falde. Dette skyldes, at pH -værdien kan påvirke formen på det aktive sted, hvilket gør det mindre effektivt til at binde til underlaget.
Nøglekoncepter:
* enzymer er proteiner: De har en bestemt tredimensionel form, der er kritisk for deres funktion.
* Aktivt sted: Den del af enzymet, der binder til underlaget.
* optimal pH: Den pH, hvor et enzym fungerer bedst.
* denaturering: Ekstreme pH -niveauer kan få enzymer til at miste deres form og blive inaktive.
Dataanalyse
* Graf dine resultater, og planlægger pH-værdierne på x-aksen og reaktionshastigheden (f.eks. Mængde af iltgas produceret eller fald i brintperoxidkoncentration) på Y-aksen.
* Du skal se en klokkeformet kurve, hvor toppen repræsenterer den optimale pH for enzymet.
Lad mig vide, om du har mere specifikke spørgsmål eller ønsker at udforske andre eksperimenter!
 Varme artikler
Varme artikler
-
 Pomodoro -teknikken:Du kan klare enhver opgave 25 minutter ad gangenAt arbejde hele natten for at gennemføre et projekt er ikke den bedste måde at opnå gode resultater på. At arbejde i korte spor er faktisk bedre for dig og din kreativitet. LumiNola/Getty Images Fore
Pomodoro -teknikken:Du kan klare enhver opgave 25 minutter ad gangenAt arbejde hele natten for at gennemføre et projekt er ikke den bedste måde at opnå gode resultater på. At arbejde i korte spor er faktisk bedre for dig og din kreativitet. LumiNola/Getty Images Fore -
 Hvorfor går folk normalt i samme retning?Når du går en tur rundt om blokken, er der noget der driver dig til at dreje til højre eller venstre? Er der noget mere ved dette end vane? Erik Witsoe/EyeEm/Getty Images Vil du slå stregerne under d
Hvorfor går folk normalt i samme retning?Når du går en tur rundt om blokken, er der noget der driver dig til at dreje til højre eller venstre? Er der noget mere ved dette end vane? Erik Witsoe/EyeEm/Getty Images Vil du slå stregerne under d -
 Sådan fungerer BRCA -generDet er en brystkræftcelle som fanget af et scannende elektronmikroskop, som producerer et 3D-billede. Billede høflighed Bruce Wetzel og Harry Schaefer)/National Cancer Institutes websted Takket være
Sådan fungerer BRCA -generDet er en brystkræftcelle som fanget af et scannende elektronmikroskop, som producerer et 3D-billede. Billede høflighed Bruce Wetzel og Harry Schaefer)/National Cancer Institutes websted Takket være -
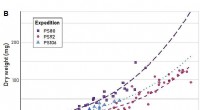 At måle er at vide:Hvor lang er en krill, og hvor tung er en polartorsk?Længde-vægt forhold af amfipoden Themisto libellula fanget under flere arktiske ekspeditioner om bord på den tyske isbryder Polarstern. Disse ekspeditioner fandt sted i forskellige perioder af året. (
At måle er at vide:Hvor lang er en krill, og hvor tung er en polartorsk?Længde-vægt forhold af amfipoden Themisto libellula fanget under flere arktiske ekspeditioner om bord på den tyske isbryder Polarstern. Disse ekspeditioner fandt sted i forskellige perioder af året. (
- Hvordan adskiller den nukleare sekvens af kodningstrand et DNA -molekyle fra RNA produceret?
- Hvad er lighederne mellem plante- og dyreceller?
- Hvilke bjergarter er mest modtagelige for biologisk forvitring og hvorfor?
- Hvad er energifaluta for kroppen?
- Smart software -værktøj kan bane vejen for at ændre, hvordan tingene bliver designet, lavet, og l…
- Hvilken form for DCPIP reduceret eller oxideret har højere energi?


