Hvad kaldes lange kæder af aminosyrer? Forståelse af proteiner og polypeptider
Af Paul Dohrman
Opdateret 24. marts 2022
Proteiner:Polymerer af aminosyrer
Proteiner er lange polymerer lavet af de 20 naturligt forekommende aminosyrer. Selvom nogle proteiner inkorporerer ikke-kanoniske rester, er rygraden i hvert protein en kæde af aminosyrer forbundet med peptidbindinger.
Fra DNA til protein:Oversættelsesprocessen
Rejsen begynder i kernen, hvor et segment af DNA transskriberes til messenger RNA (mRNA). mRNA'et forlader kernen og binder sig til et ribosom, cellens proteinsyntesemaskine. Transfer RNA (tRNA) molekyler bringer de passende aminosyrer til ribosomet, hvor de sekventielt føjes til den voksende polypeptidkæde.
Peptidbindinger og polypeptider
Tilstødende aminosyrer forbindes hoved-mod-hale via peptidbindinger:carboxylgruppen (-COOH) i en rest binder til aminogruppen (-NH2) i den næste. Den resulterende kæde kaldes et polypeptid. Peptidbindingen giver planaritet til rygraden, men tillader rotation omkring enkeltbindingerne, hvilket giver den nødvendige kædefleksibilitet til foldning.
Sidekæder former proteinstruktur
Hver aminosyre har en særskilt sidekæde (R-gruppe) knyttet til dens centrale kulstof. Disse sidekæder adskiller sig i størrelse, ladning og hydrofobicitet, hvilket påvirker, hvordan kæden interagerer med sig selv og med det vandige cellulære miljø. Polære sidekæder har en tendens til at orientere sig mod opløsningsmidlet, mens ikke-polære grupper samles inde i proteinkernen og driver foldningsprocessen.
Sekvensen bestemmer foldningen
Den primære aminosyresekvens koder for den unikke tredimensionelle form af proteinet. Fordi rygraden kan rotere frit, foldes de fleste polypeptider spontant til en enkelt, energisk favoriseret konformation. Selv en enkelt aminosyresubstitution kan forstyrre foldningen, hvilket gør proteinet ufunktionelt.
Kombinatorisk mangfoldighed og funktionelle begrænsninger
Med 20 tilgængelige aminosyrer er der 20 n teoretiske polypeptider med længden n. Imidlertid foldes kun en meget lille del af disse sekvenser til stabile, funktionelle proteiner. Langt de fleste ville være ustabile eller antage flere lavenergikonformationer, så evolutionært tryk udvælger kun de få sekvenser, der opfylder organismens funktionelle behov.
Referencer
- Cellens molekylærbiologi; Alberts et al.; 1994
- Kemi; Raymond Chang; 1984
 Varme artikler
Varme artikler
-
 Hvad er forskellen mellem en bakteriel og viral infektion?Den kraftfulde MRSA -bakterie kan forårsage en række sygdomme og symptomer hos mennesker. Science Photo Library/SCIEPRO/Getty Images Det er ikke sjovt at vågne med halsen i brand og hovedet banker. D
Hvad er forskellen mellem en bakteriel og viral infektion?Den kraftfulde MRSA -bakterie kan forårsage en række sygdomme og symptomer hos mennesker. Science Photo Library/SCIEPRO/Getty Images Det er ikke sjovt at vågne med halsen i brand og hovedet banker. D -
 Svage sociale bånd en dræber for hanhvalerEn spækhugger fra sydstaterne bryder ud af vandet. Kredit:Kenneth Balcomb, Center for Hvalforskning Spækhuggere er mere tilbøjelige til at dø, hvis de ikke er i centrum af deres sociale gruppe, ty
Svage sociale bånd en dræber for hanhvalerEn spækhugger fra sydstaterne bryder ud af vandet. Kredit:Kenneth Balcomb, Center for Hvalforskning Spækhuggere er mere tilbøjelige til at dø, hvis de ikke er i centrum af deres sociale gruppe, ty -
 Forskere fuldfører den første omfattende trusselsvurdering af alle amerikanske træerUnge træer af truet Q. Oglethorpensis ved Morton Arboretum. Kredit:Morton Arboretum For første gang har forskere gennemført trusselsvurderinger for alle 881 hjemmehørende træarter i det sammenhænge
Forskere fuldfører den første omfattende trusselsvurdering af alle amerikanske træerUnge træer af truet Q. Oglethorpensis ved Morton Arboretum. Kredit:Morton Arboretum For første gang har forskere gennemført trusselsvurderinger for alle 881 hjemmehørende træarter i det sammenhænge -
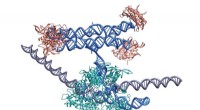 RNA origami muliggør applikationer inden for syntetisk biologiMolekylær model, der viser dCas9 bundet til et guide RNA-RNA origami fusionsmolekyle, der bringer transkriptionsfaktorer til en promotorsekvens. Kredit:Cody Geary, Aarhus Universitet Udvikling af v
RNA origami muliggør applikationer inden for syntetisk biologiMolekylær model, der viser dCas9 bundet til et guide RNA-RNA origami fusionsmolekyle, der bringer transkriptionsfaktorer til en promotorsekvens. Kredit:Cody Geary, Aarhus Universitet Udvikling af v
- Når teorien om, at solen går rundt på Jorden, blev erstattet med dette eksempel på?
- To radiorelikvier opdaget i galaksehoben Abell 168
- Sådan finder du townships og sektioner på en Map
- Der er 8 millioner grunde til, at du skal være ligeglad, hvis Magic Leap lykkes
- Lockheed Martin vinder $7,2 mia Air Force satellitkontrakt
- Hvad er levende organismer, der forårsager sygdom?


