DIY-batteri:Forsyn et kredsløb med cola og eddike
Af Chris Deziel – Opdateret 24. marts 2022
Alexander Shalamov/Hemera/Getty Images
Batterier omdanner kemisk energi til elektrisk energi. Mens et citronbatteri kun giver et beskedent output, demonstrerer det det samme princip, som driver bilbatterier. Denne vejledning viser, hvordan man bygger en funktionel elektrokemisk celle derhjemme ved hjælp af to hverdagsting:Coca‑Cola og eddike.
Sådan fungerer et batteri
En grundlæggende elektrokemisk celle består af en anode, en katode og en elektrolyt. Anoden (negativ elektrode) og katoden (positiv elektrode) er lavet af to forskellige metaller, der reagerer med forskellige hastigheder. Isoleret strømmer elektroner for langsomt til at generere brugbar strøm. Nedsænkning af elektroderne i en elektrolyt - normalt en sur opløsning - skaber en kemisk gradient, der skubber elektroner gennem et eksternt kredsløb. Så længe den kemiske reaktion fortsætter, producerer cellen en konstant spænding.
Lav et cola-batteri
Enhver læskedrik, der indeholder phosphorsyre, kan tjene som elektrolytten; Coca‑Cola (almindelig eller diæt) er et populært valg. Klip en strimmel fra aluminiumsdåsen, og slib derefter malingen af for at blotlægge metallet. Brug en lille kobberstrimmel til anoden. Læg begge strimler i et glas Coca-Cola og tilslut et voltmeter. Du bør læse omkring 0,75 V. Aluminium fungerer som katode, mens kobber fungerer som anode.
Lav et eddikebatteri
Eddike, som indeholder eddikesyre, er en fremragende elektrolyt. Brug en kobberstrimmel til anoden. En zinkelektrode - såsom en galvaniseret søm belagt med zink - tjener som en bedre katode end aluminium. Nedsænkning af de to elektroder i eddike giver omkring 1 V. For at forsyne en lysdiode skal du forbinde to celler i serie:Sæt lysdioden mellem anoden på den første celle og katoden på den anden, og slå derefter de resterende elektroder med en ledning.
Observation af en eddikecelle
Fordi eddike er klar, kan du se reaktionen i realtid. Efter at have kørt en LED natten over, inspicer zinkelektroden. En mørk, sort aflejring af kobberatomer vil være dannet, da hydrogenioner kombineres med elektroner og sætter sig på zinkoverfladen. Du kan også se, at der dannes bobler af brintgas på kobberstrimlen - hydrogenioner får elektroner til at blive til brintatomer, som parres til H₂-molekyler.
 Varme artikler
Varme artikler
-
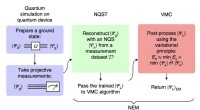 En neuralt netværksbaseret strategi til at forbedre kortsigtede kvantesimuleringerFigur, der opsummerer strategien for reduktion af neurale fejl. Kredit:Bennewitz et al. Kortsigtede kvantecomputere, kvantecomputere udviklet i dag eller i den nærmeste fremtid, kunne hjælpe med at
En neuralt netværksbaseret strategi til at forbedre kortsigtede kvantesimuleringerFigur, der opsummerer strategien for reduktion af neurale fejl. Kredit:Bennewitz et al. Kortsigtede kvantecomputere, kvantecomputere udviklet i dag eller i den nærmeste fremtid, kunne hjælpe med at -
 Højesteret afviser appel om netneutralitetI denne 9. okt. 2018 foto, politikontor bevogter hovedindgangen til højesteret i Washington. Højesteret har afsluttet rettens kamp om ophævede Obama-æra-regler om netneutralitet, der krævede, at inter
Højesteret afviser appel om netneutralitetI denne 9. okt. 2018 foto, politikontor bevogter hovedindgangen til højesteret i Washington. Højesteret har afsluttet rettens kamp om ophævede Obama-æra-regler om netneutralitet, der krævede, at inter -
 Opbygning af en hjemmelavet generatorspole:Trin-for-trin instruktionerAf Kim Sarah | Opdateret 24. marts 2022 En generator omdanner mekanisk energi til elektricitet ved at inducere en magnetisk ændring i en trådspole. Med blot nogle få husholdningsartikler kan du bygge
Opbygning af en hjemmelavet generatorspole:Trin-for-trin instruktionerAf Kim Sarah | Opdateret 24. marts 2022 En generator omdanner mekanisk energi til elektricitet ved at inducere en magnetisk ændring i en trådspole. Med blot nogle få husholdningsartikler kan du bygge -
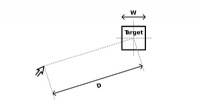 Opdatering af en lov, der former din teknologiDiagram over Fitts lov -- som nu skal ændres. Kredit:North Carolina State University Selvom du måske ikke tænker over, hvordan knapperne og ikonerne på din computerskærm blev designet, der er mang
Opdatering af en lov, der former din teknologiDiagram over Fitts lov -- som nu skal ændres. Kredit:North Carolina State University Selvom du måske ikke tænker over, hvordan knapperne og ikonerne på din computerskærm blev designet, der er mang
- Hvad holder ionerne sammen i natriumchlorid indikerer specifikke ladninger, der er involveret?
- Hvad hedder den store organelle, der kontrollerer alle aktiviteter?
- Hvorfor bruger nogle bygherrer kalksten og sandsten?
- Hvorfor perovskite solceller er så effektive
- Mod et orrery for kvantemålteori
- Hvorfor ser vi alle typer bølger i det elektromagnetiske spektrum?


