Hvad sker der med størrelsen af atomer, når du bevæger dig ned i det periodiske system i gruppe 7?
Her er en oversigt over tendensen:
1. Fluor (F):Det mindste atom i gruppe 7. Det har kun én elektronskal og en lille atomradius.
2. Klor (Cl):Større end fluor. Den har to elektronskaller, hvilket øger atomradius.
3. Brom (Br):Større end klor. Den har tre elektronskaller, hvilket resulterer i en yderligere stigning i atomradius.
4. Jod (I):Det største atom i gruppe 7. Det har fem elektronskaller, hvilket bidrager til dets væsentligt større atomradius sammenlignet med de andre grundstoffer i gruppen.
Så når du bevæger dig ned i gruppe 7 fra fluor til jod, øges atomernes størrelse på grund af tilføjelsen af flere elektronskaller, hvilket svarer til det stigende atomnummer.
Sidste artikelHvordan påvirker osmotisk potentiale diffusionen?
Næste artikelHvad er hydrogen fysisk tilstand ved stuetemperatur?
 Varme artikler
Varme artikler
-
 Spintronics:Hurtigere databehandling gennem ultrakorte elektriske impulserKredit:CC0 Public Domain Fysikere ved Martin Luther University Halle-Wittenberg (MLU) og Lanzhou University i Kina udviklede et simpelt koncept, der betydeligt kunne forbedre magnetisk-baseret dat
Spintronics:Hurtigere databehandling gennem ultrakorte elektriske impulserKredit:CC0 Public Domain Fysikere ved Martin Luther University Halle-Wittenberg (MLU) og Lanzhou University i Kina udviklede et simpelt koncept, der betydeligt kunne forbedre magnetisk-baseret dat -
 Første rapport om superledningsevne i et nikkeloxidmaterialeEn illustration viser et nøgletrin i at skabe en ny type superledende materiale:Ligesom at trække blokke fra et tårn i et Jenga-spil, videnskabsmænd brugte kemi til pænt at fjerne et lag iltatomer. De
Første rapport om superledningsevne i et nikkeloxidmaterialeEn illustration viser et nøgletrin i at skabe en ny type superledende materiale:Ligesom at trække blokke fra et tårn i et Jenga-spil, videnskabsmænd brugte kemi til pænt at fjerne et lag iltatomer. De -
 Livets arkitektur beskrevet ved computermodelleringEn af de enkleste tensegrity -strukturer - tre stive stænger (blå) holdt fast i en stabil konformation af fleksible strenge (sort) - kan også tjene som model for proteinstrukturer, hvor et komplekst a
Livets arkitektur beskrevet ved computermodelleringEn af de enkleste tensegrity -strukturer - tre stive stænger (blå) holdt fast i en stabil konformation af fleksible strenge (sort) - kan også tjene som model for proteinstrukturer, hvor et komplekst a -
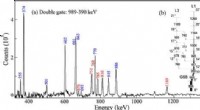 Forskere observerer tværgående slingrende bånd i neodym-136Figur 1. (a) Dobbelt-gatet spektrum på 989- og 390-keV-overgangene, der viser overgangene i bånd L1 og L3. Overgangene af grundtilstandsbåndet og af bånd L1 er angivet med blåt, mens overgangene af bå
Forskere observerer tværgående slingrende bånd i neodym-136Figur 1. (a) Dobbelt-gatet spektrum på 989- og 390-keV-overgangene, der viser overgangene i bånd L1 og L3. Overgangene af grundtilstandsbåndet og af bånd L1 er angivet med blåt, mens overgangene af bå
- Langsomst roterende radiopulsar opdaget af astronomer
- Var Jordens flercellede liv afhængig af pladetektonikken?
- Fremtidig brug af træ sikrer langsigtet klimafordel fra kommercielle skove
- Sort kulstof og anden forurening frø skyer. Var lige begyndt at forstå klimakonsekvenserne
- At finde flydende vand koldeste temperatur og dets særpræg
- Hvordan guldsmede retter sig, når de falder på hovedet


