Hvad er den formelle afgift på bor i BF4?
Bor har et atomnummer på 5, så et neutralt boratom har fem valenselektroner. I BF4 danner bor fire enkeltbindinger med fire fluoratomer. Hver binding repræsenterer to elektroner, der deles mellem bor og fluor, så bor bidrager med i alt 4 elektroner til molekylet.
Ved at bruge den formelle ladningsligning (formel ladning =valenselektroner - ikke-bindende elektroner - 1/2 bindende elektroner), kan vi beregne den formelle ladning på bor i BF4:
Formel ladning på bor =5 - 0 - 4/2
=5 - 0 - 2
=+3
Derfor er den formelle ladning på bor i BF4 +3.
Sidste artikelHvor mange protoner neutroner og elektroner har et menneske?
Næste artikelHvad er de tre orbitaler i et P-underniveau?
 Varme artikler
Varme artikler
-
 Sådan kan en cykel bevæge sig nær lysets hastighed se ud for en menneskelig observatørFigur, der illustrerer deformation af en 2-D cykel med β =0,9 med den stiplede linje, der repræsenterer tværsnittet af y – z-planet. Kredit: Proceedings of the Royal Society A:Matematisk, Fysisk og in
Sådan kan en cykel bevæge sig nær lysets hastighed se ud for en menneskelig observatørFigur, der illustrerer deformation af en 2-D cykel med β =0,9 med den stiplede linje, der repræsenterer tværsnittet af y – z-planet. Kredit: Proceedings of the Royal Society A:Matematisk, Fysisk og in -
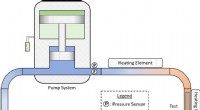 En eksperimentel sløjfe til simulering af atomreaktorer i rummetDen varme brint -testsløjfe, vist i dette diagram, vil cirkulere hydrogengas ved høje temperaturer til materialetest. Kredit:Billede leveret af Will Searight Nuklear termisk fremdrift, som bruger
En eksperimentel sløjfe til simulering af atomreaktorer i rummetDen varme brint -testsløjfe, vist i dette diagram, vil cirkulere hydrogengas ved høje temperaturer til materialetest. Kredit:Billede leveret af Will Searight Nuklear termisk fremdrift, som bruger -
 Fysikere rapporterer lovende tilgang til at udnytte eksotisk elektronisk adfærdMIT-fysikere har fundet ud af, at et moiré-supergitter (billedet til højre) kunne bruges til at udnytte en eksotisk form for elektronisk adfærd. Supergitteret er sammensat af to ark af atomisk tynde l
Fysikere rapporterer lovende tilgang til at udnytte eksotisk elektronisk adfærdMIT-fysikere har fundet ud af, at et moiré-supergitter (billedet til højre) kunne bruges til at udnytte en eksotisk form for elektronisk adfærd. Supergitteret er sammensat af to ark af atomisk tynde l -
 Den dobbelt magiske kerne af bly-208-den snurrer, selvom det ikke burdeEn halvkugle i Gammasfæren, det mest avancerede instrument til påvisning af gammastråler. Kredit:Roy Kaltschmidt, Lawrence Berkeley Lab fotograf Forskere forestiller sig generelt atomkerner er mer
Den dobbelt magiske kerne af bly-208-den snurrer, selvom det ikke burdeEn halvkugle i Gammasfæren, det mest avancerede instrument til påvisning af gammastråler. Kredit:Roy Kaltschmidt, Lawrence Berkeley Lab fotograf Forskere forestiller sig generelt atomkerner er mer
- Ny proces omdanner biomasseaffald til nyttige elektroniske enheder
- Har kommercielle jetfly låse på dørene og tændingsnøgler?
- Ægindustriens miljøaftryk
- Undersøgelse foreslår, hvordan man bygger en bedre 'nanopore' biosensor
- En maskinlæringsbaseret tilgang til at opdage nanokompositfilm til bionedbrydelige plastalternative…
- Forskere finder, hvordan enzymmiljø ændrer hastigheden og retningen af en reaktion


