Er det meste af massen i et atom elektroner?
- Protoner har en positiv ladning og en masse på omkring 1 atommasseenhed (amu).
- Neutroner har ingen ladning og en masse på omkring 1 amu.
- Elektroner har en negativ ladning og en masse på omkring 0,0005 amu.
Til sammenligning måles et atoms masse typisk i dalton (Da) eller atommasseenheder (amu), hvor 1 Da eller 1 amu er omtrent lig med massen af en enkelt proton eller neutron.
Her er et eksempel med kulstof som reference for at illustrere masseforskellen:
- Et kulstofatom har seks protoner, seks neutroner og seks elektroner .
- De seks protoner bidrager med 6 amu til atomets masse.
- De seks neutroner bidrager med yderligere 6 amu.
- De seks elektroner bidrager med ubetydelig 0,003 amu til den samlede masse.
Derfor kommer størstedelen af kulstofmassen (12 amu) fra protonerne og neutronerne i dets kerne, hvor elektronerne bidrager med en meget lille del.
Sammenfattende, mens elektroner spiller en afgørende rolle i atomers kemiske adfærd og egenskaber, bidrager de meget lidt til deres samlede masse.
Sidste artikelHvad er de fem faser af stof eller tilstande stof?
Næste artikelVar teorien korrekt eller forkert?
 Varme artikler
Varme artikler
-
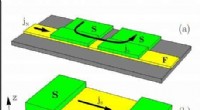 Bevægelige domænevægge inducerer tab i superleder/ferromagnet hybridsystemerJosephson Junction. Kredit:Universitetet i Jyväskylä/ Mihail Silaev Fysikere har vist, at bevægelsen af domænevægge kan detekteres ved at overvåge spænding genereret i superledende enheder. Denn
Bevægelige domænevægge inducerer tab i superleder/ferromagnet hybridsystemerJosephson Junction. Kredit:Universitetet i Jyväskylä/ Mihail Silaev Fysikere har vist, at bevægelsen af domænevægge kan detekteres ved at overvåge spænding genereret i superledende enheder. Denn -
 Selvkørende tankeløse små robotter arbejder sammen om at flytte en korralSamlinger af små, simple bots kan en dag udføre nyttige opgaver som udforskning, så forskere ønsker at lære om deres grundlæggende principper for drift. Kredit:A. Deblais et al., Phys. Lett . (2018)
Selvkørende tankeløse små robotter arbejder sammen om at flytte en korralSamlinger af små, simple bots kan en dag udføre nyttige opgaver som udforskning, så forskere ønsker at lære om deres grundlæggende principper for drift. Kredit:A. Deblais et al., Phys. Lett . (2018) -
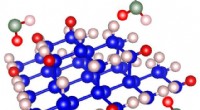 Stærkt beriget:En energieffektiv måde at berige brintisotoper i siliciumSkematisk illustration af hydrogen-til-deuterium-udvekslingsreaktionerne ved en hydrogen-termineret n-Si-overflade i nærværelse af HDO-molekyler (Deuterium:røde kugler, Brint:lyserøde kugler, Ilt:grøn
Stærkt beriget:En energieffektiv måde at berige brintisotoper i siliciumSkematisk illustration af hydrogen-til-deuterium-udvekslingsreaktionerne ved en hydrogen-termineret n-Si-overflade i nærværelse af HDO-molekyler (Deuterium:røde kugler, Brint:lyserøde kugler, Ilt:grøn -
 To-dimensionelle materialer åbner vejen til transistorer med meget lav effekt(a) Graphene på et MX2 -enkeltlag. (b) Typisk båndstruktur med spin-split-bånd med modsat spin-helicitet. (c) Tangentiel vikling af spin-tekstur i regime I og II. (d) Forholdet mellem den statiske mod
To-dimensionelle materialer åbner vejen til transistorer med meget lav effekt(a) Graphene på et MX2 -enkeltlag. (b) Typisk båndstruktur med spin-split-bånd med modsat spin-helicitet. (c) Tangentiel vikling af spin-tekstur i regime I og II. (d) Forholdet mellem den statiske mod
- Hurtigere end lette neutrinoer? Mere som defekte ledninger
- Utrættelige økosystemingeniører eller generende dyr? Beavers' tilstedeværelse mærkes i Boise Ri…
- AMX-30 Main Battle Tank
- Hvad er daglig brug af Eva Ethylene Vinyl Acetate?
- Mens Ian tønder mod Florida, forbereder beboerne sig på orkanhelvede
- Fragmentering af tropiske skove øger de globale udledninger af drivhusgasser


