Hvorfor har FR den største atomradius?
* atomradius Trend: Atomradius øges generelt, når du bevæger dig ned ad en gruppe (kolonne) og falder, når du bevæger dig over en periode (række) i den periodiske tabel.
* Franciums position: Francium er placeret i det nederste venstre hjørne af den periodiske tabel. Dette betyder, at det er i den første gruppe (alkalimetaller) og den syvende periode.
* grunde til stor radius:
* Flere elektronskaller: Når du bevæger dig ned ad en gruppe, får atomer yderligere elektronskaller, hvilket effektivt øger afstanden mellem de yderste elektroner og kernen. Francium har mange elektronskaller.
* afskærmningseffekt: De indre elektroner beskytter de ydre elektroner mod den fulde positive ladning af kernen. Denne afskærmningseffekt er stærkere i francium på grund af dens mange elektronskaller.
* svag nuklear attraktion: Kernen i Francium har et stort antal protoner, men de yderste elektroner er meget langt væk, hvilket reducerer den attraktive kraft.
Kortfattet: Franciums position i nederste venstre hjørne af den periodiske tabel kombineret med dens mange elektronskaller og afskærmningseffekten resulterer i en meget stor atomradius. Det er den største af alle de kendte elementer.
 Varme artikler
Varme artikler
-
 Nuklear - Ude af denne verdenOak Ridge National Laboratory-forskere har udviklet et eksperiment til at teste potentielle materialer til brug i interplanetariske rejser. Eksperimentet udsætter prototypematerialer for temperaturer
Nuklear - Ude af denne verdenOak Ridge National Laboratory-forskere har udviklet et eksperiment til at teste potentielle materialer til brug i interplanetariske rejser. Eksperimentet udsætter prototypematerialer for temperaturer -
 Undersøgelse understøtter standardmodel for partikelfysik, udelukker alternative modellerI denne kunstners repræsentation, en elektron kredser om et atomkerne, snurrer rundt om sin akse, mens en sky af andre subatomære partikler konstant udsendes og reabsorberes. Flere hypoteser forudsige
Undersøgelse understøtter standardmodel for partikelfysik, udelukker alternative modellerI denne kunstners repræsentation, en elektron kredser om et atomkerne, snurrer rundt om sin akse, mens en sky af andre subatomære partikler konstant udsendes og reabsorberes. Flere hypoteser forudsige -
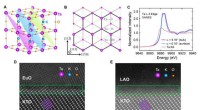 To-dimensionel superledning og anisotrop transport ved kaliumtantalat-grænsefladerSkema af KTO (111) overflade, XANES- og STEM-karakteriseringer. (A) KTaO3 gitterstruktur. De relative størrelser af ionerne er valgt for at understrege Ta-atomerne. De tre tilstødende (111) planer, de
To-dimensionel superledning og anisotrop transport ved kaliumtantalat-grænsefladerSkema af KTO (111) overflade, XANES- og STEM-karakteriseringer. (A) KTaO3 gitterstruktur. De relative størrelser af ionerne er valgt for at understrege Ta-atomerne. De tre tilstødende (111) planer, de -
 Hvordan funktion pludselig kan opstå eller forsvinde i fysiske og biologiske systemerKredit:CC0 Public Domain I fysisk, biologiske og teknologiske systemer, den tid, det tager et systems komponenter at påvirke hinanden, kan påvirke overgangen til synkronisering, en vigtig opdagels
Hvordan funktion pludselig kan opstå eller forsvinde i fysiske og biologiske systemerKredit:CC0 Public Domain I fysisk, biologiske og teknologiske systemer, den tid, det tager et systems komponenter at påvirke hinanden, kan påvirke overgangen til synkronisering, en vigtig opdagels
- NASA ser Tropical Storm Rumbia ud for Chinas østkyst
- Svagt skær i galaksehobe oplyser mørkt stof
- Hvilken metrisk enhed ville du bruge til at måle et glas vand?
- Har Facebook-data hjulpet Trump? Great Hack udforsker skandale
- Rutsjebaneforskning landede, næste flyvning:Månen og Mars
- Er der nogen videnskabelige ord i sjette klasse, der starter med Y?


