Hvordan opfører partiklerne sig i et fast stof?
Nøgleegenskaber ved partikeladfærd i faste stoffer:
* tæt pakket: Partikler i faste stoffer er tæt pakket sammen, ofte i et regelmæssigt, gentagne arrangement kaldet en krystalgitter. Denne ordning er meget stærk og stiv.
* faste positioner: Partikler i faste stoffer holdes i specifikke positioner og vibrerer kun lidt omkring deres faste punkter. De kan ikke bevæge sig frit gennem det faste stof som i væsker eller gasser.
* Stærke intermolekylære kræfter: De attraktive kræfter mellem partikler i faste stoffer er stærke, hvilket holder dem tæt sammen og forhindrer dem i at bevæge sig frit. Disse kræfter kan være ioniske, kovalente, metalliske eller van der Waals kræfter, afhængigt af typen af fast stof.
* Lav kompressibilitet: På grund af den tætte pakning og stærke kræfter er faste stoffer meget vanskelige at komprimere.
* Fast form og volumen: Faststoffer har en bestemt form og volumen, fordi deres partikler er fastgjort i position.
Eksempler:
* is: Vandmolekyler i is er arrangeret i en krystallinsk struktur, med stærke brintbindinger, der holder dem sammen.
* jern: Jernatomer i et metal er arrangeret i en meget tæt, tæt pakket gitter.
* diamant: Carbonatomer i diamant er kovalent bundet i en meget stærk, stiv tetrahedral struktur.
Kortfattet:
Partiklernes opførsel i et fast stof er kendetegnet ved tæt pakning, faste positioner, stærke intermolekylære kræfter, lav kompressibilitet og en bestemt form og volumen. Denne opførsel er ansvarlig for solidens stivhed og modstand mod ændringer i form eller volumen.
Sidste artikelHvordan påvirker massen af et objekt dens inerti?
Næste artikelHvad er lyden af glas, der er målt i decibel?
 Varme artikler
Varme artikler
-
 Forskere demonstrerer, hvordan man styrer flydende krystalmønstreForskning ledet af forskere ved University of Pennsylvania viste, at mønstre på flydende krystaller ikke kun kunne kontrolleres ved nanoskalaer, men ændringerne kunne være synlige uden mikroskoper. Kr
Forskere demonstrerer, hvordan man styrer flydende krystalmønstreForskning ledet af forskere ved University of Pennsylvania viste, at mønstre på flydende krystaller ikke kun kunne kontrolleres ved nanoskalaer, men ændringerne kunne være synlige uden mikroskoper. Kr -
 Ny mikrofluidisk enhed minimerer tab af højværdiprøverAlexandra Ros, professor ved Arizona State Universitys School of Molecular Sciences og Center for Applied Structural Discovery i Biodesign Institute. Kredit:Mary Zhu En stor samarbejdsindsats, der
Ny mikrofluidisk enhed minimerer tab af højværdiprøverAlexandra Ros, professor ved Arizona State Universitys School of Molecular Sciences og Center for Applied Structural Discovery i Biodesign Institute. Kredit:Mary Zhu En stor samarbejdsindsats, der -
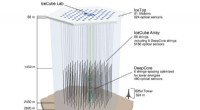 Opgradering af en research IceCubeSensorerne, der registrerer neutrinoer, er fastgjort til strengene, der sænkes ned i isen. Opgraderingen finder sted i Deep Core -området. Kredit:IceCube/NSF IceCube Neutrino Observatory i Antarkt
Opgradering af en research IceCubeSensorerne, der registrerer neutrinoer, er fastgjort til strengene, der sænkes ned i isen. Opgraderingen finder sted i Deep Core -området. Kredit:IceCube/NSF IceCube Neutrino Observatory i Antarkt -
 Ingeniører udvikler usynlighedskappe til højteknologiske behandlingschipsUniversity of Utah, lektor for elektrisk og computeringeniør Rajesh Menon (billedet) og hans team har udviklet en tilsløringsenhed til mikroskopiske fotoniske integrerede enheder - byggestenene i foto
Ingeniører udvikler usynlighedskappe til højteknologiske behandlingschipsUniversity of Utah, lektor for elektrisk og computeringeniør Rajesh Menon (billedet) og hans team har udviklet en tilsløringsenhed til mikroskopiske fotoniske integrerede enheder - byggestenene i foto
- Skiftende ledningstilstand - et skridt mod topologiske transistorer
- Hvor de hawaiianske øer dannet af jordskælv eller vulkaner?
- Vask genstridige biofilm væk ved hjælp af svampe rengøringsmidler
- Hvilken mængde affald:Ny undersøgelse viser, at britisk affald er domineret af plastik og drikkeva…
- Nogle køkkenskabe kan afgive potentielt skadelige forbindelser
- Forårsager tyngdekraften bølger og strømme?


