Hvad er vibrations- og roterende kvantetal?
vibrations- og rotations kvantetal:en hurtig forklaring
vibrations kvantenummer (v)
* hvad det beskriver: Det vibrationsenerginiveau af et molekyle.
* Værdier: 0, 1, 2, 3 ... (heltal)
* Betydning:
* V =0:Molekylet er i sin jordvibrationstilstand (laveste energi).
* V =1:Molekylet er i sin første ophidsede vibrationstilstand (et kvante energi højere end jordtilstanden).
* V =2:Molekylet er i sin anden ophidsede vibrationstilstand (to kvante energi højere end jordtilstanden) og så videre.
* Analogi: Forestil dig en bold på en forår. Forskellige vibrationstilstande svarer til forskellige mængder energi, der er gemt i strækningen og komprimeringen af foråret.
Rotations kvantenummer (J)
* hvad det beskriver: Det rotations energiniveau af et molekyle.
* Værdier: 0, 1, 2, 3 ... (heltal)
* Betydning:
* J =0:Molekylet roterer ikke.
* J =1:Molekylet roterer ved den lavest mulige rotationsenergi.
* J =2:Molekylet roterer på et højere energiniveau og så videre.
* Analogi: Forestil dig en spinding top. Forskellige rotationstilstande svarer til forskellige rotationshastigheder.
Nøglepunkter:
* Både vibrations- og rotationsenerginiveau er kvantiseret, hvilket betyder, at de kun kan eksistere ved diskrete værdier.
* Molekyler kan skifte mellem vibrations- og rotationstilstande ved at absorbere eller udsende fotoner af lys.
* Disse overgange observeres i spektroskopi, hvilket giver information om molekylernes struktur og dynamik.
Eksempel:
Overvej et diatomisk molekyle som CO. Dens vibrations- og rotationsenerginiveau kan afbildes som følger:
* vibration: Hvert vibrationsniveau har flere rotationsniveauer forbundet med det.
* Rotation: Inden for hvert vibrationsniveau kan molekylet rotere i forskellige hastigheder, svarende til forskellige rotations kvantetal.
Kortfattet: Vibrations- og roterende kvantetal er grundlæggende begreber i molekylær spektroskopi, hvilket giver værdifuld indsigt i strukturen, bevægelsen og energiniveauet for molekyler.
 Varme artikler
Varme artikler
-
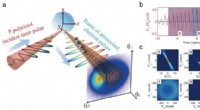 Forskere demonstrerer laser direkte kortlægning af attosekunds elektrondynamikFigur (a) laserkortlægning af attosekunds elektrondynamik (b) faserum og vinkelfordelinger (c) af elektroner udsendt fra et plasmaspejl med forskellige ejektionstider i forhold til toppen af den ref
Forskere demonstrerer laser direkte kortlægning af attosekunds elektrondynamikFigur (a) laserkortlægning af attosekunds elektrondynamik (b) faserum og vinkelfordelinger (c) af elektroner udsendt fra et plasmaspejl med forskellige ejektionstider i forhold til toppen af den ref -
 Billedteknik låser hemmelighederne op for kunstnere fra 1600 -talletGeorgia Tech -professor David Citrin vises med billeder produceret af en terahertz -billeddannelsesteknik. Forskere studerede et maleri fra 1600 -tallet ved hjælp af en terahertz reflektometri -teknik
Billedteknik låser hemmelighederne op for kunstnere fra 1600 -talletGeorgia Tech -professor David Citrin vises med billeder produceret af en terahertz -billeddannelsesteknik. Forskere studerede et maleri fra 1600 -tallet ved hjælp af en terahertz reflektometri -teknik -
 Ny neutronkilde i Canada ville anspore innovation, medicinske behandlingerNeutroner har mange anvendelser inden for videnskabelig og medicinsk forskning. Kredit:Shutterstock Teknologiske fremskridt skyldes meget vores videnskabelige forståelse af de materialer, vi bruge
Ny neutronkilde i Canada ville anspore innovation, medicinske behandlingerNeutroner har mange anvendelser inden for videnskabelig og medicinsk forskning. Kredit:Shutterstock Teknologiske fremskridt skyldes meget vores videnskabelige forståelse af de materialer, vi bruge -
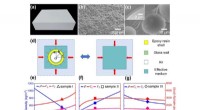 Akustikforskere udvikler en ny undervands-tæppekappeFig. 1 Karakterisering af det syntaktiske skum. Kredit:IACAS Akustisk camouflage, realiseret ved at kontrollere bølgeudbredelsen, har tiltrukket sig stor opmærksomhed i de senere år. Hjælpet af en
Akustikforskere udvikler en ny undervands-tæppekappeFig. 1 Karakterisering af det syntaktiske skum. Kredit:IACAS Akustisk camouflage, realiseret ved at kontrollere bølgeudbredelsen, har tiltrukket sig stor opmærksomhed i de senere år. Hjælpet af en
- Hvor mange flydende kombinationer kan du lave?
- Lukning af fossile kraftværker kan koste mindre end forventet
- Hvilke celler fungerer med røde blodlegemer?
- Sådan slettes matricer på en TI-84
- Sådan beregnes metriske konverteringer
- Op til halvdelen af Holocaust-relateret indhold på Telegram benægter eller fordrejer fakta


