Hvordan er bevægelserne af partikler, der er forskellig mellem statssager?
solid:
* Partikelarrangement: Partikler i et fast stof er tæt pakket sammen i et regelmæssigt, gentagne mønster (et krystalgitter).
* Bevægelse: Partikler vibrerer i faste positioner med kun begrænset bevægelse. De har lav kinetisk energi.
* Form og volumen: Faststoffer har en bestemt form og volumen, fordi partiklerne er fastgjort i deres positioner.
væske:
* Partikelarrangement: Partikler i en væske er tættere sammen end i en gas, men ikke så tæt pakket eller bestilt som i et fast stof. De kan bevæge sig rundt i hinanden.
* Bevægelse: Partikler i en væske bevæger sig mere frit end i et fast stof, men de er stadig relativt tæt sammen. De har højere kinetisk energi end faste stoffer.
* Form og volumen: Væsker har et bestemt volumen, men tager formen på deres beholder, fordi partiklerne kan bevæge sig rundt og flyde.
gas:
* Partikelarrangement: Partikler i en gas er langt fra hinanden og bevæger sig tilfældigt i alle retninger. Der er ingen fast arrangement.
* Bevægelse: Partikler i en gas har den højeste kinetiske energi. De bevæger sig meget hurtigt og kolliderer ofte med hinanden og væggene i deres beholder.
* Form og volumen: Gasser har ingen bestemt form eller volumen, der tager form og volumen på deres beholder, fordi partiklerne bevæger sig frit.
plasma:
* Partikelarrangement: Svarende til en gas, men med et stort antal ioner og frie elektroner.
* Bevægelse: Partikler i en plasma bevæger sig meget hurtigt og kolliderer ofte. De har endnu højere kinetisk energi end gasser, med nogle partikler, der endda ioniserer andre partikler.
* Form og volumen: Som en gas har plasma ingen bestemt form eller volumen.
Kortfattet:
* faste stoffer: Partikler vibrerer i faste positioner med lav kinetisk energi.
* væsker: Partikler bevæger sig rundt med hinanden med højere kinetisk energi end faste stoffer.
* Gasser: Partikler bevæger sig tilfældigt og frit med meget høj kinetisk energi.
* plasma: Svarende til en gas, men med ioniserede partikler og endnu højere kinetisk energi.
Forskellene i partikelbevægelse er grunden til, at tilstandene af stof har forskellige egenskaber.
 Varme artikler
Varme artikler
-
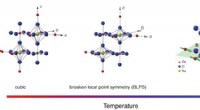 Forskning afslører ny kvantetilstand i mærkelige isolerende materialerNår en Mott-isolator med stærk spin-order-kobling afkøles, dets atomgitter forvrænger, bryde dens kubiske symmetri. Denne forvrængning driver en unik form for lagdelt magnetisme i materialerne. Kredit
Forskning afslører ny kvantetilstand i mærkelige isolerende materialerNår en Mott-isolator med stærk spin-order-kobling afkøles, dets atomgitter forvrænger, bryde dens kubiske symmetri. Denne forvrængning driver en unik form for lagdelt magnetisme i materialerne. Kredit -
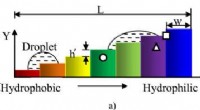 Selv dråber tager nogle gange trappen(a) Skematisk fremstilling af simuleringsdomænet for en dråbe, der klatrer på de trinvise overflader under påvirkning af differentiel befugtning, O:efterfølgende trin, Δ:førende trin, og □:trin på fod
Selv dråber tager nogle gange trappen(a) Skematisk fremstilling af simuleringsdomænet for en dråbe, der klatrer på de trinvise overflader under påvirkning af differentiel befugtning, O:efterfølgende trin, Δ:førende trin, og □:trin på fod -
 Forskere tættere på at forklare, hvorfor stof fortsætter over antistofInde i Super-Kamiokande neutrino detektoren. Kredit:Imperial College London Nye resultater viser en forskel i den måde neutrinoer og antineutrinoer opfører sig på, som kunne hjælpe med at forklare
Forskere tættere på at forklare, hvorfor stof fortsætter over antistofInde i Super-Kamiokande neutrino detektoren. Kredit:Imperial College London Nye resultater viser en forskel i den måde neutrinoer og antineutrinoer opfører sig på, som kunne hjælpe med at forklare -
 Kan du virkelig knuse et glas med en høj seddel?Hvis betingelserne er de rigtige, det er muligt at knuse glas med den menneskelige stemme. Purestock/Thinkstock Det er operaens ækvivalent til scenen med slip-on-the-banan-skrællen:Sopranen på scenen
Kan du virkelig knuse et glas med en høj seddel?Hvis betingelserne er de rigtige, det er muligt at knuse glas med den menneskelige stemme. Purestock/Thinkstock Det er operaens ækvivalent til scenen med slip-on-the-banan-skrællen:Sopranen på scenen
- Er Thorium-234 Proactinium-234 -1 en alfa-henfaldsligning?
- Elektronisk luftrensningsteknologi kan generere utilsigtede forurenende stoffer
- Golfstrømmens indtrængen føder kiselalger-hot spots
- Fragmenter af Dødehavsrulle, der menes at være tomme, afslører tekst
- 3 udbrud af Alaska-vulkaner, der spytter lava- eller askeskyer
- Hvad sker der med månemodulerne i rummet?


