Hvad er den gennemsnitlige hastighed af atomer i 2,00 mol neon ved 308 K?
1. Forstå konceptet
Den gennemsnitlige hastighed for gaspartikler er relateret til deres kinetiske energi, som er direkte proportional med temperaturen. Vi kan bruge rod-middel-kvadratet (RMS) hastighed til at repræsentere denne gennemsnitlige hastighed.
2. Formel
RMS -hastigheden (v rms ) er givet af:
v rms =√ (3RT/M)
hvor:
* R er den ideelle gaskonstant (8.314 j/mol · k)
* T er temperaturen i Kelvin
* M er den molære masse af gassen i kg/mol
3. Beregn den molære masse af neon
Neon har en atommasse på ca. 20,18 g/mol. Konverter dette til kg/mol:
M =20,18 g/mol * (1 kg/1000 g) =0,02018 kg/mol
4. Tilslut værdierne
v rms =√ (3 * 8.314 J/mol · K * 308 K/0,02018 kg/mol)
5. Beregn resultatet
v rms ≈ 517 m/s
Derfor er den gennemsnitlige hastighed af neonatomer i 2,00 mol neon ved 308 K ca. 517 m/s.
Vigtig note: Antallet af mol (2,00 mol) påvirker ikke den gennemsnitlige hastighed. RMS -hastigheden afhænger kun af temperaturen og den molære masse af gassen.
Sidste artikelHvad er en singlet i kvantefysik?
Næste artikelEt materiale, der reflekterer eller absorberer alle de lette strejker, er det?
 Varme artikler
Varme artikler
-
 Afslutter på Higgs,Seks år senere Dette funky billede viser Compact Muon Solenoid (CMS), en generel detektor ved Large Hadron Collider (LHC), der var involveret i opdagelsen af Higgs i 2012. Dean Mouhtaropoulo
Afslutter på Higgs,Seks år senere Dette funky billede viser Compact Muon Solenoid (CMS), en generel detektor ved Large Hadron Collider (LHC), der var involveret i opdagelsen af Higgs i 2012. Dean Mouhtaropoulo -
 Lavt tab, all-fiber system til stærk og effektiv kobling mellem fjerne atomerEksperimentel enhed til en fiber, koblet hulrum-QED-system. Kredit:Aoki Laboratory, Waseda Universitet Et team af forskere fra Waseda University, Japan Science and Technology Agency, og University
Lavt tab, all-fiber system til stærk og effektiv kobling mellem fjerne atomerEksperimentel enhed til en fiber, koblet hulrum-QED-system. Kredit:Aoki Laboratory, Waseda Universitet Et team af forskere fra Waseda University, Japan Science and Technology Agency, og University -
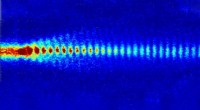 Awake-konceptet bringer protonbundter i synkroniseringEt tog af korte protonbundter rejser gennem plasmafeltet, danner en bølge, hvorpå elektroner kan accelereres. Kredit:VÅGEN Fremtiden for partikelacceleration er begyndt. Awake er et lovende koncep
Awake-konceptet bringer protonbundter i synkroniseringEt tog af korte protonbundter rejser gennem plasmafeltet, danner en bølge, hvorpå elektroner kan accelereres. Kredit:VÅGEN Fremtiden for partikelacceleration er begyndt. Awake er et lovende koncep -
 Hvad er en bølgelængde?En bølge er lavet af rejsenergi. Overvej bølgerne i en swimmingpool:Hvis du hopper i vandet, bølger rejser fra stedet, hvor du rammer til den anden side af poolen. Disse bølger er et resultat af energ
Hvad er en bølgelængde?En bølge er lavet af rejsenergi. Overvej bølgerne i en swimmingpool:Hvis du hopper i vandet, bølger rejser fra stedet, hvor du rammer til den anden side af poolen. Disse bølger er et resultat af energ


