Hvordan ændres bevægelsen af partikler i stof, når der tilsættes varme?
Den grundlæggende idé:
* varme er energi. Når du tilføjer varme til stof, giver du i det væsentlige dens partikler mere energi.
* mere energi betyder mere bevægelse. Denne energi manifesterer sig som øget bevægelse af partiklerne.
hvordan det påvirker forskellige stofstater:
* faste stoffer: I faste stoffer er partikler tæt pakket og vibrerer i faste positioner. Tilsætning af varme får dem til at vibrere hurtigere og med større amplitude. Denne øgede vibration kan føre til udvidelse af det faste stof.
* væsker: I væsker er partikler mere løst pakket og kan bevæge sig rundt i hinanden. Tilføjelse af varme øger hastigheden og fri bevægelighed for de flydende partikler. Dette fører til øget fluiditet og ekspansion.
* Gasser: Gaspartikler har mest bevægelsesfrihed. De bevæger sig hurtigt og kolliderer med hinanden og containervæggene. Tilsætning af varme øger hastigheden og kraft af disse kollisioner, hvilket fører til øget tryk og ekspansion.
Et nøglekoncept:Faseændringer
Tilføjelse af nok varme kan få et stof til at ændre tilstand:
* fast til væske (smeltning): Når der tilsættes varme til et fast stof, vibrerer partiklerne hurtigere og overvinder kræfterne, der holder dem i en fast position. Dette får det faste stof til at smelte i en væske.
* væske til gas (kogning/fordampning): Når der tilsættes varme til en væske, bevæger partiklerne sig hurtigere og har til sidst nok energi til at bryde fri fra væskens overflade og blive en gas.
Kortfattet
Varme er nøglen til at øge partikelbevægelsen i stof. Denne bevægelse kan føre til ekspansion, øget fluiditet og endda ændringer i selve stoffer.
 Varme artikler
Varme artikler
-
 At finde flydende vand koldeste temperatur og dets særprægKredit:George Hodan/public domain To forskergrupper, der arbejder uafhængigt af hinanden, har opdaget nogle bemærkelsesværdige træk ved flydende vand - det kan afkøles til -42,55 ° C, og det ser u
At finde flydende vand koldeste temperatur og dets særprægKredit:George Hodan/public domain To forskergrupper, der arbejder uafhængigt af hinanden, har opdaget nogle bemærkelsesværdige træk ved flydende vand - det kan afkøles til -42,55 ° C, og det ser u -
 Hvad er terpener, og kan de gavne dit helbred?Et hætteglas med terpener, som er aromatiske organiske forbindelser, der for det meste findes i planter og bruges i produkter som f.eks. insektmiddel, maling, opløsningsmidler, lægemidler, husholdning
Hvad er terpener, og kan de gavne dit helbred?Et hætteglas med terpener, som er aromatiske organiske forbindelser, der for det meste findes i planter og bruges i produkter som f.eks. insektmiddel, maling, opløsningsmidler, lægemidler, husholdning -
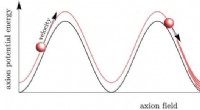 Sag for axion-oprindelse af mørkt stof vinder trækkraftAksionsfeltet løber hurtigt over de potentielle barrierer og begynder til sidst svingninger, når de bremses tilstrækkeligt af friktion. Kredit:Co &Harigaya I en ny undersøgelse af aksionsbevægelse
Sag for axion-oprindelse af mørkt stof vinder trækkraftAksionsfeltet løber hurtigt over de potentielle barrierer og begynder til sidst svingninger, når de bremses tilstrækkeligt af friktion. Kredit:Co &Harigaya I en ny undersøgelse af aksionsbevægelse -
 Hvad er en monomer?En elementær studerende undersøger en molekylær model. Hero Images/Getty Images For at forstå en monomer, billede et sæt perler lavet til et meget lille barn, designet til at hænge sammen. Hver enkel
Hvad er en monomer?En elementær studerende undersøger en molekylær model. Hero Images/Getty Images For at forstå en monomer, billede et sæt perler lavet til et meget lille barn, designet til at hænge sammen. Hver enkel
- Hvordan en global havtraktat kunne beskytte biodiversiteten i det åbne hav
- Hvordan ultratynde polymerfilm kan bruges til opbevaringsteknologi
- Hvad er forholdet mellem masseafstand og gravitationskraft?
- Evidence of Evolution: Origin of Plants, Animals & Fungi
- Hvorfor magneter ikke placeret i nærheden af mobiltelefoner?
- Nye undersøgelsesresultater stemmer overens med hunde-tæmning under istiden


