Hvad er kraften til attraktion på væsker?
Her er en sammenbrud:
interne kræfter:
* samhørighed: Dette er tiltrækningen mellem molekyler af den samme væske . Jo stærkere de sammenhængende kræfter, jo højere er overfladespændingen og jo mere resistente væsken er til at flyde eller sprede sig. Det er det, der får vanddråber til at danne kugler.
* Adhæsion: Dette er tiltrækningen mellem molekyler af væske og molekyler af et andet stof . Dette er grunden til, at vandet vugger glas (vedhæftning er stærkere end samhørighed), men ikke voksen (samhørighed er stærkere end vedhæftning).
eksterne kræfter:
* tyngdekraft: Denne kraft trækker væsken nedad og får den til at flyde og akkumuleres i bunden af en beholder.
* tryk: Denne kraft kan påføres fra det omgivende miljø eller af andre genstande, der påvirker væskens strømning og form.
Andre kræfter:
* Intermolekylære kræfter: Dette er kræfterne til tiltrækning mellem molekyler, der inkluderer van der Waals-kræfter, hydrogenbinding og dipol-dipolinteraktioner. Disse kræfter bidrager væsentligt til de sammenhængende og klæbende egenskaber ved væsker.
Det er vigtigt at bemærke:
* Styrken af disse kræfter varierer mellem forskellige væsker, hvilket forklarer, hvorfor nogle væsker er mere viskøse (som honning), mens andre er mere flydende (som vand).
* Kræfterne interagerer konstant og påvirker hinanden, hvilket gør væskernes opførsel ganske kompleks.
Så der er ikke kun en "tiltrækningskraft" på væsker. Det er en kombination af flere kræfter, der virker på én gang, hvilket skaber de unikke egenskaber og adfærd, vi observerer i væsker.
Sidste artikelKraften, der trækker vand op i smalle rør mod tyngdekraften, er en?
Næste artikelHvad er elektromagnetisk fysik?
 Varme artikler
Varme artikler
-
 Forskere udvikler en indstillelig bio-billeddannelsesenhed ved hjælp af terahertz plasmonik(a) Et fotografi af spiral Bulls eye (SBE) struktur, (b) et mikroskopbillede af de dobbeltbølgede bølger og (c) et scanningselektronmikroskopbillede af den otte-tipede Siemens-stjerneåbning i midten a
Forskere udvikler en indstillelig bio-billeddannelsesenhed ved hjælp af terahertz plasmonik(a) Et fotografi af spiral Bulls eye (SBE) struktur, (b) et mikroskopbillede af de dobbeltbølgede bølger og (c) et scanningselektronmikroskopbillede af den otte-tipede Siemens-stjerneåbning i midten a -
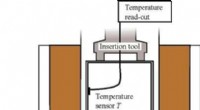 Biopsi frosset på få sekunder på operationsstuenSkematisk oversigt over det nye fryseapparat, med vævets indføringspunkt, varmebuffer, kryokøler og gasforsyning. Kredit:University of Twente Til hurtig nedfrysning af en biopsiprøve taget fra en
Biopsi frosset på få sekunder på operationsstuenSkematisk oversigt over det nye fryseapparat, med vævets indføringspunkt, varmebuffer, kryokøler og gasforsyning. Kredit:University of Twente Til hurtig nedfrysning af en biopsiprøve taget fra en -
 Partikler med øjne giver et nærmere kig på rotationsdynamikkenKredit:University of Tokyo Kolloider - blandinger af partikler fremstillet af et stof, spredt i et andet stof - dukker op på mange områder i hverdagen, herunder kosmetik, mad og farvestoffer, og d
Partikler med øjne giver et nærmere kig på rotationsdynamikkenKredit:University of Tokyo Kolloider - blandinger af partikler fremstillet af et stof, spredt i et andet stof - dukker op på mange områder i hverdagen, herunder kosmetik, mad og farvestoffer, og d -
 Et meget specielt løb for LHCb-eksperimentetLHCb -detektoren i åben konfiguration. Kredit:Anna Pantelia/CERN For første gang, LHCb-eksperimentet på CERN har indsamlet data samtidigt i collider og i fast-target-tilstande. Med dette, LHCb -sp
Et meget specielt løb for LHCb-eksperimentetLHCb -detektoren i åben konfiguration. Kredit:Anna Pantelia/CERN For første gang, LHCb-eksperimentet på CERN har indsamlet data samtidigt i collider og i fast-target-tilstande. Med dette, LHCb -sp
- Undersøgelse viser, at luftbårne partikler også er forurenet med tobaksrøgdrevne partikler
- Hvad sker der med et forslag, når 2 lige kræfter handler på objekt i modsatte retninger?
- Mens olie og dødt dyreliv skyller op, søger Californien en stopper for offshore-boringer. Hvorfor …
- Hvorfor kaldes Terai Granary of Nepal?
- Hvad var bidrag til atomet?
- Hvilke forbindelser elueres først i ikke -polær GC -søjle?


