Hvad er et resultat af interne bevægelsespartikler noget?
1. Temperatur:
* direkte relateret til gennemsnitlig kinetisk energi: Jo hurtigere partiklerne bevæger sig, jo højere er temperaturen.
* termisk energi: Den interne energi af et stof på grund af bevægelsen af dets partikler.
2. Stater med stof:
* faste stoffer: Partikler vibrerer i faste positioner, hvilket resulterer i en stiv struktur.
* væsker: Partikler bevæger sig mere frit, så de kan flyde og tage formen på deres beholder.
* Gasser: Partikler bevæger sig meget hurtigt og uafhængigt og fylder hele volumen på deres beholder.
3. Varmeoverførsel:
* ledning: Varmeoverførsel gennem direkte kontakt med partikler.
* konvektion: Varmeoverførsel gennem bevægelse af væsker (væsker og gasser).
* Stråling: Varmeoverførsel gennem elektromagnetiske bølger.
4. Udvidelse og sammentrækning:
* termisk ekspansion: Materialet udvides, når den opvarmes på grund af øget partikelbevægelse.
* termisk sammentrækning: Materiale -kontrakter, når de afkøles på grund af nedsat partikelbevægelse.
5. Tryk:
* gastryk: Kollisioner af gaspartikler mod væggene i en beholder skaber tryk.
* Fluidtryk: Tryk inden for en væske er relateret til vægten af væsken over et givet punkt.
6. Diffusion:
* Blanding af stoffer: Partikler fra regioner med høj koncentration flytter til regioner med lav koncentration, hvilket til sidst fører til en ensartet blanding.
7. Kemiske reaktioner:
* Aktiveringsenergi: Intern bevægelse giver energi til partikler til at overvinde energibarrieren og deltage i kemiske reaktioner.
* reaktionshastigheder: Hastigheden af kemiske reaktioner påvirkes af temperaturen, hvilket påvirker hastigheden for partikelkollisioner og den tilgængelige energi til reaktioner.
Dette er kun et par eksempler på de forskellige effekter af intern bevægelse i stof. At forstå disse fænomener er afgørende inden for forskellige områder, herunder fysik, kemi, teknik og materialevidenskab.
 Varme artikler
Varme artikler
-
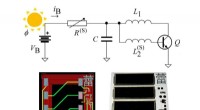 Mange knopper til at blomstre:En synkroniseringsmetode til sansning ved hjælp af mange oscillatorerHver sensorknude består af et kredsløb, der kun består af en fotovoltaisk kilde, en variabel modstand, en kondensator, to induktorer og en bipolar transistor (øverst). En induktor realiseres som et tr
Mange knopper til at blomstre:En synkroniseringsmetode til sansning ved hjælp af mange oscillatorerHver sensorknude består af et kredsløb, der kun består af en fotovoltaisk kilde, en variabel modstand, en kondensator, to induktorer og en bipolar transistor (øverst). En induktor realiseres som et tr -
 Hvad sker der egentlig ved femtosekundskryds?Dr. Tomasz Kardas fra Laser Center ved Institute of Physical Chemistry ved det polske videnskabsakademi og det fysiske fakultet, Universitetet i Warszawa, på en festlig måde visualiserer strålerne af
Hvad sker der egentlig ved femtosekundskryds?Dr. Tomasz Kardas fra Laser Center ved Institute of Physical Chemistry ved det polske videnskabsakademi og det fysiske fakultet, Universitetet i Warszawa, på en festlig måde visualiserer strålerne af -
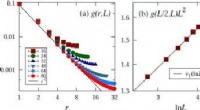 Nyt fysisk billede fører til en præcis skalering af (3+1) -dimensionalt O (n) kritisk systemBevis for den formodede skaleringsform i eksemplet med den kritiske 4D XY -model. (a) To-punkts korrelationsfunktion. (b) To-punkts korrelation ved afstanden til halvdelen af den lineære systemstørr
Nyt fysisk billede fører til en præcis skalering af (3+1) -dimensionalt O (n) kritisk systemBevis for den formodede skaleringsform i eksemplet med den kritiske 4D XY -model. (a) To-punkts korrelationsfunktion. (b) To-punkts korrelation ved afstanden til halvdelen af den lineære systemstørr -
 Let kerne forudsagde at være stabil på trods af at have to mærkelige kvarkerEn kunstners indtryk af en bundet kerne indeholdende tre normale nukleoner, som har op og ned kvarker, og en Xi-hyperon (guldkugle nederst til højre), som indeholder to mærkelige kvarker. Beregninger
Let kerne forudsagde at være stabil på trods af at have to mærkelige kvarkerEn kunstners indtryk af en bundet kerne indeholdende tre normale nukleoner, som har op og ned kvarker, og en Xi-hyperon (guldkugle nederst til højre), som indeholder to mærkelige kvarker. Beregninger
- Smarte polymerer omdanner elektrisk energi til mekanisk arbejde
- Hvorfor har dyrecellemembraner forskellige former og derefter plantemembraner?
- Europas direktiv om vedvarende energi er klar til at skade globale skove
- Problemet med afskaffelse af fængsler? misforstå det
- Hvad er de fysiske egenskaber ved aloe?
- Hvordan blev Mount Shasta og Lassen Peak dannet?


