Hvilke måler den gennemsnitlige hastighed for luftmolekyler?
Her er hvorfor:
* kinetisk teori om gasser: Denne teori siger, at temperaturen på en gas er direkte proportional med den gennemsnitlige kinetiske energi af dens molekyler.
* kinetisk energi: Kinetisk energi er bevægelsesenergien. Jo hurtigere molekyler bevæger sig, jo højere er deres kinetiske energi.
* Temperatur og hastighed: Derfor betyder en højere temperatur, at molekylerne i gennemsnit bevæger sig hurtigere, hvilket resulterer i en højere gennemsnitlig hastighed.
Bemærk: Mens temperaturen er den primære foranstaltning, er der andre relaterede koncepter:
* rod-middel-kvadrathastighed (RMS-hastighed): Dette er en specifik beregning, der tager højde for fordelingen af hastigheder inden for gassen. Det er et mere præcist mål for gennemsnitshastigheden, men temperaturen giver stadig en generel indikation.
* Gennemsnitlig hastighed: Dette er et andet mål for gennemsnitlig hastighed, men det er mindre nøjagtigt end RMS -hastighed, fordi det ikke tager højde for fordelingen af hastigheder også.
Fortæl mig, hvis du gerne vil have flere detaljer om nogen af disse koncepter!
 Varme artikler
Varme artikler
-
 Kvantemekanik kunne forklare, hvorfor DNA spontant kan mutere3D-model af DNA. Kredit:Michael Ströck/Wikimedia/GNU Free Documentation License Livets molekyler, DNA, replikerer med forbløffende præcision, men denne proces er ikke immun over for fejl og kan før
Kvantemekanik kunne forklare, hvorfor DNA spontant kan mutere3D-model af DNA. Kredit:Michael Ströck/Wikimedia/GNU Free Documentation License Livets molekyler, DNA, replikerer med forbløffende præcision, men denne proces er ikke immun over for fejl og kan før -
 En ramme til at simulere den samme fysik ved hjælp af to forskellige HamiltonianereTroskab mellem kvantetilstande genereret af enakset vridende Hamiltonian og tilstande genereret af Heisenberg XXX-modellen med forskudt felt. Kredit:Gietka et al. Forskere ved Okinawa Institute of
En ramme til at simulere den samme fysik ved hjælp af to forskellige HamiltonianereTroskab mellem kvantetilstande genereret af enakset vridende Hamiltonian og tilstande genereret af Heisenberg XXX-modellen med forskudt felt. Kredit:Gietka et al. Forskere ved Okinawa Institute of -
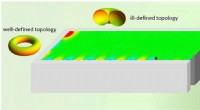 At standse en bølge i dens sporI et system med en dårligt defineret topologi kan antallet af kantbølger, der udbreder sig indad til et eller andet samlingspunkt, være forskelligt fra antallet af kantbølger, der udbreder sig i udadg
At standse en bølge i dens sporI et system med en dårligt defineret topologi kan antallet af kantbølger, der udbreder sig indad til et eller andet samlingspunkt, være forskelligt fra antallet af kantbølger, der udbreder sig i udadg -
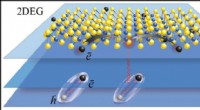 Ny mekanisme for elektronspredning i grafenlignende 2-D-materialerHybridsystem dannet ved at kombinere Bose-Einstein-kondensat (BEC) og 2D-elektrongas (2DEG) i nye 2D-materialer, såsom MoS2. Elektroner (sorte kugler) bevæger sig i 2D elektrongas (2DEG, øverste lag),
Ny mekanisme for elektronspredning i grafenlignende 2-D-materialerHybridsystem dannet ved at kombinere Bose-Einstein-kondensat (BEC) og 2D-elektrongas (2DEG) i nye 2D-materialer, såsom MoS2. Elektroner (sorte kugler) bevæger sig i 2D elektrongas (2DEG, øverste lag),


