Hvad er styrken af tiltrækning mellem partikler i et fast stof?
Her er en sammenbrud:
* Stærke intermolekylære kræfter: Partiklerne i et fast stof holdes sammen af stærke intermolekylære kræfter, såsom ioniske bindinger, kovalente bindinger eller metalliske bindinger.
* Lukkethed: Partiklerne pakkes tæt sammen og minimerer rummet mellem dem.
* Begrænset bevægelse: Partiklerne kan kun vibrere i deres faste positioner med meget begrænset bevægelse.
styrken af disse attraktioner varierer afhængigt af typen af fast stof:
* ioniske faste stoffer: Disse har stærke elektrostatiske attraktioner mellem modsat ladede ioner, hvilket resulterer i høje smeltepunkter og hårdhed.
* kovalente netværksstoffer: Disse holdes sammen af stærke kovalente bindinger og danner et kæmpe netværk af atomer. De er ekstremt hårde og har meget høje smeltepunkter (f.eks. Diamond).
* Metalliske faste stoffer: Disse har et "hav af elektroner", der holder metalatomerne sammen, hvilket resulterer i høj elektrisk ledningsevne og formbarhed.
I modsætning til faste stoffer har væsker svagere intermolekylære kræfter, hvilket gør det muligt for partikler at bevæge sig mere frit. Gasser har de svageste intermolekylære kræfter, med partikler bevæger sig frit og tilfældigt.
 Varme artikler
Varme artikler
-
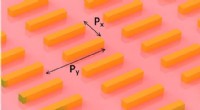 En ny lov for metamaterialerEn ny skalalov afdækker fysikken bag metamaterialers kollektive termiske emissionsadfærd. Kredit:College of Engineering, Carnegie Mellon University Metamaterialer, som er konstrueret til at have e
En ny lov for metamaterialerEn ny skalalov afdækker fysikken bag metamaterialers kollektive termiske emissionsadfærd. Kredit:College of Engineering, Carnegie Mellon University Metamaterialer, som er konstrueret til at have e -
 Forskere tager højhastighedsvideo af bølger for bedre at forstå havsprøjtKredit:CC0 Public Domain Bølger, der styrter på kyster, genererer små vanddråber kendt som havsprøjt. Havspray flytter varme og vand fra havet til atmosfæren, men forskere er usikre på, hvilken de
Forskere tager højhastighedsvideo af bølger for bedre at forstå havsprøjtKredit:CC0 Public Domain Bølger, der styrter på kyster, genererer små vanddråber kendt som havsprøjt. Havspray flytter varme og vand fra havet til atmosfæren, men forskere er usikre på, hvilken de -
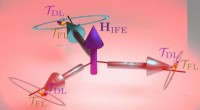 En forsømt mekanisme i antiferromagneter kan være nøglen til spintronicsOptiske laserpulser genererer to typer moment, feltlignende (? FL) og dæmpningslignende (? DL), der påvirker de tre magnetiseringer af YMnO3. Det dæmpningslignende drejningsmoment har en udtalt effekt
En forsømt mekanisme i antiferromagneter kan være nøglen til spintronicsOptiske laserpulser genererer to typer moment, feltlignende (? FL) og dæmpningslignende (? DL), der påvirker de tre magnetiseringer af YMnO3. Det dæmpningslignende drejningsmoment har en udtalt effekt -
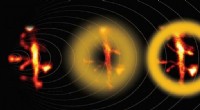 Ny kalibreringsprocedure til superopløselig hjernebilleddannelseMulti-foton STED-mikroskopi forbedret med adaptiv optik fanger de fine detaljer i neuronale dendritter. Kredit:Bancelin et al. Lys - og alle bølger - kan bøje rundt om hjørnerne af forhindringer,
Ny kalibreringsprocedure til superopløselig hjernebilleddannelseMulti-foton STED-mikroskopi forbedret med adaptiv optik fanger de fine detaljer i neuronale dendritter. Kredit:Bancelin et al. Lys - og alle bølger - kan bøje rundt om hjørnerne af forhindringer,
- Hvordan tilføjer du energi og stof?
- Hvordan dannes en anticline -bjerg?
- Skotland siger nej til fracking
- Sabeltandede katte med mundskader spiste blødere mad end deres uskadte modstykker
- Sådan finder du en Equivalence Point Titration
- Hvilke to former for energi er mest anvendt i Canada giver et eksempel på, hvordan hver form bruges…


