Den gennemsnitlige hastighed for partiklerne i et stof?
Her er hvorfor:
* Gennemsnitlig hastighed er ikke nok: Partikler i et stof bevæger sig tilfældigt i alle retninger. Nogle bevæger sig hurtigt, nogle bevæger sig langsomt. Et simpelt gennemsnit af deres hastigheder ville ikke give en ægte repræsentation af deres samlede kinetiske energi.
* rod-middel-kvadrat: RMS -hastigheden beregnes af:
1. kvadrering Hastigheden for hver partikel.
2. gennemsnit Disse kvadratiske hastigheder.
3. tager kvadratroden af gennemsnittet.
Denne metode giver et mere nøjagtigt mål for den gennemsnitlige kinetiske energi for partiklerne, som er direkte relateret til stoffets temperatur.
Faktorer, der påvirker RMS -hastighed:
* Temperatur: Højere temperatur betyder højere kinetisk energi og derfor højere RMS -hastighed.
* molekylær masse: Lysere molekyler bevæger sig hurtigere end tungere ved den samme temperatur.
Formel for RMS -hastighed:
RMS -hastigheden (v rms ) af en gas er givet af:
v rms =√ (3RT/M)
hvor:
* R er den ideelle gaskonstant
* T er temperaturen i Kelvin
* M er den molære masse af gassen
Denne formel gælder for ideelle gasser, men begrebet RMS -hastighed er vigtigt for at forstå partiklernes opførsel i alle tilstande.
Sidste artikelHvilke er ikke tværgående bølger?
Næste artikelHvad er kraften til tiltrækning mellem genstande afhængigt af masse og afstand?
 Varme artikler
Varme artikler
-
 3D holografisk head-up display kan forbedre trafiksikkerhedenTil venstre:et billede af et træ baseret på LiDAR -data. Til højre:det samme billede gemt i et hologram. Kredit:Jana Skirnewskaja Forskere har udviklet det første LiDAR-baserede augmented reality
3D holografisk head-up display kan forbedre trafiksikkerhedenTil venstre:et billede af et træ baseret på LiDAR -data. Til højre:det samme billede gemt i et hologram. Kredit:Jana Skirnewskaja Forskere har udviklet det første LiDAR-baserede augmented reality -
 Billedteknik lader almindelige kameraer optage højhastighedsbilleder af revnedannelseKredit:CC0 Public Domain Direkte billeddannelse af dynamiske revner, efterhånden som de opstår, kan fortælle os meget om brudens fysik og brudmaterialers egenskaber, hvilket ville gavne mange områ
Billedteknik lader almindelige kameraer optage højhastighedsbilleder af revnedannelseKredit:CC0 Public Domain Direkte billeddannelse af dynamiske revner, efterhånden som de opstår, kan fortælle os meget om brudens fysik og brudmaterialers egenskaber, hvilket ville gavne mange områ -
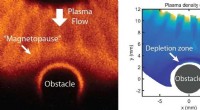 En fantastisk præstation:Magnetiseret rumvind i laboratorietOptiske billeder fra MAGPIE -eksperimenter (til venstre) viser en løsrevet grænse, minder om Jordens magnetopause, dannet, når en model solvind støder på en magnetiseret forhindring. En plasmaudtømnin
En fantastisk præstation:Magnetiseret rumvind i laboratorietOptiske billeder fra MAGPIE -eksperimenter (til venstre) viser en løsrevet grænse, minder om Jordens magnetopause, dannet, når en model solvind støder på en magnetiseret forhindring. En plasmaudtømnin -
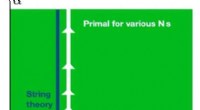 Forskere bruger S-matrix bootstrap til at undersøge, om strengteori er den eneste konsistente teori…Strengteori dækker hele eller næsten hele det tilladte kvantetyngdekraftteorirum. Kredit:Guerrieri, Penedones &Vieira. S-matrix bootstrap er en numerisk metode, der kan bruges til at bestemme elle
Forskere bruger S-matrix bootstrap til at undersøge, om strengteori er den eneste konsistente teori…Strengteori dækker hele eller næsten hele det tilladte kvantetyngdekraftteorirum. Kredit:Guerrieri, Penedones &Vieira. S-matrix bootstrap er en numerisk metode, der kan bruges til at bestemme elle
- Er tyngdekraften en form for energi?
- Hvilken er en bedre leder af varmejern eller alkohol?
- Hvor mange elektroner er der i hver ring på et atom af svovl?
- Hvordan overfører trækvarmeenergi?
- Udbryderpartier truer med at forstyrre Sydkoreas topartisystem. Kan de også bringe den parlamentari…
- Sådan fungerer olieraffinering


