Hvad er det matematiske udtryk for første lov om termodynamik?
ΔU =q - w
Hvor:
* ΔU Repræsenterer ændringen i et systems interne energi.
* q Repræsenterer varmen, der er tilføjet til systemet.
* w repræsenterer det arbejde, der udføres af systemet.
Forklaring:
* intern energi (U): Dette er den samlede energi indeholdt i et system, inklusive kinetisk og potentiel energi fra dets molekyler.
* varme (q): Dette er den energi, der overføres mellem systemet og dets omgivelser på grund af en temperaturforskel.
* arbejde (W): Dette er den energi, der overføres mellem systemet og dets omgivelser på grund af en kraft, der virker på afstand.
Nøglepunkter:
* Den første lov om termodynamik siger, at energi ikke kan skabes eller ødelægges, kun overføres eller transformeres.
* Ligningen udtrykker, at ændringen i et systems interne energi er lig med den varme, der tilføjes systemet minus det arbejde, der udføres af systemet.
* Hvis der tilsættes varme til systemet (q> 0), øges den interne energi (ΔU> 0).
* Hvis arbejdet udføres af systemet (W> 0), falder den interne energi (ΔU <0).
Bemærk:
* Tegnskonventionen for arbejde kan vendes afhængigt af den anvendte definition. Nogle kilder definerer arbejde udført * på * systemet som positivt, mens andre definerer arbejde * af * systemet som positivt.
* Den første lov om termodynamik er et grundlæggende princip i fysik og har vidtgående anvendelser inden for forskellige områder, herunder teknik, kemi og biologi.
Sidste artikelHvilken egenskab ved et objekt kan ikke ændres af en styrke?
Næste artikelHvad er forskellen mellem forskydning og hastighed?
 Varme artikler
Varme artikler
-
 Forskere løser store begrænsninger af stratosfærisk ballon nyttelastBOBCAT nyttelasten hænger fra løfteraketten under test før opsendelse fra Fort Sumner, Ny mexico, i august 2019. Kredit:Nick Bellis Næsten alle fotoner udsendt efter Big Bang er nu kun synlige ved
Forskere løser store begrænsninger af stratosfærisk ballon nyttelastBOBCAT nyttelasten hænger fra løfteraketten under test før opsendelse fra Fort Sumner, Ny mexico, i august 2019. Kredit:Nick Bellis Næsten alle fotoner udsendt efter Big Bang er nu kun synlige ved -
 Stickiness nøglen til bedre diagnostik og lægemidlerKlæbrigheden, eller viskositet, væsker er utrolig vigtig i biologi, Professor Bowen sagde. Kredit:University of Queensland Klæbrigheden, eller viskositet, af mikroskopiske væsker kan nu måles tusi
Stickiness nøglen til bedre diagnostik og lægemidlerKlæbrigheden, eller viskositet, væsker er utrolig vigtig i biologi, Professor Bowen sagde. Kredit:University of Queensland Klæbrigheden, eller viskositet, af mikroskopiske væsker kan nu måles tusi -
 Elektron fanget i handlingenLektor i fysik Igor Litvinyuk i Australian Attosecond Science Facility. Kredit:Griffith University. Australiens hurtigste kamera har afsløret den tid, det tager for molekyler at bryde fra hinanden
Elektron fanget i handlingenLektor i fysik Igor Litvinyuk i Australian Attosecond Science Facility. Kredit:Griffith University. Australiens hurtigste kamera har afsløret den tid, det tager for molekyler at bryde fra hinanden -
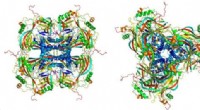 Røntgenimpulser afslører strukturen af viral kokon:Forskere analyserer de mindste proteinkrystal…Atommodel af de krystallinske okklusionslegemer, afledt af røntgendiffraktionsbillederne optaget ved røntgenfri-elektronlaseren LCLS ved SLAC National Accelerator Laboratory. De enkelte proteiner (til
Røntgenimpulser afslører strukturen af viral kokon:Forskere analyserer de mindste proteinkrystal…Atommodel af de krystallinske okklusionslegemer, afledt af røntgendiffraktionsbillederne optaget ved røntgenfri-elektronlaseren LCLS ved SLAC National Accelerator Laboratory. De enkelte proteiner (til


