Sammenlignet med en kold væske, hvordan ville partiklerne i varme væsker bevæge sig?
* Højere kinetisk energi: Partikler i en varm væske har betydeligt mere kinetisk energi end dem i en kold væske. Dette betyder, at de bevæger sig hurtigere Og med mere kraft .
* hyppigere kollisioner: Partiklernes øgede hastighed og energi i en varm væske fører til hyppigere kollisioner med hinanden. Dette bidrager til væskens samlede "travle" natur.
* Større afstand mellem kollisioner: Mens partiklerne kolliderer oftere, betyder den øgede kinetiske energi også, at de rejser længere mellem kollisioner.
* bredere bevægelsesområde: Den hurtigere bevægelse giver partiklerne mulighed for at udforske et større volumen inden for væsken, hvilket fører til mere kaotisk bevægelse.
Analogi: Tænk på et overfyldt rum. I en varm væske er det som om alle løber rundt begejstret og støder ofte på hinanden. I en kold væske er det mere som en langsom, bølgende spadseretur med færre kollisioner.
Nøglepunkter:
* Denne øgede bevægelse i varme væsker er det, der får dem til at udvide (Tag mere plads).
* Forskellen i partikelbevægelse er også det, der fører til varmeoverførsel, da de hurtigere bevægende partikler i en varm væske kolliderer med langsommere bevægende partikler i et køligere objekt og overfører energi.
Sidste artikelHvad får foton til at bevæge sig?
Næste artikelHvordan påvirker afstanden mellem 2 gebyrer dem?
 Varme artikler
Varme artikler
-
 Ny laserteknologi til kemiske sensorer i mikrochipstørrelseLasersystemet udviklet på TU Wien skaber mange frekvenser med lige stor afstand mellem dem. Credit:TU Wien De fleste lasere udsender fotoner med nøjagtig samme bølgelængde, producerer en enkelt fa
Ny laserteknologi til kemiske sensorer i mikrochipstørrelseLasersystemet udviklet på TU Wien skaber mange frekvenser med lige stor afstand mellem dem. Credit:TU Wien De fleste lasere udsender fotoner med nøjagtig samme bølgelængde, producerer en enkelt fa -
 Nye fund bringer fysikere tættere på at forstå dannelsen af planeter og stjernerPPPL-fysiker Kyle Caspary, der har en tendens til magnetorotationel ustabilitetseksperiment. Kredit:Elle Starkman Ned ad en gang i det amerikanske energiministeriums (DOE) Princeton Plasma Physics
Nye fund bringer fysikere tættere på at forstå dannelsen af planeter og stjernerPPPL-fysiker Kyle Caspary, der har en tendens til magnetorotationel ustabilitetseksperiment. Kredit:Elle Starkman Ned ad en gang i det amerikanske energiministeriums (DOE) Princeton Plasma Physics -
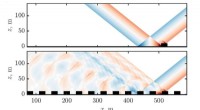 By-kløfter forlænger soniske boom i byerUdbredelse af en N-bølge lydbom over (a) en isoleret bygning og (b) flere bygninger. Kredit:Didier Dragna Tyve år efter Concordes pensionering ønsker flere industri- og forskningsprojekter at gøre
By-kløfter forlænger soniske boom i byerUdbredelse af en N-bølge lydbom over (a) en isoleret bygning og (b) flere bygninger. Kredit:Didier Dragna Tyve år efter Concordes pensionering ønsker flere industri- og forskningsprojekter at gøre -
 Chipbaseret nanoskopi:Mikroskopi i HD-kvalitetNyt billeddannelsespotentiale:Standardopløsning (venstre) i forhold til (center, til højre) høj opløsning og superopløsning opnået med den chipbaserede teknik. Kredit:Bielefeld University/Robin Diekma
Chipbaseret nanoskopi:Mikroskopi i HD-kvalitetNyt billeddannelsespotentiale:Standardopløsning (venstre) i forhold til (center, til højre) høj opløsning og superopløsning opnået med den chipbaserede teknik. Kredit:Bielefeld University/Robin Diekma
- Hvor varmt eller koldt er et stof?
- Ny elektronmikroskopiteknik giver første kig på tidligere skjulte processer
- Uber, Cabify stopper tjenester i Barcelona på grund af strammere love
- Karakteristika ved planter og dyr
- Når en ballon opvarmes, fordobles dens volumen, hvad sker der med densitet?
- Hvor mange milligram er 30x lig med?


