Hvornår bevæger partikler sig hurtigere?
1. Højere temperatur: Den mest grundlæggende faktor, der påvirker partikelhastigheden, er temperatur . Når temperaturen stiger, øges den gennemsnitlige kinetiske energi af partiklerne, hvilket fører til hurtigere bevægelse.
2. Nedre masse: For en given temperatur vil lettere partikler bevæge sig hurtigere end tungere partikler. Dette skyldes, at kinetisk energi er proportional med både masse og hastighed kvadrat.
3. Mindre intermolekylære kræfter: Partikler i gasser bevæger sig hurtigere end dem i væsker, og partikler i væsker bevæger sig hurtigere end dem i faste stoffer. Dette skyldes, at intermolekylære kræfter (attraktive kræfter mellem molekyler) er svagere i gasser og stærkere i faste stoffer og begrænser bevægelse.
4. Nedsat viskositet: I væsker Viskositet (Modstand mod flow) kan påvirke partikelhastigheden. Nedre viskositet gør det muligt for partikler at bevæge sig mere frit.
5. Øget tryk (for gasser): I gasser øget tryk kan føre til hurtigere partikelbevægelse på grund af hyppigere kollisioner. Dette er dog en mindre signifikant faktor sammenlignet med temperatur.
Vigtig note: Ovenstående faktorer beskriver hovedsageligt gennemsnitlig hastighed af partikler. I virkeligheden bevæger partikler i et stof konstant i forskellige hastigheder, og deres hastigheder ændrer sig konstant på grund af kollisioner.
Fortæl mig, hvis du gerne vil have mig til at uddybe nogen af disse punkter!
Sidste artikelHvad angår deres lov om planetarisk bevægelsesstat?
Næste artikelHvilken type bølge er en mekanisk bølge?
 Varme artikler
Varme artikler
-
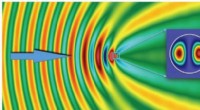 Kæmpe forbedring af elektromagnetiske bølger afsløret i små dielektriske partiklerMagnetfeltets intensitet ved spredning af en elektromagnetisk bølge. Hændelsesbølgen formerer sig fra venstre mod højre, som den er angivet med den blå pil. Farvebjælken har forskellige skalaer for fe
Kæmpe forbedring af elektromagnetiske bølger afsløret i små dielektriske partiklerMagnetfeltets intensitet ved spredning af en elektromagnetisk bølge. Hændelsesbølgen formerer sig fra venstre mod højre, som den er angivet med den blå pil. Farvebjælken har forskellige skalaer for fe -
 Ny type lysinteraktion med atomer giver mulighed for at manipulere skyformKredit: Fysisk gennemgangsbreve (2017). DOI:10.1103/PhysRevLett.119.163201 Et team af forskere ved Weizmann Institute of Science i Israel har fundet en ny måde at manipulere atomer ved hjælp af l
Ny type lysinteraktion med atomer giver mulighed for at manipulere skyformKredit: Fysisk gennemgangsbreve (2017). DOI:10.1103/PhysRevLett.119.163201 Et team af forskere ved Weizmann Institute of Science i Israel har fundet en ny måde at manipulere atomer ved hjælp af l -
 Forskere er ved at optrevle mysteriet om tidens pilKredit:Pixabay/CC0 Public Domain Tidens flow fra fortiden til fremtiden er et centralt træk ved, hvordan vi oplever verden. Men præcis hvordan dette fænomen, kendt som tidens pil, opstår fra de mik
Forskere er ved at optrevle mysteriet om tidens pilKredit:Pixabay/CC0 Public Domain Tidens flow fra fortiden til fremtiden er et centralt træk ved, hvordan vi oplever verden. Men præcis hvordan dette fænomen, kendt som tidens pil, opstår fra de mik -
 Præcisionseksperiment først for at isolere, måle svag kraft mellem protoner, neutronerForskere analyserede gammastrålerne udsendt under NPDGamma-eksperimentet og fandt paritetskrænkende asymmetri, som er en specifik ændring i adfærd i kraften mellem en neutron og en proton. De målte en
Præcisionseksperiment først for at isolere, måle svag kraft mellem protoner, neutronerForskere analyserede gammastrålerne udsendt under NPDGamma-eksperimentet og fandt paritetskrænkende asymmetri, som er en specifik ændring i adfærd i kraften mellem en neutron og en proton. De målte en
- Koordinationspolymerkrystaller viser lovende som ny generation af lyskilder til industri, medicin
- Hvad er Aegyptopithecus?
- Hvilke ting er lavet af elektricitet?
- Hvad får du, når du multiplicerer en objektermasse ved acceleration?
- Hvordan adskiller bakker sig fra bjerge?
- Gammel dovendyr fundet at være blevet bidt af gammel krokodille


