Infrarød spektroskopi:Beregning af vibrationsfrekvenser og kraftkonstanter
Beregning af fundamental vibrationsfrekvens og kraftkonstant fra infrarød spektroskopi
Infrarød (IR) spektroskopi giver information om molekylers vibrationstilstande. Ved at analysere absorptionstoppene i IR-spektret kan vi udtrække information om de fundamentale vibrationsfrekvenser og kraftkonstanter.
Sådan gør du:
1. Identifikation af absorptionstoppene:
- Opnå et IR-spektrum: Optag IR-spektret for molekylet af interesse.
- Find absorptionstoppene: Identificer toppene i spektret, der svarer til vibrationstilstande. Disse toppe vises normalt som fald i transmissionen af IR-lys.
2. Beregning af den fundamentale vibrationsfrekvens:
- Tildel toppene: Identificer, hvilken top der svarer til den specifikke vibrationstilstand, du er interesseret i. Dette kan involvere konsultation af databaser, teoretiske beregninger eller sammenligning med lignende molekyler.
- Konverter bølgenumre til frekvens: IR-spektret er typisk afbildet i bølgetal (cm⁻¹). For at opnå vibrationsfrekvensen (ν) i Hertz (Hz), skal du bruge følgende ligning:
ν =c * ν̃
hvor:
* c er lysets hastighed (2.998 x 10⁸ m/s)
* ν̃ er bølgetallet i cm⁻¹
3. Beregning af kraftkonstanten:
- Anvend Hooke's Law-modellen: For et diatomisk molekyle kan vibrationsfrekvensen relateres til kraftkonstanten (k) ved hjælp af Hookes lov:
ν =(1 / 2π) * √(k/μ)
hvor:
* μ er den reducerede masse af det diatomiske molekyle. Det beregnes som:μ =(m₁ * m₂) / (m₁ + m₂)
* m₁ og m₂ er masserne af de to atomer i det diatomiske molekyle.
- Løs kraftkonstanten: Omarranger ovenstående ligning for at opnå kraftkonstanten:
k =4π²μν²
4. Begrænsninger og overvejelser:
- Forenkling: Hooke's Law-modellen er en forenkling. Det antager et harmonisk potentiale, som ikke altid er nøjagtigt for rigtige molekyler.
- Anharmonicitet: Reelle molekyler udviser anharmonicitet, hvor den potentielle energi ikke er strengt kvadratisk. Dette fører til overtoner og kombinationsbånd i IR-spektret.
- Polyatomiske molekyler: For polyatomiske molekyler bliver analysen mere kompleks, hvilket kræver forståelse af normale tilstande og gruppeteori.
Eksempel:
Lad os sige, at du har et diatomisk molekyle CO med en absorptionstop på 2143 cm⁻¹ i dets IR-spektrum.
- Hyppighed: ν =c * ν̃ =(2,998 x 10⁸ m/s) * (2143 cm⁻¹) =6,42 x 10¹³ Hz
- Reduceret masse: μ =(12.011 u * 15.999 u) / (12.011 u + 15.999 u) =6.857 u
* Bemærk:'u' er atommasseenheden, hvor 1 u ≈ 1,66054 x 10⁻²⁷ kg.
- Tvingskonstant: k =4π²μν² =4π² * (6,857 * 1,66054 x 10⁻²⁷ kg) * (6,42 x 10¹³ Hz)² ≈ 1,90 x 10³ N/m
Bemærk: Kraftkonstanten giver information om styrken af bindingen i molekylet. En højere kraftkonstant indikerer en stærkere binding.
Konklusion:
Ved at analysere IR-spektret kan vi opnå de fundamentale vibrationsfrekvenser og estimere kraftkonstanter for molekyler. Denne information er afgørende for at forstå strukturen og dynamikken af molekyler og har anvendelser inden for forskellige områder som kemi, materialevidenskab og biokemi.
Sidste artikelForstå materiens tilstande:væskers egenskaber
Næste artikelRutherfords guldfolieeksperiment:bevis for atomkernen
 Varme artikler
Varme artikler
-
 Ensartet teori forklarer, hvordan materialer omdannes fra faste stoffer til væskerSlimlaget på undersiden af en sneglefod er et eksempel på et blødt materiale, der giver efter for stress op til et vist punkt, så flyder. denne adfærd, forenklet i en ny undersøgelse fra forskere ve
Ensartet teori forklarer, hvordan materialer omdannes fra faste stoffer til væskerSlimlaget på undersiden af en sneglefod er et eksempel på et blødt materiale, der giver efter for stress op til et vist punkt, så flyder. denne adfærd, forenklet i en ny undersøgelse fra forskere ve -
 Undersøgelse af elektroner med et traditionelt scanningsmikroskopKvantekohærent elektron-lys-kobling i en ultrahurtig SEM. Elektroner fotoemitteret af ultraviolette laserimpulser (lilla) forplanter sig gennem søjlen på en kommerciel SEM. Elektronstrålen (grøn) er f
Undersøgelse af elektroner med et traditionelt scanningsmikroskopKvantekohærent elektron-lys-kobling i en ultrahurtig SEM. Elektroner fotoemitteret af ultraviolette laserimpulser (lilla) forplanter sig gennem søjlen på en kommerciel SEM. Elektronstrålen (grøn) er f -
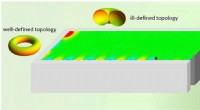 At standse en bølge i dens sporI et system med en dårligt defineret topologi kan antallet af kantbølger, der udbreder sig indad til et eller andet samlingspunkt, være forskelligt fra antallet af kantbølger, der udbreder sig i udadg
At standse en bølge i dens sporI et system med en dårligt defineret topologi kan antallet af kantbølger, der udbreder sig indad til et eller andet samlingspunkt, være forskelligt fra antallet af kantbølger, der udbreder sig i udadg -
 Udforske kilden til stjerner og planeter i et laboratoriumFysiker Himawan Winarto med figurer fra papir bag sig. Kredit:Elle Starkman/PPPL Office of Communications. En ny metode til at verificere en udbredt, men ubevist teoretisk forklaring på dannelsen
Udforske kilden til stjerner og planeter i et laboratoriumFysiker Himawan Winarto med figurer fra papir bag sig. Kredit:Elle Starkman/PPPL Office of Communications. En ny metode til at verificere en udbredt, men ubevist teoretisk forklaring på dannelsen
- Hyundai viser gangvognsprojekt
- Hvad er blokbjerge?
- Ny undersøgelse afslører en beregningsstyret tilgang til at undertrykke kræfttumorvækst
- Hvad er et katalysatorkontrolcenter?
- Nuklear overførsel og udvikling:Genetisk informations rolle
- NASAs nyligt genopdagede IMAGE-mission leverede vigtig auroraforskning


