Ny undersøgelse afslører en beregningsstyret tilgang til at undertrykke kræfttumorvækst
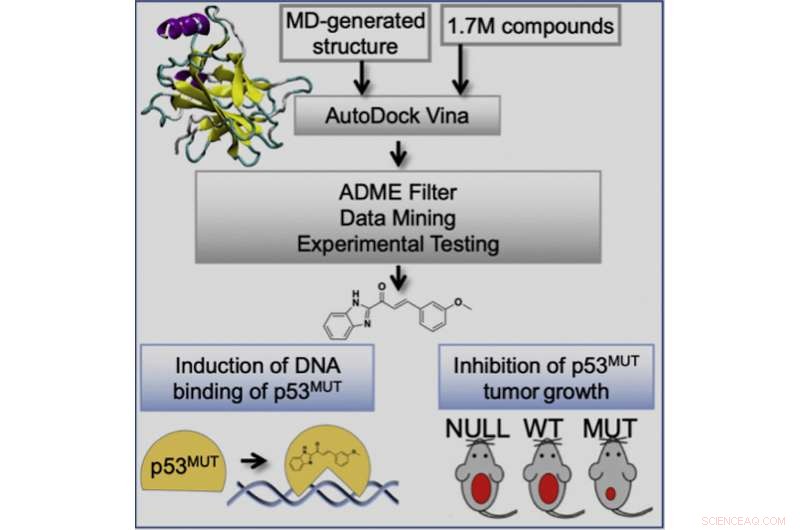
Grafisk abstrakt. Kredit:Geetha Durairaj et al., Cell Chemical Biology (2022). DOI:10.1016/j.chembiol.2022.07.003
En ny undersøgelse, ledet af forskere fra University of California, Irvine og University of California, San Diego, afslører en ny beregningsstyret tilgang til at identificere små molekyler, der kan genoprette aspekter af vildtype p53-tumorundertrykkelsesfunktion til muteret p53, som spiller en vigtig rolle i mange kræftformer hos mennesker. Denne fremgangsmåde var vellykket både in vitro og in vivo. Denne strategi kan øge den kemiske mangfoldighed af p53-korrektormolekyler til klinisk udvikling.
Tumorsuppressoren p53 er en af de mest kraftfulde mekanismer, organismer bruger til at beskytte sig mod kræft. Elefanter har flere kopier af p53-genet og får sjældent kræft. Mennesker har kun én kopi, og det er det mest muterede gen, der findes i kræft hos mennesker. Forskellige terapeutiske tilgange forfølges aktivt for at målrette denne vej.
"Interessant nok er en stor del af p53-ændringer missense-mutationer, hvor den genetiske kode for p53 ændres på en måde, der producerer en anden aminosyre, end den normalt ville," forklarede Peter Kaiser, Ph.D., professor og formand for Institut for Biologisk Kemi ved UCI School of Medicine. "Dette resulterer i overflod af mutant p53-proteinniveauer i tumorer, der i princippet er modtagelige for en korrigerende lægemiddeltilgang."
Udgivet i Cell Chemical Biology , identificerede undersøgelsen små lægemiddellignende forbindelser, der virker gennem en veldefineret virkemåde; kræver ikke kovalent binding, induktion af redox-ubalance eller metalbinding; og har selektive anti-cancer aktiviteter på tumorer med p53 missense mutationer. Denne forskning tilvejebringer en ramme for opdagelse af p53-reaktiveringsforbindelser, der kan bidrage til at øge den kemiske diversitet og forbedre de farmakologiske egenskaber, der er nødvendige for oversættelse af farmaceutisk p53-mutant-reaktivering til klinikken.
"Denne undersøgelse viser succesfuldt gennemførligheden og effektiviteten af farmaceutisk reaktivering af mutant p53," sagde Kaiser. "Disse resultater er opmuntrende i betragtning af det store antal kræftpatienter med p53-mutationer, som kunne drage fordel af sådanne lægemidler."
Denne undersøgelse involverede anvendelsen af en ensemble-baseret virtuel screening tilgang, udviklet i laboratoriet af Rommie Amaro, professor og begavet formand i Institut for Kemi og Biokemi ved UC San Diego, som har potentialet til at identificere forbindelser med øget kræftdræbende potentiale og med et bredt spektrum af aktivitet på tværs af et panel af p53-mutanter. Forskerne viste, at deres forbindelser binder mutant p53 og ændrer mutant p53-konformation til vildtype-lignende strukturer. Dette genopretter p53 DNA-bindingsaktivitet for at aktivere p53-transkriptionsresponset, hvilket igen forhindrer tumorprogression i musemodeller selektivt for tumorer med en p53 missense-mutation.
Der er fortsat udfordringer med at definere nøjagtige mekanismer og udvikle meget aktive korrektorlægemidler til muteret p53, og fremtidige eksperimenter er nødvendige for at optimere farmakologiske egenskaber for at udvikle sig mod klinisk terapeutik. + Udforsk yderligere
Det kræver mere end én mutant kopi af PIK3CA-genet for at gøre brystkræft mere aggressiv
 Varme artikler
Varme artikler
-
 Metoder til vandrensningHvilke mange fattige mennesker, backcountry vandrere og dem, der bor i fjerntliggende områder, har til fælles en afhængighed af ubehandlede lokale vandkilder, der kan være forurenet og skal renses, fø
Metoder til vandrensningHvilke mange fattige mennesker, backcountry vandrere og dem, der bor i fjerntliggende områder, har til fælles en afhængighed af ubehandlede lokale vandkilder, der kan være forurenet og skal renses, fø -
 Team skaber bedre fingeraftryk for at opdage undvigende, værdifulde kemiske forbindelserBálint Sztáray, venstre, fra University of the Pacific, og Sandia National Laboratories kemiker David Osborn viser PEPICO-instrumentet. Kredit:Sandia National Laboratories Forestil dig at kunne se
Team skaber bedre fingeraftryk for at opdage undvigende, værdifulde kemiske forbindelserBálint Sztáray, venstre, fra University of the Pacific, og Sandia National Laboratories kemiker David Osborn viser PEPICO-instrumentet. Kredit:Sandia National Laboratories Forestil dig at kunne se -
 Tryk kan være nøglen til at bekæmpe klimaændringer med termoelektriske generatorerKunstners opfattelse af, hvordan påføring af tryk i diamantamboltcellen ændrer den elektroniske struktur af bly -selenid. Kredit:Xiao-Jia Chen Tryk forbedrer materialers evne til at omdanne varme
Tryk kan være nøglen til at bekæmpe klimaændringer med termoelektriske generatorerKunstners opfattelse af, hvordan påføring af tryk i diamantamboltcellen ændrer den elektroniske struktur af bly -selenid. Kredit:Xiao-Jia Chen Tryk forbedrer materialers evne til at omdanne varme -
 Karakteristika ved gode buffereEn puffer er en vandbaseret opløsning indeholdende en blanding af enten en syre og dens konjugatbase eller en base og dens konjugatsyre. De syrer og baser, der bruges i en buffer, er ret svage, og
Karakteristika ved gode buffereEn puffer er en vandbaseret opløsning indeholdende en blanding af enten en syre og dens konjugatbase eller en base og dens konjugatsyre. De syrer og baser, der bruges i en buffer, er ret svage, og
- Reaktionstype med kobber & salpetersyre
- Amazon sænker det månedlige gebyr for at øge salget af dagligvarelevering
- Ny opdagelse om meteoritter informerer om vurdering af atmosfærisk indtrængning
- En teoretisk forklaring på en forbedret termisk Hall-respons i høj-temperatur superledere
- Undersøgelse:Landbrugssamfundet godkender afgrøder og bæredygtig forvaltningspraksis valgt til di…
- Sådan beregnes lagerstørrelse


