Hvordan man laver methan Gas
Metan (CH4) er en farveløs, lugtfri gas ved standardtryk og er den primære bestanddel af naturgas. Det er en attraktiv brændstofkilde, fordi den brænder rent og er relativt rigelig. Metan bruges også i vid udstrækning i industriel kemi, da det er forløberen for mange kemiske reaktioner. Methan ekstraheres kommercielt fra naturgas og kul og kan også fremstilles ud fra en række kemiske reaktioner. Landmændene kan også få metan i mindre omfang fra husdyrgødning og kompost.
Udvind methan fra naturgas. Naturgas er ca. 75 procent methan, og udvindingsprocessen består i at fjerne alle de øvrige komponenter i naturgassen. Dette er en kompleks flertrinsproces, der fjerner gasser med specifikke egenskaber på hvert trin.
Fremstil methan ved brænding af kul. Råkul indeholder mindst 15 procent brændbart materiale, der kaldes bituminøst kul. Brændende bituminøst kul producerer methan i kommercielle mængder sammen med andre gasser som ammoniak, kuldioxid og benzen blandt mange andre.
Hent methan med Sabatier reaktionen. Denne metode blander kuldioxid med hydrogen for at fremstille methan og vand. Sabatier-reaktionen kan bruge nikkel som katalysator for at fremskynde reaktionen til en kommercielt rentabel hastighed.
Hent metan fra biogas. De bakterier, der gærer gødning, kompost og andet organisk stof i fravær af ilt producerer gylle som et biprodukt. Denne metode er generelt ikke økonomisk i kommerciel skala, men kan være en effektiv metode til genanvendelse af affaldsprodukter.
Find methan fra alternative kilder. Methanhydrater er tilgængelige i store mængder på havbunden og kan i fremtiden give en økonomisk kilde til metan.
Sidste artikelSådan beregnes den gennemsnitlige naturligt forekommende atommasseprocent
Næste artikelHvordan er saltet krystalliseret?
 Varme artikler
Varme artikler
-
 Hvilke elementer udgør luften, vi indånder?Jordens atmosfære er så stor som den er usynlig. En enorm boble af gasser omgiver jorden, som mennesker og dyr er afhængige af for at forblive i live, men ikke ser eller interagere med bevidsthed. På
Hvilke elementer udgør luften, vi indånder?Jordens atmosfære er så stor som den er usynlig. En enorm boble af gasser omgiver jorden, som mennesker og dyr er afhængige af for at forblive i live, men ikke ser eller interagere med bevidsthed. På -
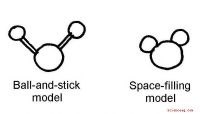 Hvordan man laver en model af Molecular Structure of WaterVand er det mest studerede molekyle i hele videnskaben. Det er et simpelt molekyle, der består af kun ét oxygenatom og to hydrogenatomer. Det er et af de nemmeste atomer at bygge en model af, og er de
Hvordan man laver en model af Molecular Structure of WaterVand er det mest studerede molekyle i hele videnskaben. Det er et simpelt molekyle, der består af kun ét oxygenatom og to hydrogenatomer. Det er et af de nemmeste atomer at bygge en model af, og er de -
 Tips til at huske stærke syrer og baserHvis du skal huske navnene på stærke syrer og baser til en kemiundersøgelse, skal du ikke få panik. Hvis enkel gentagelse ikke fungerer, kan du prøve at skrive lister eller bruge en mnemonic til at
Tips til at huske stærke syrer og baserHvis du skal huske navnene på stærke syrer og baser til en kemiundersøgelse, skal du ikke få panik. Hvis enkel gentagelse ikke fungerer, kan du prøve at skrive lister eller bruge en mnemonic til at -
 Hvad er forskellen mellem molmasse og molekylvægt?Molmasse og molekylvægt forveksles ofte, men deres værdier er meget forskellige. Molmasse er massen af en mol af et stof, mens molekylvægt er massen af et molekyle af et stof. En mol er antalle
Hvad er forskellen mellem molmasse og molekylvægt?Molmasse og molekylvægt forveksles ofte, men deres værdier er meget forskellige. Molmasse er massen af en mol af et stof, mens molekylvægt er massen af et molekyle af et stof. En mol er antalle


